中国科学院微生物研究所、中国微生物学会主办
文章信息
- 刘欢, 孟颖颖, 牛丽芳, 林浩
- Liu Huan, Meng Yingying, Niu Lifang, Lin Hao
- 基因编辑技术研究进展及其在苜蓿等豆科饲草作物中的应用
- Genome editing technology and its application in forage legumes
- 生物工程学报, 2017, 33(10): 1733-1743
- Chinese Journal of Biotechnology, 2017, 33(10): 1733-1743
- 10.13345/j.cjb.170169
-
文章历史
- Received: April 24, 2017
- Accepted: June 12, 2017
近年来,基因编辑技术的快速发展为生物学研究开辟了新的研究领域。基因编辑技术是基于序列特异核酸酶在基因组水平上对靶标基因进行定向、准确修饰的一种新兴的基因工程方法[1-3]。序列特异性核酸酶通过识别和锚定基因组上的靶标位点序列,对目标DNA进行切割产生双链断裂(Double strand breaks,DSBs),引起生物体内发生同源重组(Homologous recombination,HR)或非同源末端连接(Non homologous end joining,NHEJ)进行修复,造成基因组特定位点出现碱基缺失或插入进而实现对基因组的定向修饰[4-5]。目前,已成功发展的基因编辑技术主要包括锌指核酸酶(Zinc finger nucleases,ZFNs)技术[6-7]、类转录激活子效应蛋白核酸酶(Transcription activator-like effector nucleases,TALENs)技术[8-9]、巨核酶(Meganucleases,MGNs)技术[10]以及新近发展的CRISPR/Cas系统(The clustered regularly interspersed short palindromic repeats/CRISPR-associated)[11-14]。其中CRISPR/Cas基因编辑技术由于具有操作简单、编辑高效、成本低廉等优点,目前已广泛应用于拟南芥、烟草、西红柿、马铃薯、水稻、小麦、玉米等植物和主要农作物的基因功能研究和重要农艺性状遗传改良[15-23]。
优化调整种植业结构,支持饲料作物种植,促进粮食作物、经济作物、饲料作物三元种植结构协调发展是我国新形势下应对居民膳食结构改变、缓解粮食供求矛盾的重要举措。享有“牧草之王”美誉的紫花苜蓿Medicago sativa是世界上应用最广、经济价值最高和栽培面积最大的一种优质豆科饲料作物。苜蓿的产量和品质改良是我国当前饲料业、畜牧业和奶业发展的重大迫切需求。与水稻、小麦、玉米、大豆等主要粮食作物和经济作物相比,目前苜蓿等饲草作物功能基因组学研究尚处于起步阶段,相应的基因功能研究和分子遗传改良的研究工具和技术手段有限,极大地限制了饲草作物分子育种技术的应用与发展。本文简要回顾ZFN、TALEN、MGN以及CRISPR/Cas9等基因编辑技术的发展历程,重点介绍新近发展的CRISPR/Cas9技术在植物中的研究进展,并对该基因编辑技术在苜蓿等饲草作物中的应用进行探讨和展望,希望为苜蓿等豆科饲草作物的功能基因组学研究及遗传改良提供新的研究思路。
1 基因编辑技术的发展历程 1.1 ZFN基因编辑技术ZFN是一种人工改造的核酸酶,由负责特异性识别靶标序列的锌指蛋白DNA结合域(Zinc finger DNA-binding domain)和TypeⅡS类限制酶FokⅠ[24] C端的非特异性DNA切割结构域两部分组合而成[25]。通过定向改造ZFN锌指DNA结合域的序列识别特异性,可以实现ZFN特异性地结合生物基因组中的靶标基因序列,并利用FokⅠ的DNA切割结构域进行剪切,达到基因编辑的目的[6, 26]。1996年,Kim等首先报道了将锌指蛋白连接到FokⅠ的DNA切割结构域可以产生1个新型的有活性的位点识别特异性核酸酶,并且该人工改造的新型锌指核酸酶可以特异性地切割DNA序列[25],标志着ZFN基因编辑技术的出现。
目前最常用的ZF (Zinc finger)结构为Cys2-His2锌指,大约由30个氨基酸包裹1个锌原子构成,每个锌指蛋白结构域能够特异性地识别和结合3个核酸碱基[27]。研究表明,通过增加锌指蛋白的数量可以扩大ZFN识别靶标DNA序列的长度,进而提高其序列识别特异性[28]。FokⅠ是一种TypeⅡS限制核酸酶,由于FokⅠ仅在二聚体状态下才具备核酸酶活性,因此通常针对1个靶位点需要设计一对ZFNs,并且二者结合序列的间隔区域保持在6−8 bp以确保FokⅠ二聚体的形成[29]。ZFN利用锌指结构域特异性地结合目标DNA序列,并通过FokⅠ的DNA切割结构域对靶位点进行切割,导致目标DNA双链断裂,进而利用细胞内的同源重组或非同源末端连接等修复机制实现目标基因的靶向敲除[6, 30-31]。目前ZFN技术已成功应用于拟南芥、烟草、玉米和大豆等植物基因编辑[2, 32]。
1.2 TALEN基因编辑技术TALEN技术是第二代人工改造核酸酶技术,TALEN的构成与ZFN相似,由TAL效应因子(Transcription activator-like effector)的DNA结合域与核酸酶FokⅠ的DNA切割结构域两部分组成[33]。TAL效应因子是黄单胞属Xanthomonas植物病原菌分泌的一种细菌侵染植物的效应蛋白,第一个TAL效应因子AvrBs3于1989年在野油菜辣椒斑点病菌中被发现[34]。TAL效应因子含有串联重复的核心结构域、核定位信号(Nuclear localization signal,NLS)和转录激活区(Acidic activation domain,AD)[35-37],其中串联重复的核心结构域具有特异性识别和结合DNA的功能,每个串联重复单元通常由34个氨基酸组成,且不同单元的氨基酸序列高度保守,仅在12位和13位氨基酸上存在差异,被称为重复可变双氨基酸残基(Repeat variable di-residue,RVD)[38]。RVD决定了重复单元的DNA识别特异性:Asn/Ile (NI)识别A,Asn/Gly (NG)识别T,His/Asp (HD)识别C,Asn/Asn (NN)识别G和A,Asn/Lys (NK)识别G[37-40]。TAL串联重复结构域中的RVD与靶标DNA序列之间的对应关系,使得TAL效应子的串联重复单元可以替换ZFN的DNA识别元件,从而发展了新型的基因定点编辑工具TALEN[41-44]。
与ZFN技术相比,TALEN基因编辑技术具有更高的DNA识别特异性,同时TALEN的靶标位点设计灵活方便,模块组装具有极大的便捷性。目前科研人员利用TALEN技术已成功实现对烟草、水稻等多种植物的基因编辑[2, 32],并创制出对白粉病具有广谱抗性的小麦材料[45]。
1.3 MGN基因编辑技术MGN基因编辑技术也是一种基因工程改造的核酸酶技术,MGN是一种能够识别大于12个碱基长度特异核酸序列的归巢核酸内切酶,包含保守的DNA结合结构域和酶切活性结构域,广泛存在于生物体体内[46]。通过对MGN的DNA结合结构域进行改造,可以实现特异性目标DNA序列的识别并进行基因编辑[10]。
与ZFN或TALEN不同,归巢核酸内切酶识别的目标DNA序列较长且具有很强的特异性,因此MGN改造起来难度较大,任何DNA结合结构域的改变都有可能影响目标DNA序列的识别和切割。由于MGN的基因工程改造成本较高,MGN技术的研发和应用主要集中在生物公司。目前已有研究报道MGN技术可应用于玉米等作物的基因组修饰[47]。
1.4 CRISPR/Cas基因编辑技术CRISPR/Cas是细菌和古细菌在长期进化过程中应对外来病毒和DNA入侵而形成的一种免疫应答反应系统[48-54]。1987年大阪大学(Osaka University)的研究人员报道了细菌基因组中存在成簇的规律间隔的短回文重复序列(CRISPR)[52],随后发现在CRISPR附近区域还存在高度保守的CRISPR相关蛋白Cas[53],并证明Cas蛋白具有核酸酶活性,可以对DNA序列进行特异性切割[54]。CRISPR/Cas系统通过将入侵的噬菌体和质粒DNA的片段整合到CRISPR序列中,并利用CRISPR RNA (crRNA)来指导同源序列的降解。根据功能元件的不同,可以将CRISPR/Cas系统分为TypeⅠ、TypeⅡ、Type Ⅲ三种类型,其中TypeⅡ类型CRISPR/Cas9系统最为简单,由pre-crRNA、tracrRNA和Cas9蛋白构成[12],该系统的作用原理是tracrRNA与pre-crRNA结合,随后在Cas9存在的条件下,RNase Ⅲ完成对pre-crRNA/tracrRNA的切割,进而形成成熟的crRNA-tracrRNA-Cas9复合体对靶位点DNA序列进行剪切,产生DNA双链断裂[13-14]。
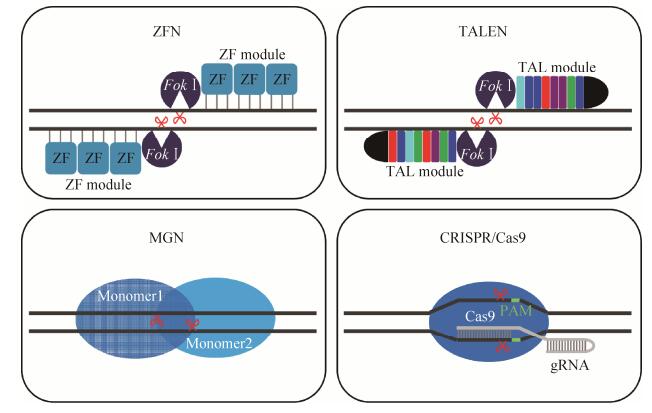
2012年Jinek等将tracrRNA和crRNA表达为一条嵌合的向导RNA (Single guide RNA,sgRNA),并在体外证明sgRNA可以发挥tracrRNA和crRNA的功能[55]。改造后的CRISPR/Cas9系统主要由sgRNA和Cas9蛋白构成,Cas9在sgRNA的指引下对基因组的PAM基序(Protospacer adjacent motifs)上游进行定点切割[12]。通常PAM位点由3个保守的核苷酸NGG (N可以为任何氨基酸)[13]组成。由于CRISPR的sgRNA识别序列一般仅需20个核苷酸左右,且Cas9蛋白不需要形成蛋白二聚体起作用,因此CRISPR/Cas9系统与ZFN、TALEN和MGN等技术相比具有构建简单、编辑高效等优点,目前已广泛应用于动植物等基因组编辑研究[12, 14, 56]。图 1所示为ZFN、TALEN、MGN以及CRISPR/Cas9技术的原理示意图。此外,由于Cas9能够共定位RNA、DNA和蛋白,从而拥有巨大的改造和应用潜力[14]。
|
| 图 1 ZFN、TALEN、MGN以及CRISPR/Cas9基因编辑技术原理示意图 Figure 1 Schematic presentation of ZFN, TALEN, MGN and CRISPR/Cas9 methods for genome editing. |
| |
CRISPR/Cas基因编辑技术一经面世就受到植物科学家的广泛关注。2013年Nature Biotechnology杂志同时报道利用CRISPR/Cas9技术可以在双子叶植物拟南芥、烟草和单子叶作物水稻、小麦中成功实现基因编辑。Li等和Nekrasov等研究人员分别利用植物密码子优化的CRISPR/Cas9系统成功实现对拟南芥和烟草中的PDS基因进行定点敲除,同时发现烟草的编辑效率明显高于拟南芥[57-58],表明CRISPR/Cas9系统对于不同植物的编辑效率存在差异。Shan等科研人员利用CRISPR/Cas9系统分别定点突变了水稻和小麦两个作物中的OsPDS和TaMLO等5个基因,并且在T0代获得了水稻纯合pds突变体,呈现预期的白化和矮小表型,该研究证实CRISPR/Cas9系统能够应用于水稻等单子叶作物的基因组编辑[59]。此后,CRISPR/Cas9系统被陆续报道成功应用于拟南芥、烟草、水稻、小麦、玉米、高粱、番茄等多种植物和农作物中[15-23]。表 1所示为本文中介绍的CRISPR/Cas9技术在一些主要植物和作物中的应用情况。
| Plant species | Target genes | Gene editing type | References |
| Arabidopsis thaliana | AtPDS3, AtFLS2 | Site-specified knockout | [57] |
| Nicotiana benthamiana | NbPDS | Site-specified knockout | |
| Nicotiana benthamiana | NbPDS | Site-specified knockout | [58] |
| Oryza sativa | OsPDS, OsBADH2 et al | Site-specified knockout | [59] |
| Triticum aestivum | TaMLO | Site-specified knockout | |
| Oryza sativa | CAO1, LAZY1 | Site-specified knockout | [15] |
| Oryza sativa | ROC5, SPP, YSA | Site-specified knockout | [16] |
| Arabidopsis thaliana | BRI1, JAZ, GAI | Site-specified knockout | |
| Sorghum bicolor | DsRED2 | Site-specified knockout | [21] |
| Solanum lycopersicum | SlAGO7 | Site-specified knockout | [22] |
| Solanum tuberosum | StIAA2 | Site-specified knockout | [19] |
| Zea mays | LIG1, Ms26 et al | Site-specified knockout | [17] |
| Glycine max | GS1, CHI | Site-specified knockout | [68] |
| Medicago truncatula | MtPDS | Site-specified knockout | [70] |
| Zea mays | LIG | Gene replacement and insertion | [17] |
| Glycine max | DD20, DD43 | Gene replacement and insertion | [60] |
| Oryza sativa | EPSPS | Gene replacement and insertion | [61] |
| Arabidopsis thaliana | AtRACK1b, AtRACK1c | Multiplex gene knockout | [57] |
| Arabidopsis thaliana | TRY, CPC, ETC2 | Multiplex gene knockout | [62] |
| Arabidopsis thaliana | mTERF et al | Multiplex gene knockout | [63] |
| Oryza sativa | 46 genomic targets | Multiplex gene knockout | |
| Lotus japonicus | LjLb1, LjLb2, LjLb3 | Multiplex gene knockout | [69] |
| Oryza sativa | OsSBEIIb, OsPDS | Precise base editing | [65] |
| Oryza sativa | OsCDC48, OsNRT1.1B, OsSPL14 | Precise base editing | [66] |
| Zea mays | ZmCENH3 | Precise base editing | |
| Triticum aestivum | TaLOX2 | Precise base editing |
利用基因编辑技术实现基因组水平的基因定点插入和精确替换对于植物遗传改良具有重要的应用意义。2015年Svitashev等和Li等利用CRISPR/Cas9技术分别在玉米和大豆中实现基因定点插入和替换[17, 60]。2016年,中国科学院遗传与发育研究所的研究人员通过非同源末端修复(NHEJ)途径开发了一种内含子介导的位点特异性基因定点插入和替换方法,通过使用一对靶向相邻内含子的sgRNA和包含同一对sgRNA位点的供体DNA模板,在水稻中实现了5-烯醇丙酮酸莽草酸-3-磷酸合酶(5-enolpyruvylshikimate-3-phosphate synthase,EPSPS)基因的定点替换[61]。该研究拓展了CRISPR/Cas9技术在植物中的应用,为植物基因功能的解析和农作物分子设计育种提供了一个全新的技术路线。
2.3 多基因敲除作物的重要农艺性状通常受到多基因调控,因此开发多基因CRISPR定点编辑技术对于解析作物重要农艺性状形成的遗传基础非常重要。Li等利用拟南芥原生质体系统研究发现CRISPR/Cas9可以实现多基因敲除[57]。Xing等于2014年开发了基于pGreen或pCAMBIA骨架的CRISPR/Cas9载体,可以在1个克隆步骤中同时产生Cas9蛋白和1个或多个gRNA的表达载体,并利用该套CRISPR载体成功获得可以稳定遗传的多基因敲除突变体,表明CRISPR/Cas9技术可以应用于植物的多基因编辑[62]。2015年,Ma等设计出了一种基于PCR的方式来快速构建多个sgRNA表达盒,并采用Golden Gate ligation或Gibson Assembly连接方法在一轮克隆中将表达盒装配到CRISPR/Cas9双元载体中[63],研究人员利用该系统在水稻中成功编辑了46个靶位点,突变率平均为85.4%,其中大多数为纯合突变和双等位基因突变(Biallelic mutation);同时在双子叶植物拟南芥中利用该多基因表达载体在T1代获得了双重杂合、纯合和嵌合突变,并证实在水稻和拟南芥中的上述突变位点都可以稳定遗传[63]。上述工作为研究植物基因家族功能以及创制多基因突变体提供了一个重要的研究工具。
2.4 基因单碱基精确突变基因敲除是解析植物基因功能的重要研究手段,然而在植物研究中发现,一些单核苷酸点突变是作物许多重要农艺性状发生变异的遗传基础。2016年,美国哈佛大学的Komor等对CRISPR/Cas9技术进行定向改进,构建出一种新型的“碱基编辑” (Base editor,BE)系统[64]。研究人员首先突变Cas9蛋白使其丧失DNA双链切割活性但保持其DNA双链的解旋功能(BE1);随后把可以将胞嘧啶(C)转变为尿嘧啶(U)的大鼠胞嘧啶脱氨酶APOBEC1融合到突变的Cas9蛋白N端,同时将尿嘧啶DNA糖基酶抑制剂(Uracil DNA glycosylase inhibitor,UDI)连接到APOBEC1-CRISPR/dCas9融合蛋白的C端(BE2),实现单碱基的精确转变;为进一步提高点突变的编辑效率,研究人员利用了哺乳动物细胞中固有的错配修复(Mismatch repair,MMR)机制,通过定点突变恢复Cas9蛋白的DNA单链切割活性(BE3),最终实现高效的基因单碱基精确突变[64]。2016年,Li等通过利用胞嘧啶脱氨酶、Cas9 (D10A)和尿嘧啶糖基化酶抑制剂(UGI)的融合蛋白(BE3),构建植物表达载体,成功对水稻OsPDS和OsSBEIIb基因进行单碱基定点替换,效率最高可达20%左右[65]。最近,Zong等利用Cas9变体(nCas9-D10A)融合大鼠胞嘧啶脱氨酶(rAPOBEC1) 和UGI,构成了高效的植物单碱基编辑系统nCas9-PBE,成功地在水稻、小麦和玉米等农作物基因组中实现高效、精确的单碱基定点突变[66],该项技术不需要外源DNA供体和双链DNA的切割,具有简单、广适、高效的特点,为高效和大规模创制单碱基突变体提供了一个可靠方案。
3 CRISPR/Cas9基因编辑技术在苜蓿等豆科饲草作物中的应用紫花苜蓿是世界著名优良牧草,也是我国栽培面积最大的一种豆科饲料作物,由于其具有蛋白质丰富、适应性强、能改良土壤和经济价值高等优点而享有“牧草之王”的美誉。但由于紫花苜蓿是多年生同源四倍体牧草,虫媒传粉,其复杂的遗传特性使得紫花苜蓿与二倍体作物相比在重要性状基因挖掘及遗传改良方面的研究工作相对滞后。蒺藜苜蓿Medicago truncatula是豆科苜蓿属一年生放牧型牧草,二倍体,与紫花苜蓿、黄花苜蓿、三叶草等豆科饲草具有高度的遗传相似性,随着蒺藜苜蓿全基因组测序的完成,蒺藜苜蓿已成为研究紫花苜蓿等豆科牧草遗传学和功能基因组学的理想模式[67]。
与水稻、小麦、玉米、大豆等主要粮食作物和经济作物相比,目前关于CRISPR/Cas9基因编辑技术在苜蓿等豆科饲草作物中的应用研究非常有限。为研究CRISPR/Cas9基因编辑技术在大豆等豆科作物中的应用,美国明尼苏达大学的研究人员开发了一个可以预测CRISPR/Cas9目标位点的网页工具,在此基础上,利用大豆密码子优化的Cas9蛋白构建了一个同时包含sgRNA的CRISPR/Cas9载体,并通过根毛转染的方法分别转化大豆和豆科模式牧草蒺藜苜蓿,分子检测发现在大豆和蒺藜苜蓿的根毛转化细胞中靶标基因出现一系列的突变[68]。2016年,Wang等在豆科模式植物百脉根中利用CRISPR技术成功实现LjLb1、LjLb2和LjLb3的多基因敲除,导致百脉根产生白色根瘤[69]。最近,我们实验室利用蒺藜苜蓿特异表达的U6启动子结合密码子优化的Cas9蛋白建立了1个适用于农杆菌介导的苜蓿CRISPR/Cas9基因组编辑系统,并利用该系统成功对蒺藜苜蓿的内源基因MtPDS进行了定点敲除,在T0代得到了比例达到10.35%的具有白化表型的蒺藜苜蓿纯合敲除突变体[70]。上述研究工作为苜蓿等豆科植物功能基因组学研究提供了重要的研究工具,同时为CRISPR/Cas9技术应用于紫花苜蓿等具有复杂基因组豆科饲草作物的遗传改良提供研究思路和技术参考。
4 展望随着我国经济快速发展,人民生活水平日益提高,广大城乡居民的饮食结构发生了很大改变,居民口粮消费逐渐下降,对牛羊肉、禽肉和奶制品等草食畜产品的消费不断加大,进而对苜蓿等优质饲草料的需求与日俱增。目前我国苜蓿等优质草种和饲草产品缺口较大,无法满足畜牧业生产的消费需要,导致苜蓿大量进口,对我国的饲料产业和畜产品安全造成严重威胁。
通过分子育种与传统育种相结合,加快培育高产优质苜蓿新品种,对于解决我国饲料作物生产和畜产品安全等问题至关重要。CRISPR/Cas9系统作为一种新兴的基因编辑技术,由于其具有操作简单灵活、编辑特异高效等特点,并且可以同时对多个基因进行高效精确定点修饰,目前已在植物基因定点编辑方面得到了大量应用,然而CRISPR/Cas9系统在使用上仍存在着一定的局限性。CRISPR/Cas9系统工作时需要将crRNA与tracrRNA融合在一起,并且需要在宿主RNA酶的帮助下才能发挥作用。最近,Zetsche等发现并改造出新型CRISPR/Cpf1系统,克服了CRISPR/Cas9系统的上述局限,CRISPR/Cpf1系统不需要tracrRNA的辅助,并且Cpf1蛋白兼具DNA剪切酶和RNA修剪酶双重功能,不但可以切割DNA双链,而且能把非成熟型crRNA (pre-crRNA)加工剪切为成熟型crRNA[71],目前科研人员利用该系统可简单高效地在动植物中实现多基因敲除,进一步拓展了CRISPR技术的应用[71-73]。相信随着CRISPR/Cas基因编辑技术的不断发展和完善,未来基因编辑技术将在农作物,尤其是饲草作物的产量、品质和抗性等重要性状的基因功能解析和遗传改良中发挥更大的作用。
| [1] | Gaj T, Gersbach CA, Barbas Ⅲ CF. ZFN, TALEN, and CRISPR/Cas-based methods for genome engineering. Trends Biotechnol, 2013, 31(7): 397–405. DOI: 10.1016/j.tibtech.2013.04.004 |
| [2] | Zhang K, Raboanatahiry N, Zhu B, et al. Progress in genome editing technology and its application in plants. Front Plant Sci, 2017, 8: 177. |
| [3] | Kim H, Kim JS. A guide to genome engineering with programmable nucleases. Nat Rev Genet, 2014, 15(5): 321–334. DOI: 10.1038/nrg3686 |
| [4] | Symington LS, Gautier J. Double-strand break end resection and repair pathway choice. Annu Rev Genet, 2011, 45: 247–271. DOI: 10.1146/annurev-genet-110410-132435 |
| [5] | Bleuyard JY, Gallego ME, White CI. Recent advances in understanding of the DNA double-strand break repair machinery of plants. DNA Repair, 2006, 5(1): 1–12. DOI: 10.1016/j.dnarep.2005.08.017 |
| [6] | Urnov FD, Miller JC, Lee YL, et al. Highly efficient endogenous human gene correction using designed zinc-finger nucleases. Nature, 2005, 435(7042): 646–651. DOI: 10.1038/nature03556 |
| [7] | Beumer K, Bhattacharyya G, Bibikova M, et al. Efficient gene targeting in Drosophila with zinc-finger nucleases. Genetics, 2006, 172(4): 2391–2403. |
| [8] | Li T, Liu B, Spalding MH, et al. High-efficiency TALEN-based gene editing produces disease-resistant rice. Nat Biotechnol, 2012, 30(5): 390–392. DOI: 10.1038/nbt.2199 |
| [9] | Katsuyama T, Akmammedov A, Seimiya M, et al. An efficient strategy for TALEN-mediated genome engineering in Drosophila. Nucleic Acids Res, 2013, 41(17): e163. DOI: 10.1093/nar/gkt638 |
| [10] | Smith J, Grizot S, Arnould S, et al. A combinatorial approach to create artificial homing endonucleases cleaving chosen sequences. Nucleic Acids Res, 2006, 34(22): e149. DOI: 10.1093/nar/gkl720 |
| [11] | Amitai G, Sorek R. CRISPR-Cas adaptation: insights into the mechanism of action. Nat Rev Microbiol, 2016, 14(2): 67–76. DOI: 10.1038/nrmicro.2015.14 |
| [12] | Hsu PD, Lander ES, Zhang F. Development and applications of CRISPR-Cas9 for genome engineering. Cell, 2014, 157(6): 1262–1278. DOI: 10.1016/j.cell.2014.05.010 |
| [13] | Doudna JA, Charpentier E. Genome editing: the new frontier of genome engineering with CRISPR-Cas9. Science, 2014, 346(6213): 1258096. DOI: 10.1126/science.1258096 |
| [14] | Mali P, Esvelt KM, Church GM. Cas9 as a versatile tool for engineering biology. Nat Methods, 2013, 10(10): 957–963. DOI: 10.1038/nmeth.2649 |
| [15] | Miao J, Guo DS, Zhang JZ, et al. Targeted mutagenesis in rice using CRISPR-Cas system. Cell Res, 2013, 23(10): 1233–1236. DOI: 10.1038/cr.2013.123 |
| [16] | Feng ZY, Zhang BT, Ding WN, et al. Efficient genome editing in plants using a CRISPR/Cas system. Cell Res, 2013, 23(10): 1229–1232. DOI: 10.1038/cr.2013.114 |
| [17] | Svitashev S, Young JK, Schwartz C, et al. Targeted mutagenesis, precise gene editing, and site-specific gene insertion in maize using Cas9 and guide RNA. Plant Physiol, 2015, 169(2): 931–945. DOI: 10.1104/pp.15.00793 |
| [18] | Liang Z, Chen KL, Li TD, et al. Efficient DNA-free genome editing of bread wheat using CRISPR/Cas9 ribonucleoprotein complexes. Nat Commun, 2017, 8: 14261. DOI: 10.1038/ncomms14261 |
| [19] | Wang SH, Zhang SB, Wang WX, et al. Efficient targeted mutagenesis in potato by the CRISPR/Cas9 system. Plant Cell Rep, 2015, 34(9): 1473–1476. DOI: 10.1007/s00299-015-1816-7 |
| [20] | Mao YF, Zhang H, Xu NF, et al. Application of the CRISPR-Cas system for efficient genome engineering in plants. Mol Plant, 2013, 6(6): 2008–2011. DOI: 10.1093/mp/sst121 |
| [21] | Jiang WZ, Zhou HB, Bi HH, et al. Demonstration of CRISPR/Cas9/sgRNA-mediated targeted gene modification in Arabidopsis, tobacco, sorghum and rice. Nucleic Acids Res, 2013, 41(20): e188. DOI: 10.1093/nar/gkt780 |
| [22] | Brooks C, Nekrasov V, Lippman ZB, et al. Efficient gene editing in tomato in the first generation using the clustered regularly interspaced short palindromic repeats/CRISPR-associated9 system. Plant Physiol, 2014, 166(3): 1292–1297. DOI: 10.1104/pp.114.247577 |
| [23] | Butler NM, Atkins PA, Voytas DF, et al. Generation and inheritance of targeted mutations in potato (Solanum tuberosum L.) using the CRISPR/Cas system. PLoS ONE, 2015, 10(12): e0144591. DOI: 10.1371/journal.pone.0144591 |
| [24] | Kim YG, Chandrasegaran S. Chimeric restriction endonuclease. Proc Natl Acad Sci USA, 1994, 91(3): 883–887. DOI: 10.1073/pnas.91.3.883 |
| [25] | Kim YG, Cha J, Chandrasegaran S. Hybrid restriction enzymes: zinc finger fusions to FokⅠcleavage domain. Proc Natl Acad Sci USA, 1996, 93(3): 1156–1160. DOI: 10.1073/pnas.93.3.1156 |
| [26] | Zhang F, Maeder ML, Unger-Wallace E, et al. High frequency targeted mutagenesis in Arabidopsis thaliana using zinc finger nucleases. Proc Natl Acad Sci USA, 2010, 107(26): 12028–12033. DOI: 10.1073/pnas.0914991107 |
| [27] | Pavletich NP, Pabo CO. Zinc finger-DNA recognition: crystal structure of a Zif268-DNA complex at 2.1 A. Science, 1991, 252(5007): 809–817. DOI: 10.1126/science.2028256 |
| [28] | Miller J, McLachlan AD, Klug A. Repetitive zinc-binding domains in the protein transcription factor ⅢA from Xenopus oocytes. EMBO J, 1985, 4(6): 1609–1614. |
| [29] | Beerli RR, Barbas Ⅲ CF. Engineering polydactyl zinc-finger transcription factors. Nat Biotechnol, 2002, 20(2): 135–141. DOI: 10.1038/nbt0202-135 |
| [30] | H ndel EM, Alwin S, Cathomen T. Expanding or restricting the target site repertoire of zinc-finger nucleases: the inter-domain linker as a major determinant of target site selectivity. Mol Ther, 2009, 17(1): 104–111. DOI: 10.1038/mt.2008.233 |
| [31] | Townsend JA, Wright DA, Winfrey RJ, et al. High-frequency modification of plant genes using engineered zinc-finger nucleases. Nature, 2009, 459(7245): 442–445. DOI: 10.1038/nature07845 |
| [32] | Zhu CF, Bortesi L, Baysal C, et al. Characteristics of genome editing mutations in cereal crops. Trends Plant Sci, 2017, 22(1): 38–52. DOI: 10.1016/j.tplants.2016.08.009 |
| [33] | Boch J, Bonas U. Xanthomonas Avrbs3 family-type Ⅲ effectors: discovery and function. Annu Rev Phytopathol, 2010, 48: 419–436. DOI: 10.1146/annurev-phyto-080508-081936 |
| [34] | Bonas U, Stall RE, Staskawicz B. Genetic and structural characterization of the avirulence gene Avrbs3 from Xanthomonas campestris pv. vesicatoria. Mol Gen Genet, 1989, 218(1): 127–136. DOI: 10.1007/BF00330575 |
| [35] | van den Ackerveken G, Marois E, Bonas U. Recognition of the bacterial avirulence protein Avrbs3 occurs inside the host plant cell. Cell, 1996, 87(7): 1307–1316. DOI: 10.1016/S0092-8674(00)81825-5 |
| [36] | Zhu WG, Yang B, Chittoor JM, et al. Avrxa10 contains an acidic transcriptional activation domain in the functionally conserved C terminus. Mol Plant Microbe Interact, 1998, 11(8): 824–832. DOI: 10.1094/MPMI.1998.11.8.824 |
| [37] | Moscou MJ, Bogdanove AJ. A simple cipher governs DNA recognition by TAL effectors. Science, 2009, 326(5959): 1501. DOI: 10.1126/science.1178817 |
| [38] | Boch J, Scholze H, Schornack S, et al. Breaking the code of DNA binding specificity of TAL-type Ⅲ effectors. Science, 2009, 326(5959): 1509–1512. DOI: 10.1126/science.1178811 |
| [39] | Miller JC, Tan SY, Qiao GJ, et al. A TALE nuclease architecture for efficient genome editing. Nat Biotechnol, 2011, 29(2): 143–148. DOI: 10.1038/nbt.1755 |
| [40] | Morbitzer R, R mer P, Boch J, et al. Regulation of selected genome loci using de novo-engineered transcription activator-like effector (TALE)-type transcription factors. Proc Natl Acad Sci USA, 2010, 107(50): 21617–21622. DOI: 10.1073/pnas.1013133107 |
| [41] | Joung JK, Sander JD. TALENs: a widely applicable technology for targeted genome editing. Nat Rev Mol Cell Biol, 2013, 14(1): 49–55. |
| [42] | Cermak T, Doyle EL, Christian M, et al. Efficient design and assembly of custom TALEN and other TAL effector-based constructs for DNA targeting. Nucleic Acids Res, 2011, 39(12): e82. DOI: 10.1093/nar/gkr218 |
| [43] | Bedell VM, Wang Y, Campbell JM, et al. In vivo genome editing using a high-efficiency TALEN system. Nature, 2012, 491(7422): 114–118. DOI: 10.1038/nature11537 |
| [44] | Christian M, Cermak T, Doyle EL, et al. Targeting DNA double-strand breaks with TAL effector nucleases. Genetics, 2010, 186(2): 757–761. DOI: 10.1534/genetics.110.120717 |
| [45] | Wang YP, Cheng X, Shan QW, et al. Simultaneous editing of three homoeoalleles in hexaploid bread wheat confers heritable resistance to powdery mildew. Nat Biotechnol, 2014, 32(9): 947–951. DOI: 10.1038/nbt.2969 |
| [46] | Stoddard BL. Homing endonuclease structure and function. Q Rev Biophys, 2005, 38(1): 49–95. |
| [47] | Gao HR, Smith J, Yang MZ, et al. Heritable targeted mutagenesis in maize using a designed endonuclease. Plant J, 2010, 61(1): 176–187. DOI: 10.1111/tpj.2009.61.issue-1 |
| [48] | Sorek R, Lawrence CM, Wiedenheft B. CRISPR-mediated adaptive immune systems in bacteria and archaea. Annu Rev Biochem, 2013, 82: 237–266. DOI: 10.1146/annurev-biochem-072911-172315 |
| [49] | Mojica FJ, Díez-Villase or C, García-Martínez J, et al. Intervening sequences of regularly spaced prokaryotic repeats derive from foreign genetic elements. J Mol Evol, 2005, 60(2): 174–182. DOI: 10.1007/s00239-004-0046-3 |
| [50] | Mojica FJM, Díez-Villase or C, Soria E, et al. Biological significance of a family of regularly spaced repeats in the genomes of archaea, bacteria and mitochondria. Mol Microbiol, 2000, 36(1): 244–246. DOI: 10.1046/j.1365-2958.2000.01838.x |
| [51] | Barrangou R, Fremaux C, Deveau H, et al. CRISPR provides acquired resistance against viruses in prokaryotes. Science, 2007, 315(5819): 1709–1712. DOI: 10.1126/science.1138140 |
| [52] | Ishino Y, Shinagawa H, Makino K, et al. Nucleotide sequence of the iap gene, responsible for alkaline phosphatase isozyme conversion in Escherichia coli, and identification of the gene product. J Bacteriol, 1987, 169(12): 5429–5433. DOI: 10.1128/jb.169.12.5429-5433.1987 |
| [53] | Jansen R, van Embden JD, Gaastra W, et al. Identification of genes that are associated with DNA repeats in prokaryotes. Mol Microbiol, 2002, 43(6): 1565–1575. DOI: 10.1046/j.1365-2958.2002.02839.x |
| [54] | Garneau JE, Dupuis ME, Villion M, et al. The CRISPR/Cas bacterial immune system cleaves bacteriophage and plasmid DNA. Nature, 2010, 468(7320): 67–71. DOI: 10.1038/nature09523 |
| [55] | Jinek M, Chylinski K, Fonfara I, et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science, 2012, 337(6096): 816–821. DOI: 10.1126/science.1225829 |
| [56] | Sander JD, Joung JK. CRISPR-Cas systems for editing, regulating and targeting genomes. Nat Biotechnol, 2014, 32(4): 347–355. DOI: 10.1038/nbt.2842 |
| [57] | Li JF, Norville JE, Aach J, et al. Multiplex and homologous recombination-mediated genome editing in Arabidopsis and Nicotiana Benthamiana using guide RNA and Cas9. Nat Biotechnol, 2013, 31(8): 688–691. DOI: 10.1038/nbt.2654 |
| [58] | Nekrasov V, Staskawicz B, Weigel D, et al. Targeted mutagenesis in the model plant Nicotiana Benthamiana using Cas9 RNA-guided endonuclease. Nat Biotechnol, 2013, 31(8): 691–693. DOI: 10.1038/nbt.2655 |
| [59] | Shan QW, Wang YP, Li J, et al. Targeted genome modification of crop plants using a CRISPR-Cas system. Nat Biotechnol, 2013, 31(8): 686–688. DOI: 10.1038/nbt.2650 |
| [60] | Li ZS, Liu ZB, Xing AQ, et al. Cas9-guide RNA directed genome editing in soybean. Plant Physiol, 2015, 169(2): 960–970. DOI: 10.1104/pp.15.00783 |
| [61] | Li J, Meng XB, Zong Y, et al. Gene replacements and insertions in rice by intron targeting using CRISPR-Cas9. Nat Plants, 2016, 2: 16139. DOI: 10.1038/nplants.2016.139 |
| [62] | Xing HL, Dong L, Wang ZP, et al. A CRISPR/Cas9 toolkit for multiplex genome editing in plants. BMC Plant Biol, 2014, 14: 327. DOI: 10.1186/s12870-014-0327-y |
| [63] | Ma XL, Zhang QY, Zhu QL, et al. A robust CRISPR/Cas9 system for convenient, high-efficiency multiplex genome editing in monocot and dicot plants. Mol Plant, 2015, 8(8): 1274–1284. DOI: 10.1016/j.molp.2015.04.007 |
| [64] | Komor AC, Kim YB, Packer MS, et al. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Nature, 2016, 533(7603): 420–424. DOI: 10.1038/nature17946 |
| [65] | Li JY, Sun YW, Du JL, et al. Generation of targeted point mutations in rice by a modified CRISPR/Cas9 system. Mol Plant, 2017, 10(3): 526–529. DOI: 10.1016/j.molp.2016.12.001 |
| [66] | Zong Y, Wang YP, Li C, et al. Precise base editing in rice, wheat and maize with a Cas9-cytidine deaminase fusion. Nat Biotechnol, 2017, 35(5): 438–440. DOI: 10.1038/nbt.3811 |
| [67] | Young ND, Debellé F, Oldroyd GED, et al. The Medicago genome provides insight into the evolution of rhizobial symbioses. Nature, 2011, 480(7378): 520–524. |
| [68] | Michno JM, Wang XB, Liu JQ, et al. CRISPR/Cas mutagenesis of soybean and Medicago truncatula using a new web-tool and a modified Cas9 enzyme. GM Crops Food, 2015, 6(4): 243–252. DOI: 10.1080/21645698.2015.1106063 |
| [69] | Wang LX, Wang LL, Tan Q, et al. Efficient inactivation of symbiotic nitrogen fixation related genes in Lotus japonicus using CRISPR-Cas9. Front Plant Sci, 2016, 7: 1333. |
| [70] | Meng YY, Hou YL, Wang H, et al. Targeted mutagenesis by CRISPR/Cas9 system in the model legume Medicago truncatula. Plant Cell Rep, 2017, 36(2): 371–374. DOI: 10.1007/s00299-016-2069-9 |
| [71] | Zetsche B, Heidenreich M, Mohanraju P, et al. Multiplex gene editing by CRISPR-Cpf1 using a single crRNA array. Nat Biotechnol, 2017, 35(1): 31–34. |
| [72] | Wang MG, Mao YF, Lu YM, et al. Multiplex gene editing in rice using the CRISPR-Cpf1 system. Mol Plant, 2017, 10(7): 1011–1013. DOI: 10.1016/j.molp.2017.03.001 |
| [73] | Hu XX, Wang C, Liu Q, et al. Targeted mutagenesis in rice using CRISPR-Cpf1 system. J Genet Genomics, 2017, 44(1): 71–73. DOI: 10.1016/j.jgg.2016.12.001 |
 2017, Vol. 33
2017, Vol. 33




