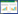中国科学院微生物研究所、中国微生物学会主办
文章信息
- 王方圆, 赵德华, 亓磊
- Fangyuan Wang, Dehua Zhao, Lei Stanley Qi
- 基因组工程在医学合成生物学中的应用
- Application of genome engineering in medical synthetic biology
- 生物工程学报, 2017, 33(3): 422-435
- Chin J Biotech, 2017, 33(3): 422-435
- 10.13345/j.cjb.160420
-
文章历史
- Received: November 2, 2016
- Accepted: February 7, 2017
2 斯坦福大学 生物工程系,CA 94305,美国
亓磊 国际知名的生物工程专家,在医学合成生物学领域和基因组编辑领域作出重要的贡献,目前在斯坦福大学任助理教授。毕业于清华大学,在美留学期间,师从美国第12任能源部部长朱棣文教授,并在加州大学伯克利分校获得生物工程学博士学位。由于成绩显著,毕业后即被加州大学旧金山医学院聘为研究员。近年来先后作为第一作者和通讯作者在Nature、Cell及其子刊等国际顶尖学术期刊上多次发表重要成果,引用超过1 500次,在国际上有重要影响力。并在Science、Cell等多家刊物任审稿人。参加过多项美国国立卫生研究院的课题研究,拥有多项专利。同时还是美国多家协会 (包括生物工程学学会、合成生物学学会) 的会员,组织了多项重要的学术会议
2 Department of Bioengineering, Stanford University, CA 94305, USA
合成生物学是21世纪初新兴的交叉学科,涉及到生物学、工程学及计算机科学等多学科的综合。合成生物学旨在通过人工设计和构建自然界中不存在的生物元件和系统,或重新工程化改造和优化现有的生物元件和系统,或利用系统生物学、计算模拟以及定量分析等方法来制造复杂的生物系统。虽然是一个新兴学科,但合成生物学在多个领域已展现了重要的应用,比如通过酵母生产生物能源[1-2]和制造多功能材料[3]、利用微生物净化水源和土壤来保护环境[4-5]、或是生产可杀死癌细胞的免疫细胞来治疗疾病[6]。发展合成生物学对于发展其他学科有重要意义。合成生物学不仅依赖于多学科的交叉和发展,同时又促进多学科、多产业 (如医学、药学、环境和能源等) 的发展,因此正在成为生物工程学的核心学科,也是会带来革命性突破的战略性学科之一[7-8]。基于其广泛的应用,发展合成生物学具有重大的科学意义、经济意义和社会意义。
合成生物学的核心思想是将复杂的生物系统变得可编程。很多合成生物学家受到计算机科学的启发,将一个复杂的生命系统 (如细胞或人体) 类比于一台计算机。那么区别在哪里?计算机中运行的是数字化的信息程序,是人们通过编程可以控制计算机的代码。而生命系统中流动的是生命的信息,是通过上亿年进化产生的关于自身复制、产生功能和凋亡的程序。理解这种复杂的生命程序背后的意义是生物学的研究目标,而编程、调控这一复杂生命程序则是合成生物学的研究目标。
近年来,合成生物学研究主要包括以下内容:大规模基因元件的构建和定量测量、理解基因线路和系统的设计原理、大规模DNA合成技术的开发、基因组编辑和调控平台的建立。
合成生物学的核心概念之一是基因线路 (Genetic circuit) 的构造。基因线路是由基因元件构成的,而基因元件包括编码蛋白的基因 (如编码酶的基因)、调控基因表达的元件 (如启动子、增强子、调控蛋白和RNA等) 以及可以感应外在信号的分子 (如可以结合小分子的蛋白和RNA)。基因调控元件包括转录水平元件 (如启动子、终止子等调控序列) 和转录后水平元件 (如mRNA序列或非编码RNA序列)[9]。而基因线路则是通过将不同的基因元件按一定逻辑规律连接在一起构成网络,比如上游的基因蛋白产物可以调控下游的基因表达,如此环环相扣实现特定的生物学功能。通过在活体细胞中实现复杂的、有功能的基因线路一直是合成生物学研究的热点,这不仅需要基础研究来理解构造复杂线路的基本原理,更重要的是会带来多方面的实际应用,如解决医学、环境和能源行业等面临的问题[10-11]。
一条典型的基因线路通常包含三部分:感应器 (检测接收的输入信号)、处理器 (针对输入信号做出计算) 和执行器 (行使细胞功能)。这些器件联结、搭配起来,可执行各种特定的生物学功能,如逻辑门[12-16]、基因表达开关[17-18]、记忆设备[19]和细胞内通讯[20-21]。这些“合成型”调控元件必须是有效的 (能够调控靶基因的表达水平到期望值)、程序性的 (能够被调控至期望的靶点发挥作用),并且可有效避免与细胞中原有的基因交互干扰反应,从而实现对细胞的编程。目前,针对基因组的可编程、合成型调控元件主要包括锌指蛋白 (Zinc finger protein,ZFP)、类转录激活效应因子 (Transcription activator-like effector,TALE) 和CRISPR干扰 (CRISPR interference,CRISPRi)。
2 基因组工程基因组工程是指对细胞的基因组进行工程性操作,包含对基因组DNA的修改、重组和编辑,从而实现新的、有用的生物体性状,如细菌品种改良、提高农作物产量、或是生产用于治疗的干细胞。随着人类基因组测序的普及,读取基因组的信息已经不是基因组研究的瓶颈。如何有效改写和调控基因组的信息在近几年随之成为一个焦点。正是在这种背景下,基因组编辑技术获得了突飞猛进的发展。
至今,已有多种高效的DNA靶向内切酶被发现,如锌指核酸酶 (Zinc finger nuclease,ZFN)[22]、类转录激活样效应因子核酸酶 (Transcription activator-like effector nuclease,TALEN)[23-24]和成簇规律间隔短回文重复序列 (Clustered regulatory interspaced short palindromic Repeats,CRISPR) 相关蛋白[25-26]。这些靶向内切酶都可以结合到DNA的特定位点并进行切割,造成DNA双链断裂 (Double-strand break,DSB)。为了修复双链断裂,细胞随即利用自身的修复机制 (DNA repair pathway) 在该位点产生同源重组 (Homology-directed recombination,HDR) 或非同源末端连接 (Non-homologous end joining,NHEJ),从而实现靶基因编辑。如今,ZFN、TALEN和CRISPR技术已成为基因组工程学的基本工具,而它们在合成生物学中的应用也正在为合成生物学带来新的突破。
3 CRISPR技术 3.1 CRISPR/Cas自2013年CRISPR/Cas9技术成功用于人细胞中基因组编辑,由于其较高的编辑效率、便捷的操作方式和较低的脱靶率,CRISPR/Cas介导的基因组编辑技术成为一项新型的基因组编辑的主流方法。其研究和应用最近几年也取得了突飞猛进的发展。
CRISPR起初是源于细菌中的发现,指的是细菌体内通过序列特异性互补配对,以抵御噬菌体外源DNA侵染的分子机制[27]。该机制的独特之处在于,不同于其他仅仅依靠蛋白质分子和DNA特异性结合的识别机制 (如ZFN和TALEN),CRISPR是通过RNA (核糖核酸) 和DNA (脱氧核糖核酸) 的碱基互补配对原则 (即A/T或A/U互补,G/C互补) 来识别特定的DNA序列并且切割该序列。目前已被发现的CRISPR/Cas系统有3种,分别为Ⅰ型、Ⅱ型和Ⅲ型[28-29]。其中Ⅱ型系统CRISPR/Cas9组分最为简单,只需要一个Cas9蛋白 (CRISPR-associated protein 9) 就可以实现DNA识别和剪切[30]。Cas9蛋白与工程化的向导RNA (Single guide RNA,sgRNA,向导RNA) 结合,在sgRNA指引下Cas9/sgRNA能够识别与向导RNA中的指引序列互补配对的靶DNA序列,并进行切割,形成DNA双链断裂 (Double-strand breaks,DSB),随后DNA通过NHEJ或HDR方式进行修复,造成基因敲除或编辑 (Gene editing)[25] (图 1A)。
|
| 图 1 CRISPR工具箱。(A) Cas9核酸酶和序列特异的向导RNA (sgRNA) 可以特异识别基因组的序列并切割基因组。这允许人们对基因组的特异序列进行编辑 (Gene editing)。(B) 核酸酶失活的Cas9 (dCas9) 和序列特异的sgRNA可以特异结合基因组的序列并产生基因调控功能。在原核生物中,dCas9和sgRNA直接结合到基因组可以直接阻断基因转录;在真核生物中,dCas9和KRAB蛋白域的融合蛋白可以更有效地抑制下游基因的表达。(C) dCas9融合蛋白和序列特异的sgRNA可以特异地结合基因组的序列并激活基因表达。第一代激活技术基于dCas9和VP64的直接融合,但是效率欠佳;第二代激活技术,包括Suntag、VPR、SAM等系统可以大大提高基因激活的效率。(D) dCas9和表观遗传学因子的融合蛋白可以允许人们对基因组进行表观遗传学修饰编辑。 Figure 1 The CRISPR toolkits. (A) The Cas9 nuclease and sequence-specific sgRNA can recognize and cut desired DNA sequence in the genome. This allows gene editing of specific genome sequences. (B) The nuclease-deactivated Cas9 (dCas9) and sequence-specific sgRNA can bind to desired DNA sequence and modulate its transcription. In prokaryotes, binding of dCas9 and sgRNA to the genome can sterically block transcription. In eukaryotes, dCas9 fused with KRAB can more effectively inhibit downstream gene expression. (C) dCas9 fusion proteins and sgRNAs can activate gene expression in the genome. The first generation of dCas9 activators is based on dCas9 fused to VP64, with only a moderate efficiency. The second generation technique, including Suntag, VPR, and SAM can enhance gene activation efficiency. (D) dCas9 fused with epigenetic factors allows modifying the epigenetic modifications of the genome |
| |
CRISPR作为一项新兴技术,近年来大幅度扩展了合成生物学的基因元件库。CRISPR/Cas9与其他元件 (RNA、蛋白质等) 结合到一起,成为“超级合成生物学元件”。比如,CRISPR与sgRNA结合可作为感应器感知信号,可作为处理器传递信号,也可作为执行器行使功能。
3.2 CRISPR/Cas9优势CRISPR/Cas9技术的优势在于其特异性、有效性和便利性。一方面,碱基互补配对原则使得CRISPR/Cas9几乎可以识别任何DNA序列,实现了整个基因组范围内的识别,同时大大简化了sgRNA的设计、克隆和功能测试。另一方面,CRISPR/Cas9在不同物种中都展现了功能。已发表的研究工作显示CRISPR系统可以高效且特异地识别多种物种的基因组,包括细菌[31]、酵母[32]、果蝇[33]、线虫[34]、斑马鱼[35]、水稻[36]、小鼠[37-38]、大鼠[39]、猪[40]以及人的细胞[41],另外CRISPR/Cas9技术也在HeLa和K562[42]等多种癌细胞、小鼠胚胎干细胞、人脐带静脉内皮细胞、人成纤维细胞和人诱导性多功能干细胞 (Induced pluripotent stem cells,iPS) 以及iPS细胞分化的神经干细胞中实现了基因敲除、基因敲入和基因突变等编辑[43]。
CRISPR/Cas9技术的另一大优势是,除了基因编辑,还能够在原技术基础上,对Cas9蛋白进行改造,实现序列特异的、精准的基因表达调控。我们在过去的工作中首次发明了核酸酶失活的Cas9 (Deactivated Cas9或dCas9) (图 1B),使Cas9蛋白失去剪切DNA序列的功能,但仍具有sgRNA导向的序列特异结合功能。这种技术称为CRISPR干扰 (CRISPR interference,CRISPRi),是指通过dCas9 “占位”阻挡了RNA聚合酶结合到启动子,或者RNA聚合酶的“前进”,或者RNA聚合酶与其他转录因子的结合等,实现对多种物种基因表达抑制的调控[44]。关于dCas9的基因表达调控技术在下面会详细讨论。
4 CRISPR技术在合成生物学中的应用 4.1 基于CRISPR/Cas9的调控工具通过将dCas9与多种不同调控因子融合,目前我们已经实现了基因组范围内的定向抑制基因表达,激活基因表达,在同一细胞内的双向调控和较大DNA区域上表观遗传学修饰的改变 (表 1)。将dCas9与转录抑制因子 (KRAB) (图 1B) 融合,可以沉默内源基因如干性基因OCT4、NANOG、SOX2等的表达,且可被抑制到精准的表达量[44];将dCas9与转录激活因子 (VP16、p65等) (图 1C) 融合,可以激活内源基因表达[45]。使用基于dCas9抑制元件和激活元件,可精准确定基因被抑制或激活的水平,以揭示影响生物功能的基因活性变化的程度。另外,将dCas9与人乙酰转移酶p300核心结构域融合 (图 1D),使靶基因启动子和增强子的组蛋白H3第27位赖氨酸均被乙酰化 (H3K27ac),可实现靶基因的表观遗传学修饰[46]。基于dCas9基因工程表达调控元件还可以方便地进行多位点的调控。因为只需要表达多个不同的gRNA,同一个dCas9即可靶向不同基因。最近一项研究显示,向细胞中共转染10个gRNA,可同时激活这10个gRNA靶向的基因,尽管激活效率比这10个基因分别被单个gRNA激活低[47]。
除将dCas9以融合蛋白的方法改造成调控因子,改造sgRNA成为效应因子招募序列,为调控基因提供了更多的工具。在sgRNA 3′-末端增加效应因子招募序列,形成CRISPR RNA支架 (Scaffold RNA,scRNA) (图 1C,如SAM系统)。scRNA不仅具有普通gRNA的靶向DNA结合序列能力,还可以通过招募序列 (称为aptamer) 与其他蛋白质相互作用,使效应因子 (转录激活子或抑制子) 结合到sgRNA。因此,一个scRNA招募一种转录因子如VP64到一个基因来调控该基因,而另一个scRNA可同时招募同种类型转录因子到另一个基因,也可招募不同类型转录因子如KRAB转录抑制子到另一个基因 (dCas9不变),于是使得同时上调多个基因、或同时下调多个基因、或在上调某一 (些) 基因的同时下调另一 (些) 基因 (双向调控),得以实现[48]。值得一提的是,CRISPR也可与其他合成型调控工具 (如RNAi、miRNA、shRNA等) 整合到一起,组成一个工具箱,从而发挥复杂的程序性调控作用[49]。
最近另一项对sgRNA进行改造的研究发现,缩短sgRNA中向导序列的长度到16个核苷酸,尽管Cas9的核酸酶活性大大降低,但它仍然可以与DNA相互作用识别靶DNA;非常有趣的是,进一步将Cas9与转录激活因子VPR融合,Cas9-VPR与缩短的sgRNA结合,却不仅与Cas9具有相同的核酸酶活性,而且能够同时激活下游报告基因的表达。这使得CRISPR/Cas9-VPR成为能同时发挥基因编辑和转录调控作用的多能工具,使同时调控DNA和RNA成为现实[50]。
但是,在CRISPR/Cas9应用于人的细胞时,由于RNA聚合酶Ⅱ表达的RNA会被运送至细胞质,而sgRNA需要在细胞核内结合到基因组DNA,因此sgRNA只能由RNA聚合酶Ⅲ表达。然而RNA聚合酶Ⅲ只占RNA聚合酶中的一小部分,且很多组织及诱导型表达系统只能利用RNA聚合酶Ⅱ,这大大限制了CRISPR/Cas技术在基因调控和基因组工程上的应用。研究表明,应用RNA三螺旋 (RNA-Triple-Helix) 结构和结合并切割RNA的Csy4组合成的复合体 (Triplex/Csy4),可实现通过RNA聚合酶Ⅱ表达gRNA[49],大大增加了CRISPR人工转录因子和CRISPR基因线路 (CRISPR/Cas-based circuits) 的应用范围,提高了调控效率。
在现有的CRISPR/Cas9技术中,基于化脓性链球菌Streptococcus pyogenes sp.的Cas9的基因编辑和调控工具应用得最为广泛。但是在一种细胞中,基于同一种Cas9的多基因调控并不是平行的和独立的正交控制系统。利用来源于不同种细菌的Cas9蛋白和与其共轭的sgRNA,可以实现基于CRIPSR/Cas9的正交调控。使用一整套Cas9同源体 (Cas9 orthologs),它们分别来源于化脓性链球菌、嗜热链球菌Streptococcus thermophilus、脑膜炎奈瑟菌Meningococcal meningitidis和齿垢密螺旋体Treponema denticola,不仅可以在细胞中 (细菌或人) 同时地、独立地、互不干扰地介导基因编辑和基因调控,而且可以同时调控转录激活和转录抑制[51]。
利用CRISPR人工转录因子 (CRISPR/Cas transcription factors,CRISPR-TF) 和设计sgRNA得到新的调控元件,可以轻松实现同时调控多个基因和复杂的基因线路。与基于CRIPSR/Cas9的正交调控结合,为构建大规模合成型基因线路,对天然调控网络进行重新组合以及模拟天然状态下的基因网络提供了特别丰富的工具。
4.2 基于CRISPR/Cas9的基因线路合成生物学中,构建复杂基因调控线路的一个重要原则是:上游元件的输出信号可以作为下游元件的输入信号。例如,经改造后,哺乳动物细胞中上游sgRNA与dCas9的复合物可调控下游sgRNA的表达,而下游sgRNA随即调控荧光蛋白的表达[49],如此环环相扣。
CRISPR/Cas9已经被用来构建多种应用型的基因线路。最近一项研究表明,CRISPR/Cas9可用于构造新型“分子信号传导器” (CRISPR-Cas9-based ‘signal conductor’),有效感知、处理和操控生物信号,指导细胞内信息传递,调控内源基因转录[52]。该研究使用带适配器 (感知信号) 的加长型sgRNA,以及可识别信号的核糖开关 (Riboswitch),这两个看似毫不相关的分子结合到一起,也组成一个RNA支架 (图 2A)。当环境中不存在特异性信号时,sgRNA与其反义链结合,不能结合到DNA靶点;当出现特异性信号A (或B) 时,A结合到sgRNA的适配器上,造成RNA支架构象发生变化,sgRNA随即与DNA靶点结合,影响信号B (或A) 的转录。该装置不仅可用于构建所有类型的布尔逻辑门 (Boolean logic gates) 等,也可通过构建一些偶联不同信号通路的合成型结点,用于重新排列、组织细胞信号通路;最重要的是,该装置通过调控双向 (ON-OFF) 基因转录,能够重新组织癌基因信号转导路径,使癌细胞发生重编程甚至逆转。
CRISPR逻辑与门 (AND gate) 的构建可用于筛选膀胱癌细胞,用于临床治疗[53]。此基因线路由肿瘤细胞特异的启动子 (hTERT) 驱动、靶向lacⅠ基因的sgRNA (sgRNA-lacⅠ) 和膀胱细胞特异的启动子 (hUPⅡ) 驱动的dCas9组成,当sgRNA和dCas9都表达时,lacⅠ基因 (编码转录抑制因子lacⅠ) 被阻遏,lacⅠ介导的转录抑制过程被缓解,其下游信号通路表达,即有信号输出 (图 2B)。因此,只有在那些hTERT和hUPⅡ都表达的细胞,即膀胱癌细胞中,才有下游信号输出。下游信号可连接与治疗相关的基因,如hBax (编码前凋亡因子)、p21 (编码抗增殖因子) 和E-cadherin(编码细胞迁移抑制因子),即可发挥治疗作用。
CRISPR转录逻辑门 (Transcriptional logic gates) 可调控大肠杆菌的基因表达[54]。小分子输入信号诱导启动子表达sgRNA,sgRNA招募dCas9到合成型启动子,阻止RNA聚合酶 (RNAP) 结合到该合成型启动子,阻止了输出基因信号的表达。因此,只有缺失输入信号时,才有输出基因信号的表达和相应基因的转录,此即“非门” (NOT gate)。重要的是,“非门”和“或门”可以层层排列,搭建“也非门”及“与门”,扩增逻辑调控的数量。这些基因线路的输出信号既可以是编码某蛋白的基因,也可以是靶向大肠杆菌内源性基因的gRNA,能够操控各种各样的细菌表型变化,如生物膜形成、代谢和细菌耐药性。
最近通过使用不同的小分子诱导招募不同的转录因子,我们构建了一个基于多正交dCas9,诱导型,多基因平行上调和下调的技术平台 (图 2C)[55]。通过将来自植物的脱落酸 (Abscisic acid,ABA) 诱导的双聚物蛋白体系或是来自植物的赤霉素 (Gibberellin,GA) 诱导的双聚物蛋白体系与不同来源的dCas9进行融合,我们可以使用小分子来诱导招募转录激活因子或转录抑制因子。如果把两种双聚物蛋白体系串联融合到dCas9蛋白上,则构成了一个与门 (AND gate),即只有当两个小分子都存在时才会诱导dCas9的相关功能 (图 2D);如果把两种双聚物蛋白体系平行融合到同一个dCas9蛋白上来招募同一个转录因子 (比如VP64),则构成了一个或门 (OR gate),即任何一个小分子的存在都会诱导dCas9的相关功能 (图 2E);如果在或门中招募的是两个不同的转录因子,比如一个是激活的,而另一个是抑制的,那么这就构成了一个双向开关器件 (Diametric device) (图 2F)。这个平台的优点在于通过简单的蛋白组装就能实现预期的逻辑器件和转录线路。

|
| 图 2 基于CRISPRi的逻辑门和基因线路。(A) 使用加长型sgRNA,以及可识别信号的核糖开关 (Riboswitch),可以在有小分子配体存在下造成RNA支架构象发生变化成为基因开关。(B) 由肿瘤细胞特异的启动子 (hTERT) 和膀胱细胞特异的启动子 (hUPⅡ) 驱动,CRISPRi可以允许人们构造基因线路用于筛选膀胱癌细胞和临床治疗。(C) 通过使用不同的小分子配体诱导招募不同的转录因子,我们构建了一个诱导型、正交dCas9系统,用于可编程模式的多基因平行上调和下调。(D) 当把两种双聚物蛋白体系串联到dCas9蛋白上,这构成了一个与门 (AND gate)。(E) 当把两种双聚物蛋白体系并联到dCas9蛋白上来招募同一个转录因子 (比如VP64),这构成了一个或门 (OR gate)。(F) 如果在或门中招募的是两个不同的转录因子:一个是激活的,而另一个是抑制的,这就构成了一个双向开关器件 (Diametric device) Figure 2 CRISPRi-mediated logic gates and gene circuits. (A) Using a modified long sgRNA and a riboswitch that can recognize chemical ligands, researchers created a scaffold RNA that can undergo conformational change in response to ligands to switch genes ON and OFF. (B) Using a tumor-specific promoter (hTERT) and a bladder cell-specific promoter (hUPⅡ), CRISPRi allows researchers to construct gene circuits that can be used for bladder cancer cell detection and treatment. (C) Using different small molecule ligands to recruit transcription effectors, we constructed an inducible and orthogonal dCas9 system that can be used for multiple gene activation and repression. (D) When we fuse two ligand-inducible dimerization systems in parallel to dCas9, this leads to a AND gate. (E) When we fuse two dimerization systems in series to dCas9 (e.g., VP64), this leads to a OR gate. (F) If two opposite transcription effectors are used in the OR gate, one is activating and the other is repressing, this leads to a diametric device |
| |
此外,将生物光学感应系统与CRISPR/dCas9系统相结合,也是CRISPR在合成生物学应用的重要进展之一。研究人员构建了由蓝光激活的CRISPR/Cas9效应因子 (Light-activated CRISPR/Cas9 effector,LACE) 系统。首先分别将dCas9和CIB1融合,CRY2与VP64融合;当有蓝光照射时,dCas9-CIB1和CRY2-VP64融合形成异源二聚体,dCas9与VP64靠近,组成转录激活子,激活内源靶基因的表达[56]。
4.3 CRISPR/Cas9用于细胞底盘制造和其他应用CRISPR/Cas9为细胞底盘制造提供了有力的工具。例如多位点的目标DNA的删除。可用于移植的器官的匮乏使得许多人类疾病的治疗处于瓶颈。猪器官是目前可供人体移植的来源之一,但是猪体内的内源性反转录病毒一旦整合到人基因组,可能增加人类患癌症的风险,因此抑制或清除猪内源性病毒成为突破“猪器官移植到人”技术瓶颈的重要部分。利用CRISPR/Cas9人们可以清除猪肾上皮细胞系PK15的所有内源性病毒PERVs,为临床移植提供了重要支持[57]。
“CRISPR展示” (CRISPR-Disp) 法是使用各种可结合蛋白的RNA结构域修饰gRNA (与scRNA类似),使sgRNA在不同靶点时,细胞执行不同的功能[58]。使用该方法分别共表达sgRNA与VP64以及gRNA与荧光蛋白,可以激活一个位点的同时成像另一个位点[58]。此外,CRISP-Disp平台能够招募长链非编码RNA到特异基因组位点,成为研究RNA功能的强大工具。
4.4 其他基因组工程技术在合成生物学的应用真核生物中,ZFPs是由一系列识别DNA序列的锌指蛋白 (Cys2-His2) 串联 (一般3-4个) 而成的小结构域和一个非特异性核酸内切酶构成;每个锌指蛋白识别并结合一个特异的三联体碱基,随后内切酶对该位点的DNA双链进行切割,DNA片段与供体 (Donor) 通过同源重组修复方式相互连接,供体片段完成插入。工程化锌指蛋白核酸酶 (ZFN) 对大鼠内源性基因IgM和Rab38的敲除效率可达25%-100%[59]。对人细胞中IL2Rγ基因的X染色体相关性重度联合免疫缺陷 (X-linked severe combined immune deficiency,SCID) 突变设计相应的锌指内切酶,结果IL2Rγ基因发生改变的细胞占18%,两条X染色体的基因均发生改变的细胞占7%,说明改造后、工程化的锌指内切酶可用于临床治疗[60]。
TALEN蛋白家族来自一类植物病原体——黄单胞杆菌 (Xanthomonas spp.),可通过识别特异DNA序列调控宿主植物内源基因的表达[61]。TALEN蛋白中部包含一段长串联重复序列,具有特异性识别、结合特异DNA序列的特性,可以根据需要进行改造,靶向特异性位点。若与转录激活因子或抑制因子 (如VP64或KRAB) 连接,则可发挥转录调控作用[62-65];若与内切酶连接,则可进行位点特异性基因组编辑[60, 66]。使用GoldyTALEN支架可在斑马鱼的体细胞和生殖细胞中进行高度精准的位点特异性修饰,某些位点的修饰效率可达100%[67]。由于TALE包含大量重复的结构域,增加了合成新变体的难度。利用密码子稀缺性特点和Ⅱ型核酸酶发明了一系列连接子的同源体用于连接每个重复单体,可实现根据级别合成、定制重复结构域,并用此方法成功合成了17个特异调控人细胞内源性Sox2和Klf4基因的TALE[64]。最新研究利用TALE转录抑制子文库 (Transcription activator-like effector repressors,TALERs),在哺乳动物细胞中进行模块化拼装,以合成基因线路的研究方法[68]。TALERRs由26种正交、可逆的TALE转录抑制子组成,与新设计的、可与之搭配的启动子结合后,阻挡转录起始因子的组装,从而抑制基因转录。通过计算输入/输出转移函数,可准确预测TALER介导的基因级联线路和基因开关线路功能。该研究是哺乳动物合成生物学领域内一项突破性技术进展。
5 总结和展望基于CRISPR的基因调控为合成生物学在大规模活细胞基因线路调控上提供了新的机遇和无限的可能。尽管目前已经取得较大的进展和成绩,但是合成生物学发展的步伐仍需加速,其中一个限制因素就是不能有效地设计、合成以特定的序列为靶点、高度特异性的转录元件,并且有效地调控靶基因。基于CRISPR方法操作的简便性及调控的高效性,使用该方法获得合成型转录元件无疑是合成生物学的一个重要突破,也使科研人员能投入更多时间和精力到整体基因线路的设计上。
如前所述,利用dCas9与不同元件融合,不仅可实现基因表达的干扰或沉默 (CRISPR interference,CRISPRi)[44],还有基因表达的激活 (CRISPR activation,CRISPRa)[45]和基因的表观遗传学修饰 (Epigenetic editing)[69],甚至对全基因组进行调控 (激活和/或抑制)[70]、对多基因进行“平行”调控[48],以及在人iPS细胞及其诱导分化的细胞中实现高效的转录调控[71]。CRISPR/Cas技术的出现和发展,以其可大规模、高精度操作和低成本的特点,克服了一般合成生物学技术的瓶颈,大大促进了合成生物学的进步。
将来,充分利用CRISPR的优势会使合成生物学取得更加迅速、长足的发展。合成生物学的发展不仅促进基础科学研究,更具有广泛的实用性[72-73],包括合成生物燃料、商业化合物,检测环境,利用微生物净化有毒废物场或受污染水域等生物治理以及精准医学治疗[74-75]。CRISPR技术允许调控多个基因组内源基因,可以最大程度上模拟细胞内动态、复杂的状态,如细胞分化的机制[76],以揭示生物体各种复杂表型的分子学机制;另外,表达的多个向导RNA与多种CRISPR转录元件结合到一起,组合搭配成更多的调控元件,可用于建立更大规模、更高级别的基因合成线路。由于可以方便地设计向导RNA以激活或抑制微生物合成路径中的多个基因,微生物代谢产物的产量将得到优化,同时又可利用dCas9抑制细菌或病原菌中抗生素耐药基因的表达[77],这将促使微生物代谢工程学的发展加速前进。
合成生物学正在加速渗透到生物医学领域,正在对现代生物医学产生深刻的影响。目前普通的基因治疗只能靶向一个基因,因此只适用于单基因遗传病。而合成生物学的发展可以允许我们采用“基因线路疗法”,即通过CRISPR方法精准地调控多个基因,使得治疗多基因疾病成为可能。
而合成生物学在肿瘤免疫治疗领域也在飞速崛起。将合成生物学原理应用于肿瘤治疗使得科学家可以进行免疫细胞的设计。比如通过设计生产特异靶向的CAR-T细胞 (Chimeric antigen receptor T cells),正在开展的临床试验证明CAR-T对于治疗慢性淋巴白血病 (Chronic lymphocytic leukemia,CLL) 有较好的疗效[78]。而这一技术的核心是免疫细胞的设计,就是依据合成生物学的理念设计开发的。
展望未来,我们相信合成生物学的发展会允许我们将细胞作为药物来加以使用。工程化的细胞将成为独立于小分子药物和生物制药 (如抗体等) 以外的新药物。将工程化细胞作为药物有很多优点:比如可以在细胞中编程复杂的逻辑,让其识别更多样的外部信号组合,并根据这些信号作出判断以指导功能输出 (比如杀死癌细胞)。而这一整套从感应器到处理器再到执行器的系统功能恰好是化合物小分子等药物无法实现的。通过改造、设计细胞使其具有新的功能,为治疗癌症、阿兹海默症和自免疫系统疾病带来希望,而这也将催生出一个新的产业,我们称为“细胞设计工厂”。可以想象,未来的医学是依赖于“细胞设计工厂”来精准治疗复杂的疾病。在精准医疗的框架下,医生可以制定有针对性的、多样化的细胞治疗策略。而“细胞设计工厂”则将医疗策略通过编程、设计细胞的方法,将其转化为可以用于治疗的细胞产品。而这一产业链则可以最大可能地实现高效、安全、通用、低成本的未来医学理念,也是我们预期未来医学合成生物学发展的关系到国计民生的一个重要方向。
致谢: 感谢斯坦福大学生物工程系亓磊教授实验室全体成员,尤其是博士后王海峰在图片制作过程中提供了帮助。| [1] | Tsai CS, Kwak S, Turner TL, et al. Yeast synthetic biology toolbox and applications for biofuel production. FEMS Yeast Res, 2015, 15(1): 1–15. DOI: 10.1093/femsyr/fou003 |
| [2] | Teo WS, Ling H, Yu AQ, et al. Metabolic engineering of Saccharomyces cerevisiae for production of fatty acid short and branched-chain alkyl esters biodiesel. Biotechnol Biofuels, 2015, 8: 177. DOI: 10.1186/s13068-015-0361-5 |
| [3] | Widhe M, Johansson J, Hedhammar M, et al. Invited review current progress and limitations of spider silk for biomedical applications. Biopolymers, 2012, 97(6): 468–478. DOI: 10.1002/bip.v97.6 |
| [4] | Dvorak P, Bidmanova S, Damborsky J, et al. Immobilized synthetic pathway for biodegradation of toxic recalcitrant pollutant 1, 2, 3-trichloropropane. Environ Sci Technol, 2014, 48(12): 6859–6866. DOI: 10.1021/es500396r |
| [5] | Benedetti I, de Lorenzo V, Nikel PI. Genetic programming of catalytic Pseudomonas putida biofilms for boosting biodegradation of haloalkanes. Metab Eng, 2016, 33: 109–118. DOI: 10.1016/j.ymben.2015.11.004 |
| [6] | Chakravarti D, Wong WW. Synthetic biology in cell-based cancer immunotherapy. Trends Biotechnol, 2015, 33(8): 449–461. DOI: 10.1016/j.tibtech.2015.05.001 |
| [7] | Chen GQ. Synthetic biology: research perspectives from China. ACS Synth Biol, 2012, 1(7): 251. DOI: 10.1021/sb300057c |
| [8] | Cameron DE, Bashor CJ, Collins JJ. A brief history of synthetic biology. Nat Rev Microbiol, 2014, 12(5): 381–390. DOI: 10.1038/nrmicro3239 |
| [9] | Jusiak B, Cleto S, Perez-Piñera P, et al. Engineering synthetic gene circuits in living cells with CRISPR technology. Trends Biotechnol, 2016, 34(7): 535–547. DOI: 10.1016/j.tibtech.2015.12.014 |
| [10] | Brophy JAN, Voigt CA. Principles of genetic circuit design. Nat Methods, 2014, 11(5): 508–520. DOI: 10.1038/nmeth.2926 |
| [11] | Lienert F, Lohmueller JJ, Garg A, et al. Synthetic biology in mammalian cells: next generation research tools and therapeutics. Nat Rev Mol Cell Biol, 2014, 15(2): 95–107. DOI: 10.1038/nrm3738 |
| [12] | Liu CC, Qi L, Lucks JB, et al. An adaptor from translational to transcriptional control enables predictable assembly of complex regulation. Nat Methods, 2012, 9(11): 1088–1094. DOI: 10.1038/nmeth.2184 |
| [13] | Lohmueller JJ, Armel TZ, Silver PA. A tunable zinc finger-based framework for Boolean logic computation in mammalian cells. Nucleic Acids Res, 2012, 40(11): 5180–5187. DOI: 10.1093/nar/gks142 |
| [14] | Moon TS, Lou C, Tamsir A, et al. Genetic programs constructed from layered logic gates in single cells. Nature, 2012, 491(7423): 249–253. DOI: 10.1038/nature11516 |
| [15] | Siuti P, Yazbek J, Lu TK. Synthetic circuits integrating logic and memory in living cells. Nat Biotechnol, 2013, 31(5): 448–452. DOI: 10.1038/nbt.2510 |
| [16] | Ausländer S, Ausländer D, Müller M, et al. Programmable single-cell mammalian biocomputers. Nature, 2012, 487(7405): 123–127. |
| [17] | Deans TL, Cantor CR, Collins JJ. A tunable genetic switch based on RNAi and repressor proteins for regulating gene expression in mammalian cells. Cell, 2007, 130(2): 363–372. DOI: 10.1016/j.cell.2007.05.045 |
| [18] | Gardner TS, Gardner TS, Cantor CR. Construction of a genetic toggle switch in Escherichia coli. Nature, 2000, 403(6767): 339–342. DOI: 10.1038/35002131 |
| [19] | Farzadfard F, Lu TK. Genomically encoded analog memory with precise in vivo DNA writing in living cell populations. Science, 2014, 346(6211): 1256272. DOI: 10.1126/science.1256272 |
| [20] | You LC, Cox RS, Weiss R, et al. Programmed population control by cell-cell communication and regulated killing. Nature, 2004, 428(6985): 868–871. DOI: 10.1038/nature02491 |
| [21] | Bacchus W, Lang M, El-Baba MD, et al. Synthetic two-way communication between mammalian cells. Nat Biotechnol, 2012, 30(10): 991–996. DOI: 10.1038/nbt.2351 |
| [22] | Carroll D. Genome engineering with zinc-finger nucleases. Genetics, 2011, 188(4): 773–782. DOI: 10.1534/genetics.111.131433 |
| [23] | Li T, Huang S, Zhao X, et al. Modularly assembled designer TAL effector nucleases for targeted gene knockout and gene replacement in eukaryotes. Nucleic Acids Res, 2011, 39(14): 6315–6325. DOI: 10.1093/nar/gkr188 |
| [24] | Bedell VM, Wang Y, Campbell JM, et al. In vivo genome editing using a high-efficiency TALEN system. Nature, 2012, 491(7422): 114–118. DOI: 10.1038/nature11537 |
| [25] | Cong L, Ran FA, Cox D, et al. Multiplex genome engineering using CRISPR/Cas systems. Science, 2013, 339(6121): 819–823. DOI: 10.1126/science.1231143 |
| [26] | Mali P, Yang L, Esvelt KM, et al. RNA-guided human genome engineering via Cas9. Science, 2013, 339(6121): 823–826. DOI: 10.1126/science.1232033 |
| [27] | Brouns SJJ, Jore MM, Lundgren M, et al. Small CRISPR RNAs guide antiviral defense in prokaryotes. Science, 2008, 321(5891): 960–964. DOI: 10.1126/science.1159689 |
| [28] | Makarova KS, Haft DH, Barrangou R, et al. Evolution and classification of the CRISPR-Cas systems. Nat Rev Microbiol, 2011, 9(6): 467–477. DOI: 10.1038/nrmicro2577 |
| [29] | Makarova KS, Aravind L, Wolf YI, et al. Unification of Cas protein families and a simple scenario for the origin and evolution of CRISPR-Cas systems. Biol Direct, 2011, 6: 38. DOI: 10.1186/1745-6150-6-38 |
| [30] | Deltcheva E, Chylinski K, Sharma CM, et al. CRISPR RNA maturation by trans-encoded small RNA and host factor RNase Ⅲ. Nature, 2011, 471(7340): 602–607. DOI: 10.1038/nature09886 |
| [31] | Peters JM, Silvis MR, Zhao DH, et al. Bacterial CRISPR: accomplishments and prospects. Curr Opin Microbiol, 2015, 27: 121–126. DOI: 10.1016/j.mib.2015.08.007 |
| [32] | Walter JM, Chandran SS, Horwitz AA. CRISPR-cas-assisted multiplexing (CAM): simple same-day multi-locus engineering in yeast. J Cell Physiol, 2016, 231(12): 2563–2569. DOI: 10.1002/jcp.25375 |
| [33] | Port F, Bullock SL. Augmenting CRISPR applications in Drosophila with tRNA-flanked sgRNAs. Nat Methods, 2016, 13(10): 852–854. DOI: 10.1038/nmeth.3972 |
| [34] | Lo TW, Pickle CS, Lin S, et al. Precise and heritable genome editing in evolutionarily diverse nematodes using TALENs and CRISPR/Cas9 to engineer insertions and deletions. Genetics, 2013, 195(2): 331–348. DOI: 10.1534/genetics.113.155382 |
| [35] | Varshney GK, Carrington B, Pei WH, et al. A high-throughput functional genomics workflow based on CRISPR/Cas9-mediated targeted mutagenesis in zebrafish. Nat Protoc, 2016, 11(12): 2357–2375. DOI: 10.1038/nprot.2016.141 |
| [36] | Xu RF, Qin RY, Li H, et al. Generation of targeted mutant rice using a CRISPR-Cpf1 system. Plant Biotechnol J, 2016. DOI: 10.1111/pbi.12669 |
| [37] | Wang HY, Yang H, Shivalila CS, et al. One-step generation of mice carrying mutations in multiple genes by CRISPR/Cas-mediated genome engineering. Cell, 2013, 153(4): 910–918. DOI: 10.1016/j.cell.2013.04.025 |
| [38] | Yang H, Wang HY, Shivalila CS, et al. One-step generation of mice carrying reporter and conditional alleles by CRISPR/Cas-mediated genome engineering. Cell, 2013, 154(6): 1370–1379. DOI: 10.1016/j.cell.2013.08.022 |
| [39] | Li DL, Qiu ZW, Shao YJ, et al. Heritable gene targeting in the mouse and rat using a CRISPR-Cas system. Nat Biotechnol, 2013, 31(8): 681–683. DOI: 10.1038/nbt.2661 |
| [40] | Su YH, Lin TY, Huang CL, et al. Construction of a CRISPR-Cas9 system for pig genome targeting. Anim Biotechnol, 2015, 26(4): 279–288. DOI: 10.1080/10495398.2015.1027774 |
| [41] | Dever DP, Bak RO, Reinisch A, et al. CRISPR/Cas9 β-globin gene targeting in human haematopoietic stem cells. Nature, 2016, 539(7629): 384–389. DOI: 10.1038/nature20134 |
| [42] | Baresova V, Krijt M, Skopova V, et al. CRISPR-Cas9 induced mutations along de novo purine synthesis in HeLa cells result in accumulation of individual enzyme substrates and affect purinosome formation. Mol Genet Metab, 2016, 119(3): 270–277. DOI: 10.1016/j.ymgme.2016.08.004 |
| [43] | Yu C, Liu YX, Ma TH, et al. Small molecules enhance CRISPR genome editing in pluripotent stem cells. Cell Stem Cell, 2015, 16(2): 142–147. DOI: 10.1016/j.stem.2015.01.003 |
| [44] | Larson MH, Gilbert LA, Wang XW, et al. CRISPR interference (CRISPRi) for sequence-specific control of gene expression. Nat Protoc, 2013, 8(11): 2180–2196. DOI: 10.1038/nprot.2013.132 |
| [45] | Tanenbaum ME, Gilbert LA, Qi LS, et al. A protein-tagging system for signal amplification in gene expression and fluorescence imaging. Cell, 2014, 159(3): 635–646. DOI: 10.1016/j.cell.2014.09.039 |
| [46] | Hilton IB, D'Ippolito AM, Vockley CM, et al. Epigenome editing by a CRISPR-Cas9-based acetyltransferase activates genes from promoters and enhancers. Nat Biotechnol, 2015, 33(5): 510–517. DOI: 10.1038/nbt.3199 |
| [47] | Konermann S, Brigham MD, Trevino AE, et al. Genome-scale transcriptional activation by an engineered CRISPR-Cas9 complex. Nature, 2015, 517(7536): 583–588. |
| [48] | Zalatan JG, Lee ME, Almeida R, et al. Engineering complex synthetic transcriptional programs with CRISPR RNA scaffolds. Cell, 2015, 160(1/2): 339–350. |
| [49] | Nissim L, Perli SD, Fridkin A, et al. Multiplexed and programmable regulation of gene networks with an integrated RNA and CRISPR/Cas toolkit in human cells. Mol Cell, 2014, 54(4): 698–710. DOI: 10.1016/j.molcel.2014.04.022 |
| [50] | Kiani S, Chavez A, Tuttle M, et al. Cas9 gRNA engineering for genome editing, activation and repression. Nat Methods, 2015, 12(11): 1051–1054. DOI: 10.1038/nmeth.3580 |
| [51] | Esvelt KM, Mali P, Braff JL, et al. Orthogonal Cas9 proteins for RNA-guided gene regulation and editing. Nat Methods, 2013, 10(11): 1116–1121. DOI: 10.1038/nmeth.2681 |
| [52] | Liu YC, Zhan YH, Chen ZC, et al. Directing cellular information flow via CRISPR signal conductors. Nat Methods, 2016, 13(11): 938–944. DOI: 10.1038/nmeth.3994 |
| [53] | Liu YC, Zeng YY, Liu L, et al. Synthesizing AND gate genetic circuits based on CRISPR-Cas9 for identification of bladder cancer cells. Nat Commun, 2014, 5: 5393. DOI: 10.1038/ncomms6393 |
| [54] | Nielsen AAK, Voigt CA. Multi-input CRISPR/Cas genetic circuits that interface host regulatory networks. Mol Syst Biol, 2014, 10(11): 763. DOI: 10.15252/msb.20145735 |
| [55] | Gao YC, Xiong X, Wong S, et al. Complex transcriptional modulation with orthogonal and inducible dCas9 regulators. Nat Methods, 2016, 13(12): 1043–1049. DOI: 10.1038/nmeth.4042 |
| [56] | Polstein LR, Gersbach CA. A light-inducible CRISPR-Cas9 system for control of endogenous gene activation. Nat Chem Biol, 2015, 11(3): 198–200. DOI: 10.1038/nchembio.1753 |
| [57] | Yang LH, Guell M, Niu D, et al. Genome-wide inactivation of porcine endogenous retroviruses (PERVs). Science, 2015, 350(6264): 1101–1104. DOI: 10.1126/science.aad1191 |
| [58] | Shechner DM, Hacisuleyman E, Younger ST, et al. Multiplexable, locus-specific targeting of long RNAs with CRISPR-display. Nat Methods, 2015, 12(7): 664–670. DOI: 10.1038/nmeth.3433 |
| [59] | Geurts AM, Cost GJ, Freyvert Y, et al. Knockout rats via embryo microinjection of zinc-finger nucleases. Science, 2009, 325(5939): 433. DOI: 10.1126/science.1172447 |
| [60] | Urnov FD, Miller JC, Lee YL, et al. Highly efficient endogenous human gene correction using designed zinc-finger nucleases. Nature, 2005, 435(7042): 646–651. DOI: 10.1038/nature03556 |
| [61] | Bogdanove AJ, Schornack S, Lahaye T. TAL effectors: finding plant genes for disease and defense. Curr Opin Plant Biol, 2010, 13(4): 394–401. DOI: 10.1016/j.pbi.2010.04.010 |
| [62] | Khalil AS, Lu TK, Bashor CJ, et al. A synthetic biology framework for programming eukaryotic transcription functions. Cell, 2012, 150(3): 647–658. DOI: 10.1016/j.cell.2012.05.045 |
| [63] | Beerli RR, Dreier B, Barbas CF. Positive and negative regulation of endogenous genes by designed transcription factors. Proc Natl Acad Sci USA, 2000, 97(4): 1495–1500. DOI: 10.1073/pnas.040552697 |
| [64] | Zhang F, Cong L, Lodato S, et al. Efficient construction of sequence-specific TAL effectors for modulating mammalian transcription. Nat Biotechnol, 2011, 29(2): 149–153. DOI: 10.1038/nbt.1775 |
| [65] | Zhang ZH, Xiang D, Heriyanto F, et al. Dissecting the roles of miR-302/367 cluster in cellular reprogramming using TALE-based repressor and TALEN. Stem Cell Rep, 2013, 1(3): 218–225. DOI: 10.1016/j.stemcr.2013.07.002 |
| [66] | Christian M, Cermak T, Doyle EL, et al. Targeting DNA double-strand breaks with TAL effector nucleases. Genetics, 2010, 186(2): 757–761. DOI: 10.1534/genetics.110.120717 |
| [67] | Polstein LR, Perez-Pinera P, Kocak DD, et al. Genome-wide specificity of DNA binding, gene regulation, and chromatin remodeling by TALE-and CRISPR/Cas9-based transcriptional activators. Genome Res, 2015, 25(8): 1158–1169. DOI: 10.1101/gr.179044.114 |
| [68] | Li YQ, Jiang Y, Chen H, et al. Modular construction of mammalian gene circuits using TALE transcriptional repressors. Nat Chem Biol, 2015, 11(3): 207–213. DOI: 10.1038/nchembio.1736 |
| [69] | Gilbert LA, Larson MH, Morsut L, et al. CRISPR-mediated modular RNA-guided regulation of transcription in eukaryotes. Cell, 2013, 154(2): 442–451. DOI: 10.1016/j.cell.2013.06.044 |
| [70] | Gilbert LA, Horlbeck MA, Adamson B, et al. Genome-scale CRISPR-mediated control of gene repression and activation. Cell, 2014, 159(3): 647–661. DOI: 10.1016/j.cell.2014.09.029 |
| [71] | Mandegar MA, Huebsch N, Frolov EB, et al. CRISPR interference efficiently induces specific and reversible gene silencing in human iPSCs. Cell Stem Cell, 2016, 18(4): 541–553. DOI: 10.1016/j.stem.2016.01.022 |
| [72] | Khalil AS, Collins JJ. Synthetic biology: applications come of age. Nat Rev Genet, 2010, 11(5): 367–379. DOI: 10.1038/nrg2775 |
| [73] | Cheng AA, Lu TK. Synthetic biology: an emerging engineering discipline. Annu Rev Biomed Eng, 2012, 14(1): 155–178. DOI: 10.1146/annurev-bioeng-071811-150118 |
| [74] | Boyle PM, Silver PA. Parts plus pipes: synthetic biology approaches to metabolic engineering. Metab Eng, 2012, 14(3): 223–232. DOI: 10.1016/j.ymben.2011.10.003 |
| [75] | Ye HF, Aubel D, Fussenegger M. Synthetic mammalian gene circuits for biomedical applications. Curr Opin Chem Biol, 2013, 17(6): 910–917. DOI: 10.1016/j.cbpa.2013.10.006 |
| [76] | Chavez A, Scheiman J, Vora S, et al. Highly efficient Cas9-mediated transcriptional programming. Nat Methods, 2015, 12(4): 326–328. DOI: 10.1038/nmeth.3312 |
| [77] | Bikard D, Scheiman J, Vora S, et al. Programmable repression and activation of bacterial gene expression using an engineered CRISPR-Cas system. Nucleic Acids Res, 2013, 41(15): 7429–7437. DOI: 10.1093/nar/gkt520 |
| [78] | Fesnak AD, June CH, Levine BL. Engineered T cells: the promise and challenges of cancer immunotherapy. Nat Rev Cancer, 2016, 16(9): 566–581. DOI: 10.1038/nrc.2016.97 |
 2017, Vol. 33
2017, Vol. 33