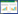中国科学院微生物研究所、中国微生物学会主办
文章信息
- 常汉臣, 王琛, 王培霞, 周见庭, 李炳志
- Chang Hanchen, Wang Chen, Wang Peixia, Zhou Jianting, Li Bingzhi
- DNA组装技术
- DNA assembly technologies: a review
- 生物工程学报, 2019, 35(12): 2215-2226
- Chinese Journal of Biotechnology, 2019, 35(12): 2215-2226
- 10.13345/j.cjb.190273
-
文章历史
- Received: June 24, 2019
- Accepted: August 30, 2019
- Published: October 10, 2019
2. 天津大学化工学院 化学科学与工程协同创新中心,天津 300072
2. Collaborative Innovation Center of Chemical Science and Engineering (Tianjin), School of Chemical Engineering and Technology, Tianjin University, Tianjin 300072, China
合成生物学旨在应用工程学的研究思路及手段去设计改造基因元件、生物途径,甚至合成基因组[1],是一个综合了科学与工程的新兴研究领域,在生物、医药、农业、能源及环保等方面具有巨大的应用潜力。DNA组装方法是整个合成生物学的基础[2]。合成生物学依赖于将组装的特定DNA片段导入底盘内发挥功能来实现意图,因此,高效的DNA组装是合成生物学的关键技术之一。随着生物科学研究的发展,对需要调控的基因功能需求越来越大,DNA长度一般情况下与其功能多少是正相关的,这就对DNA组装技术提出了越来越高的要求。尤其是近年来快速发展的基因组设计合成领域,更是需要超大DNA片段的组装技术的支撑。文中将主要从几种常用和近期发展的DNA组装技术展开阐述。
1 酶依赖的DNA组装 1.1 基于DNA聚合酶的DNA组装19世纪80年代中期,PCR的发明为依赖于DNA聚合酶的DNA组装技术的兴起与发展创造了良好的基础[3-4]。依赖于DNA聚合酶的DNA组装方法主要是利用DNA聚合酶的外切活性和聚合作用可以高效地将几个DNA片段组装在一起,现在已经发展出几种比较常用的技术,如聚合酶循环组装技术、重叠延伸PCR技术等。
聚合酶循环组装(Polymerase cycling assembly,PCA)是基于PCR技术,可将10−20条长度为40−70 bp的寡核苷酸片段组装成长片段。PCA组装的基本思路是将可化学合成的寡核苷酸通过无模板PCR组装成短的DNA片段。1989年,Pease等[5]提出重叠延伸PCR技术(Overlap extension polymerase chain reaction,OE-PCR),这种方法可以用于组装更长片段的DNA。OE-PCR示意图如图 1所示,将末端具有重叠序列的DNA片段通过变性、退火,然后互为引物,经聚合酶延伸得到融合的DNA,一般可以将2−6个DNA片段按比例混合作为模板,以最外侧两端的寡核苷酸作为引物,进行重叠延伸,同时要保证相邻的两个DNA片段之间有20−40 bp的同源重叠区。由于OE-PCR方法操作简单,省时省力,已经得到了广泛的应用[6]。2003年,Smith等[7]将连接酶拼接法(Ligase chain reaction,LCR)与重叠延伸PCR法相结合,合成了噬菌体φX174基因组全长序列(5 386 bp)。
|
| 图 1 OE-PCR方法示意图(将待组装的两个DNA片段分别用一对引物通过PCR扩增,使PCR产物之间有同源区段。接着,用F1和R2引物通过PCR扩增得到完整双链目的片段) Fig. 1 Schematic diagram of the OE-PCR method. The two DNA fragments to be assembled were separately amplified by PCR using a pair of primers having homologous segments between the PCR products. In further, the complete double-stranded fragment of interest was amplified by PCR using F1 and R2 primers. |
| |
BioBrick最初是由美国麻省理工学院的Knight研究组于2003年提出,BioBrick方法示意图如图 2所示。该方法是利用一对同尾酶和两个非同尾酶来将载体和DNA元件标准化,形成元件库;标准化的元件可以通过DNA连接酶作用根据顺序依次组装起来[8]。同尾酶是一类基因工程重要的工具酶,在发挥作用时识别的位点不相同,但是酶切之后形成的粘性末端是相同的。常用的同尾酶有:XbaⅠ/NheⅠ/SpeⅠ、BamHⅠ/BglⅡ、SalⅠ/XhoⅠ等。

|
| 图 2 BioBrick方法示意图(SpeⅠ和XbaⅠ是一对同尾酶,用SpeⅠ和XbaⅠ分别酶切DNA片段后得到的粘性末端相同,碱基互补之后原酶切位点也消失,片段成功组装) Fig. 2 Schematic diagram of the BioBrick method. SpeⅠ and XbaⅠ are a pair of homologous enzymes. After the DNA fragments were digested with SpeⅠ and XbaⅠ, the sticky ends were the same. When the bases were complementary, the original cleavage sites disappeared and the fragments were successfully assembled. |
| |
基于同尾酶酶切的连接组装方法根据所使用的同尾酶和非同尾酶的数量又可以分为BioBrick、BglBrick和ePathBrick。此类方法兴起以后产生了一大批合成生物学领域非常有价值的生物组件和途径,推动了合成生物学的发展[9-11]。这种方法的优势是可以实现元件的标准化和即插即用。但是两个DNA元件之间有6 bp的残痕,元件组装通量较低[12]。针对这种方法存在的问题,科学家们想出了两种方案,即BglBrick和ePathBrick,其主旨都是将残痕转化为融合蛋白的连接肽[13-14]。其中BglBrick采取多基因共表达的策略,要求每个基因都带有自身的表达元件,最后利用限制性同尾酶将各个元件串联起来,独立进行表达。Anderson等使用一对同尾酶(BglⅡ和BamHⅠ)、非同尾酶(EcoRⅠ和XhoⅠ)构建标准化组装载体,巧妙地将这6 bp残痕设计为两个氨基酸,既解决了DNA残痕问题,又实现了融合蛋白构建,可谓一举两得[15]。
1.2.2 Golden Gate技术Golden Gate组装是利用ⅡS类限制性核酸内切酶识别位点与切割位点不同的特性,灵活设计不同的粘性末端,从而实现同时组装多个DNA片段,如图 3所示。这一方法通过一步酶切连接,可以高效地构建得到重组质粒,从而实现多片段一步法无缝连接[16-18]。Engler等[19]利用上述原理结合基因改组技术(Gene shuffling),创造性地一次性完成了3个片段与载体的拼接,构建了理论上可达19 683种不同的重组胰蛋白酶原基因,以筛选高效表达的胰蛋白酶突变体。中国科学院深圳先进技术研究院在此技术基础上,设计了YeastFab和EcoExpress两个组装系统,拼接效率可达90%以上,主要用于工程细胞的代谢通路优化和蛋白表达[20-21]。

|
| 图 3 Golden Gate方法示意图(RFP全称是Red Fluorescent Protein.带有RFP基因的载体在组装过程有助于初步筛选阳性克隆子. BsaⅠ是ⅡS类限制性核酸内切酶.用其分别切割带有基因1、基因2、RFP的载体,得到带有粘性末端的片段和载体.最后,通过连接酶成功将基因1和基因2组装到原带有RFP的载体上) Fig. 3 Schematic diagram of the Golden Gate method. The full name of the RFP is Red Fluorescent Protein. The vector carrying the RFP gene facilitates the preliminary screening of positive clones during assembly. BsaⅠ is an ⅡS restriction endonuclease. The vector carrying the gene 1, gene 2, RFP was cleaved with BsaⅠ, respectively, obtaining two fragments having a sticky end and a vector. Finally, Gene 1 and Gene 2 were successfully assembled into the original vector containing RFP by ligase. |
| |
除此之外,近几年一些新发展的基于核酸内切酶的组装方法,如MASTER技术[22]、不完全依赖于重叠序列的拼接方法USER[23]、PSA技术[24],提升了科研人员操作DNA的能力,部分方法已经应用到合成生物学的各个方面[25]。
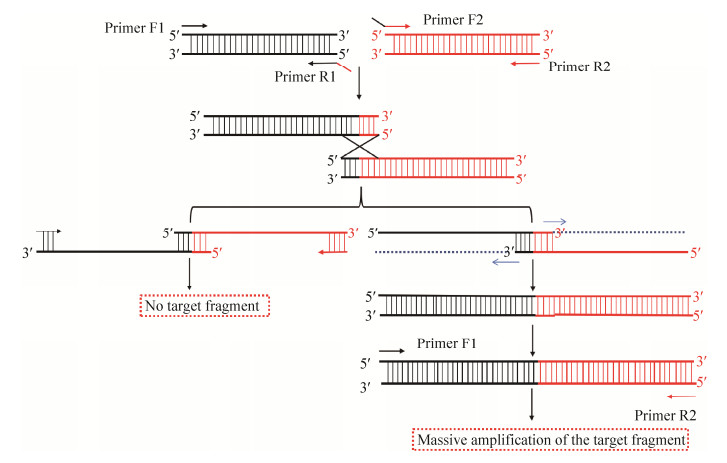
1.3 基于核酸外切酶的组装 1.3.1 Gibson组装技术Gibson组装是2009年由Gibson开发,进行DNA多片段体外一步拼接的技术[26]。Gibson组装方法示意见图 4,在反应体系中加入核酸外切酶、Pusion DNA聚合酶和Taq DNA连接酶,50 ℃下反应60 min即可完成组装。Gibson组装可以实现无缝拼接,而且组装尺度可以达到百kb大小。Gibson等[27]通过调节酶比例成功组装成163 kb的小鼠线粒体基因。
|
| 图 4 Gibson组装方法示意图(利用T5核酸外切酶的5’外切酶活性酶切片段A和片段B,然后Phusion DNA聚合酶催化填补空缺,Taq连接酶修补切口) Fig. 4 Schematic diagram of the Gibson assembly method. Fragment A and Fragment B were digested with the 5' exonuclease activity of T5 exonuclease; then Phusion DNA polymerase catalyzed the filling of the gap; finally, Taq ligase repaired the incision. |
| |
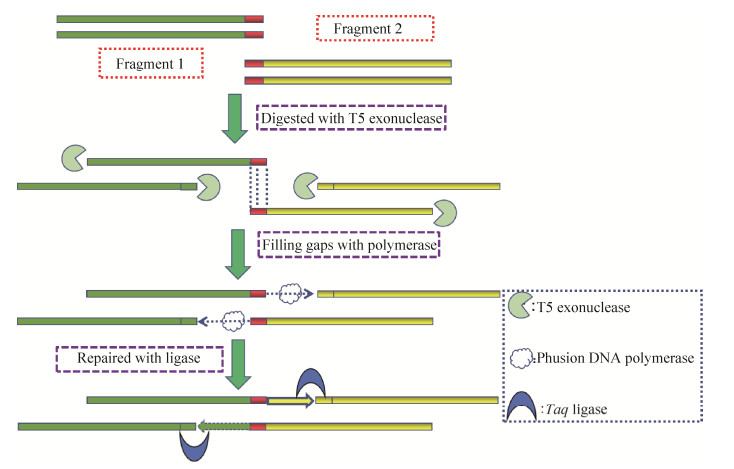
SLIC组装方法是利用T4 DNA聚合酶的外切活性,产生不同单链DNA末端,然后采用单链退火或RecA介导的体外重组,一次反应可以拼接5−10个DNA片段,SLIC组装方法示意图如图 5所示。SLIC一次性的组装较多片段时,需要片段之间有比较长的重叠区。SLIC法可进行多片段的平行组装,是构建生物途径的重要技术[28]。
|
| 图 5 SLIC组装方法示意图(用一对带有重叠序列的特异性引物扩增目的基因,用限制性内切酶或PCR扩增得到线性化质粒;接着,T4 DNA聚合酶分别处理PCR扩增得到的目的基因和线性化质粒,产生5ʹ突出端的粘性末端;最后,目的基因和线性化质粒经过重叠序列间的退火,得到带有“缺口”的环状质粒) Fig. 5 Schematic diagram of the SLIC assembly method. The target gene is amplified by a pair of specific primers with overlapping sequences, and the linearized plasmid is amplified by restriction endonuclease or PCR; then, the target gene and linearized plasmid obtained by PCR amplification are respectively treated by T4 DNA polymerase. The sticky end of the 5ʹ overhang is generated; finally, the target gene and the linearized plasmid are annealed between the overlapping sequences to obtain a circular plasmid with a "nick". |
| |
2009年,Elledge研究组[29]就是利用该方法成功实现了9个275−980 bp长度的DNA片段的一步拼接。后来,科学家又提出了SLIC组装方法的改进版SLiCE组装方法。SLICE与SLIC的不同在于它不需要额外的聚合酶和DNA连接酶,操作简单,省时省力[30]。
2 非酶依赖的DNA组装虽然酶依赖的DNA组装方法有高效、操作简单的优势,但也有其缺陷。比如,商业化限制性内切核酸酶的数量有限,大的基因片段有时很难找到合适的限制性酶切位点等。而非酶依赖的DNA组装方法在没有酶的情况下也能实现DNA组装且成本较低,在高通量组装实验条件下,非酶组装优势明显。非酶依赖的DNA组装技术主要有TPA技术和EFC技术等。
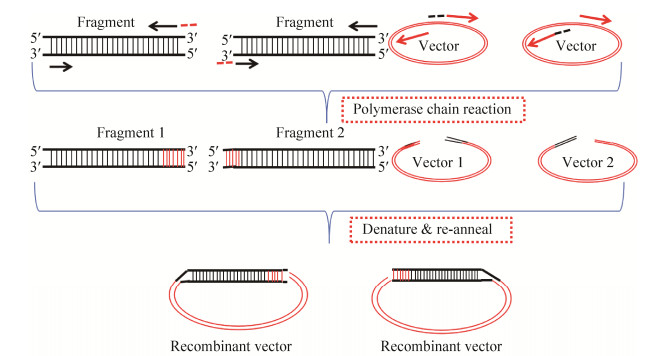
2.1 EFC技术EFC (Enzyme-free cloning)组装技术,是一种非酶依赖的DNA组装方法[31]。该技术不受限于限制性内切酶位点,具有快速可靠、简便高效的优点。该方法利用带尾引物使插入的片段与载体在PCR变性反应之后交错互补。具体来说就是对载体和片段分别进行两次PCR。虽然都是PCR,但是所用的引物是有区别的。一次PCR所用引物是用5ʹ短和3ʹ长(尾)引物,另一次PCR则使用5ʹ长和3ʹ短引物;长引物与短引物之间的区别在于长引物多了12−15 bp的尾巴。4次PCR过后两个非同源的待插入片段分别与两个载体中的一个互补,从而确保所需片段的定向克隆。将4种PCR产物的等摩尔体积混合,热变性和重新退火;从得到的产物中选择所需要的低温退火,最后得到目的片段。EFC方法示意图见图 6。
|
| 图 6 EFC组装方法示意图 Fig. 6 Schematic diagram of the EFC assembly method. |
| |
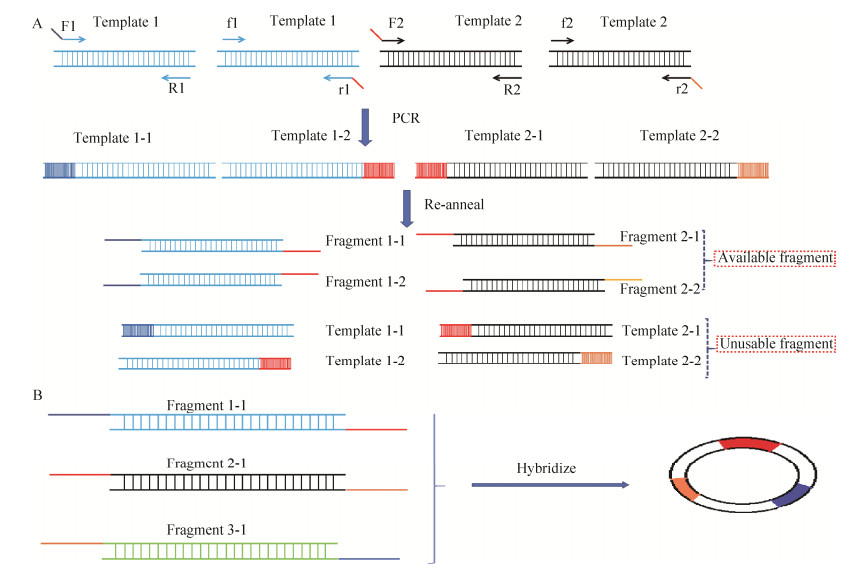
2017年,赵惠民教授的科研团队[32]提出一种高效准确的多片段DNA组装方法(具体组装流程见图 7),即Twin-primer non-enzymatic DNA assembly (TPA)。该组装方法在不使用酶的情况下能够将聚合酶链式反应扩增的片段组装成质粒,并且不留下疤痕。尽管在整个过程中都没有酶的参与,但是该方法的效果却可以和最佳的体外组装方法相当。具体操作分为两步:在第一步中,设计长上引物和短下引物以及短上引物和长下引物,利用聚合酶链式反应分别对片段进行扩增,长引物的设计为片段扩增出片段之间的同源区段。值得注意的是第一步中产生了不需要的扩增片段,需剔除。第二步中,将第一步中得到的正确的扩增片段通过退火组装成一个质粒,验证正确后转化到菌内。
|
| 图 7 TPA组装方法示意图 Fig. 7 Schematic diagram of TPA assembly method. |
| |
尽管体外拼装的片段大小已经可达几百kb,但是所得的量依然不足以进行后续实验[33]。微生物体内的同源重组使高效组装更大的DNA片段成为可能。同源重组是借由重组酶的催化作用,通过两个具有同源序列DNA分子间的交换,从而使序列发生重组。这种生物学现象在自然界正常细胞体内普遍存在。而基于同源重组的DNA组装是人工控制同源重组酶的酶切和交换功能,在体内把同源片段重组的组装方法。该方法是非常重要的遗传操作技术,广泛应用于DNA元件的组装、克隆、置换、敲除、突变等。常用的同源重组工具菌株包括酿酒酵母和枯草芽孢杆菌。
3.1 TAR技术酿酒酵母具有高效同源重组的能力,已经发展了TAR (Transformation-associated recombination)技术。TAR组装方法示意见图 8。酵母的同源重组可以组装寡核苷酸,也能组装很长的DNA片段,乃至细菌的基因组。

|
| 图 8 TAR技术合成基因示意图 Fig. 8 Schematic diagram of TAR technology synthesis gene. |
| |
2008年,Venter研究组[34]利用该方法在酿酒酵母体内完成了对生殖道支原体Mycoplasma genitalium基因组(582 970 bp)的最后一步组装。2010年,他们又成功完成了大小为1 080 Mb的丝状支原体Mycoplasma mycoides基因组在酿酒酵母体内的同源组装[35]。Shao等[36]采用类似的“DNA Assembler”法将两个生物合成途径共8个基因构建到一个载体上,并成功地检测到了代谢产物。2017年,由酵母基因组合成计划SC2.0联盟成员完成了酿酒酵母5条染色体的人工设计与合成,主要是利用了酿酒酵母同源重组能力实现了合成染色体片段对野生染色体片段的替换[37-43]。酵母细胞内组装可广泛应用于基因元件、代谢途径和基因组的组装,为后续的科学研究提供良好的材料。
3.2 CasHRA技术CasHRA技术是由中国科学院植物生理生态研究所覃重军研究员团队开发的。这种方法能够在体内有效组装多个大DNA片段。主要是利用RNA引导的Cas9核酸酶切割早先引入酿酒酵母中的大的环状DNA,从而使环状DNA变成线性,最终利用内源性同源重组系统进行组装。该课题组将此方法与上游装配方法相结合,成功构建了一个包含449个必需基因和267个重要生长基因的1.03 Mb MGE-syn1.0 (Minimal genome of Escherichia coli)[44]。该方法将对兆碱基大小的基因组的构建产生深刻的影响。
3.3 枯草芽孢杆菌体内的同源重组枯草芽孢杆菌中也有强大的重组系统。利用枯草体内的重组系统同样可将两端带同源序列的片段通过重组的方法连接起来。2005年,Itaya等[45]将3.5 Mb的集胞藻PCC6803的基因组成功克隆到4.2 Mb的枯草芽孢杆菌基因组中,所用方法被称为“蠕动延伸法”。在此方法的基础上,Itaya等[46]进一步开发了一种新的“多米诺法”,利用这种方法成功合成了16.3 kb的小鼠线粒体基因组以及134.5 kb的水稻叶绿体基因组。这种方法所用的底盘细胞是整合了pBR322序列的枯草芽孢杆菌。所用策略是将待合成的基因拆分成带有同源区段的5 kb片段,然后分别将其构建到不同的载体上,通过逐步替换,将所有的片段和抗性整合到枯草芽孢杆菌的BGM载体位点。这种组装方法由于需较长的同源臂以及耗费时间,目前未得到普遍使用。
除酵母和枯草芽孢杆菌可以利用自身的同源重组酶组装大片段的DNA之外,部分细菌通过超表达T4连接酶或整合λ Red重组系统也能够介导大片段DNA的胞内组装。将待组装的DNA片段导入宿主细胞内即可进行组装,通过筛选可得到目的片段。
3.4 Cre/loxP介导的DNA体内组装Cre/loxP重组酶系统是由Sternberg和Hamilton提出。Cre是一种来源于P1噬菌体的重组酶,Cre重组酶在没有辅助因子的情况下催化2个loxP位点之间的位点特异性重组反应[47]。loxp是一段长度为34 bp的DNA序列,由2个13 bp的反向重复序列和1个8 bp的不对称间隔区所分隔的回文结构组成,其是重组酶介导重组反应所必需的条件[48]。Cre重组酶根据2个loxP位点的排列方向介导4种不同的重组方式:1)删除。当同一条DNA分子上的2个loxP位点的排列方向相同时,则可能出现2个loxP位点之间的基因被删除的情况,最终只剩下一个loxP位点,这种方式是Cre/loxP重组酶系统最主要的作用方式。2)交叉。如果基因组中的不同DNA分子上各有loxP位点时,可能出现loxP位点前后基因发生交叉换位。3)移位。当基因两端的loxP位点方向相同时,则可能发生移位,转移到另一个位置上单独的loxP位点上。4)颠倒。同一条DNA分子上2个loxP位点方向相反时,则2个loxP位点之间的基因可能会发生颠倒。Cre/loxP重组酶系统不受制于位置以及片段长度,已经广泛应用于体内组装、体外应用中。体外应用聚焦于高通量DNA克隆和腺病毒载体构建[49-50],体内的应用则主要集中于基因的替换和敲除以及染色体畸变[51-52],拥有广阔的应用前景。
4 展望合成生物学近几年得到了飞跃式的发展,不同尺度的DNA组装方法相继诞生,为我们不断探索更长的片段组装提供了可能,特别是超大DNA的组装也越来越成为可能。不同的组装技术具有不同的适用性,通常的策略都是几项技术的联合使用。学科交叉也一定程度上推动了DNA组装技术的发展。但还是存在一些问题需要我们去解决。一方面是虽然目前我们组装的片段长度越来越长,但还是有一定的限制,需要开发更加高效的组装方法。近些年不断发展的DNA酶法合成技术为实现更长DNA片段的直接合成提供了良好的思路,其是一种高效、低耗的DNA合成方案,值得不断地去研究与拓展。另一方面DNA片段在连接过后可能会有疤痕存在,可能会对后续实验有影响,同时,组装的准确度和可调性也需要我们不断去探索更好的方法去解决。这就需要在深入揭示相关机制的基础上,不断开发新的分子生物学技术,各类组装技术的特点见图 9。

|
| 图 9 组装技术的总结 Fig. 9 Summary of assembly technology. |
| |
| [1] |
Zhao GR. Modern Pharmaceutical Technology. Beijing: Tsinghua University Press, 2015 (in Chinese). 赵广荣. 现代制药工艺学. 北京: 清华大学出版社, 2015. |
| [2] |
Chao R, Yuan YB, Zhao HM. Construction of synthetic biology manufacturing plant. China Science: Life Science, 2015, 45(10): 976-984 (in Chinese). 晁然, 原永波, 赵惠民. 构建合成生物学制造厂. 中国科学:生命科学, 2015, 45(10): 976-984. |
| [3] |
Saiki RK, Scharf S, Faloona F, et al. Enzymatic amplification of beta-globin g-enomic sequences and restriction site analysis for diagnosis of sickle cell anemia. Science, 1985, 230(1985): 1350-1354. |
| [4] |
Saiki RK, Gelfand DH, Stoffel S, et al. Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase. Science, 1988, 239(1988): 487-491. |
| [5] |
Horton RM, Hunt HD, Ho SN, et al. Engineering hybrid genes without the use of restriction enzymes: gene splicing by overlap extension. Gene, 1989, 77(1): 61-68. DOI:10.1016/0378-1119(89)90359-4 |
| [6] |
Zhai L, Dong N, Zhang YH, et al. Overlap extension without restriction sites. Application of PCR in clonal expression. J Nanchang Univer: Sci Ed, 2012, 36(3): 273-276, 281 (in Chinese). 翟玲, 董娜, 张雅慧, 等. 不需酶切位点的重叠延伸PCR在克隆表达中的应用. 南昌大学学报:理科版, 2012, 36(3): 273-276, 281. |
| [7] |
Smith HO, Hutchison Ⅲ CA, Pfannkoch C, et al. Generating a synthetic genome by whole genome assembly: φX174 bacteriophage from synthetic oligonucleotides. Proc Natl Acad Sci USA, 2003, 100(26): 15440-15445. DOI:10.1073/pnas.2237126100 |
| [8] |
Knight T. Idempotent Vector Design for Standard Assembly of Biobricks. MIT Artificial Intelligence Laboratory; MIT Synthetic Biology Working Group, 2003.
|
| [9] |
Danino T, Mondragón-Palomino O, Tsimring L, et al. A synchronized quorum of genetic clocks. Nature, 2010, 463(7279): 326-330. DOI:10.1038/nature08753 |
| [10] |
Friedland AE, Lu TK, Wang X, et al. Synthetic gene networks that count. Science, 2009, 324(5931): 1199-1202. DOI:10.1126/science.1172005 |
| [11] |
Basu S, Gerchman Y, Collins CH, et al. A synthetic multicellular system for programmed pattern formation. Nature, 2005, 434(7037): 1130-1134. DOI:10.1038/nature03461 |
| [12] |
Shetty RP, Endy D, Knight TF Jr. Engineering BioBrick vectors from BioBrick parts. J Biol Eng, 2008, 2: 5. DOI:10.1186/1754-1611-2-5 |
| [13] |
Phillips I, Silver P. A new biobrick assembly strategy designed for facile protein engineering. (2006-04-20). http://dspace.mit.edu/handle/1721.1/32535.
|
| [14] |
Grünberg R, Arndt K, Müller K. Fusion Protein (Freiburg) Biobrick assembly standard. (2009-04-18), http://dspace.mit.edu/handle/1721.1/45140.
|
| [15] |
Anderson JC, Dueber JE, Leguia M, et al. BglBricks: a flexible standard for biological part assembly. J Biol Eng, 2010, 4: 1. DOI:10.1186/1754-1611-4-1 |
| [16] |
Engler C, Kandzia R, Marillonnet S. A one pot, one step, precision cloning method with high throughput capability. PLoS ONE, 2008, 3(11): e3647. DOI:10.1371/journal.pone.0003647 |
| [17] |
Engler C, Gruetzner R, Kandzia R, et al. Golden gate shuffling: a one-pot DNA shuffling method based on type Ⅱs restriction enzymes. PLoS ONE, 2009, 4(5): e5553. DOI:10.1371/journal.pone.0005553 |
| [18] |
Sarrion-Perdigones A, Falconi EE, Zandalinas SI, et al. GoldenBraid: an iterative cloning system for standardized assembly of reusable genetic modules. PLoS ONE, 2011, 6(7): e21622. DOI:10.1371/journal.pone.0021622 |
| [19] |
Engler C, Marillonnet S. Generation of families of construct variants using golden gate shuffling//Lu C, Browse J, Wallis J, eds. cDNA Libraries. London: Humana Press, 2011, 729: 167−181.
|
| [20] |
Guo YK, Dong JK, Zhou T, et al. YeastFab: the design and construction of standard biological parts for metabolic engineering in Saccharomyces cerevisiae. Nucleic Acids Res, 2015, 43(13): e88. DOI:10.1093/nar/gkv464 |
| [21] |
Qin YR, Tan C, Lin JW, et al. Ecoexpress-highly efficient construction and expression of multicomponent protein complexes in Escherichia coli. ACS Synth Biol, 2016, 5(11): 1239-1246. DOI:10.1021/acssynbio.5b00291 |
| [22] |
Chen WH, Qin ZJ, Wang J, et al. The MASTER (methylation-assisted tailorable ends rational) ligation method for seamless DNA assembly. Nucleic Acids Res, 2013, 41(8): e93. DOI:10.1093/nar/gkt122 |
| [23] |
Nour-Eldin HH, Geu-Flores F, Halkier BA. USER cloning and USER fusion: the ideal cloning techniques for small and big laboratories//Fett-Neto A, ed. Plant Secondary Metabolism Engineering. Totowa, NJ: Humana Press, 2010, 643: 185–200.
|
| [24] |
Blake WJ, Chapman BA, Zindal A, et al. Pairwise selection assembly for sequence-independent construction of long-length DNA. Nucleic Acids Res, 2010, 38(8): 2594-2602. DOI:10.1093/nar/gkq123 |
| [25] |
Au LC, Yang FY, Yang WJ, et al. Gene synthesis by a LCR-based approach: High-level production of leptin-L54 using synthetic gene in Escherichia coli. Biochem Biophy Res Coumm, 1998, 248(1): 200-3. DOI:10.1006/bbrc.1998.8929 |
| [26] |
Gibson DG, Young L, Chuang RY, et al. Enzymatic assembly of DNA molecules up to several hundred kilobases. Nat Methods, 2009, 6(5): 343-345. DOI:10.1038/nmeth.1318 |
| [27] |
Gibson DG, Smith HO, Hutchison Ⅲ CA, et al. Chemical synthesis of the mouse mitochondrial genome. Nat Methods, 2010, 7(11): 901-903. DOI:10.1038/nmeth.1515 |
| [28] |
Zhao J, Wang X, Li BZ, et al. DNA assembly technology in synthetic biology. Life Science, 2013, 25(10): 983-992 (in Chinese). 赵鹃, 王霞, 李炳志, 等. 合成生物学中的DNA组装技术. 生命科学, 2013, 25(10): 983-992. |
| [29] |
Li MZ, Elledge SJ. Harnessing homologous recombination in vitro to generate recombinant DNA via SLIC. Nature Methods, 2007, 4(3): 251-256. DOI:10.1038/nmeth1010 |
| [30] |
Zhang YW, Werling U, Edelmann W. SLiCE: a novel bacterial cell extract-based DNA cloning method. Nucleic Acids Res, 2012, 40(8): e55. DOI:10.1093/nar/gkr1288 |
| [31] |
Tillett D, Neilan BA. Enzyme-free cloning: a rapid method to clone PCR products independent of vector restriction enzyme sites. Nucleic Acids Res, 1999, 27(19): e26-e28. DOI:10.1093/nar/27.19.e26 |
| [32] |
Liang J, Liu ZH, Low XZ, et al. Twin-primer non-enzymatic DNA assembly: an efficient and accurate multi-part DNA assembly method. Nucleic Acids Res, 2017, 45(11): e94. DOI:10.1093/nar/gkx132 |
| [33] |
Lu JN, Luo ZQ, Jiang SY, et al. DNA synthesis, assembly and transfer technology. Chin Acad Sci, 2018, 33(11): 1174-1183 (in Chinese). 卢俊南, 罗周卿, 姜双英, 等. DNA的合成、组装及转移技术. 中国科学院院刊, 2018, 33(11): 1174-1183. |
| [34] |
Gibson DG, Benders GA, Andrews-Pfannkoch C, et al. Complete chemical synthesis, assembly, and cloning of a Mycoplasma genitalium genome. Science, 2008, 319(5867): 1215-1220. DOI:10.1126/science.1151721 |
| [35] |
Gibson DG, Glass JI, Lartigue C, et al. Creation of a bacterial cell controlled by a chemically synthesized genome. Science, 2010, 329(5987): 52-56. DOI:10.1126/science.1190719 |
| [36] |
Shao ZY, Zhao HM. DNA assembler: a synthetic biology tool for characterizing and engineering natural product gene clusters. Methods Enzymol, 2011, 517: 203-224. |
| [37] |
Mercy G, Mozziconacci J, Scolari VF, et al. 3D organization of synthetic and scrambled chromosomes. Science, 2017, 355(6329): eaaf4597. DOI:10.1126/science.aaf4597 |
| [38] |
Xie ZX, Li BZ, Mitchell LA, et al. "Perfect" designer chromosome V and behavior of a ring derivative. Science, 2017, 355(6329): eaaf4704. DOI:10.1126/science.aaf4704 |
| [39] |
Wu Y, Li BZ, Zhao M, et al. Bug mapping and fitness testing of chemically synthesized chromosome X. Science, 2017, 355(6329): eaaf4706. DOI:10.1126/science.aaf4706 |
| [40] |
Shen Y, Wang Y, Chen T, et al. Deep functional analysis of synⅡ, a 770-kilobase synthetic yeast chromosome. Science, 2017, 355(6329): eaaf4791. DOI:10.1126/science.aaf4791 |
| [41] |
Mitchell LA, Wang A, Stracquadanio G, et al. Synthesis, debugging, and effects of synthetic chromosome consolidation: synVI and beyond. Science, 2017, 355(6329): eaaf4831. DOI:10.1126/science.aaf4831 |
| [42] |
Zhang WM, Zhao GH, Luo ZQ, et al. Engineering the ribosomal DNA in a megabase synthetic chromosome. Science, 2017, 355(6329): eaaf3981. DOI:10.1126/science.aaf3981 |
| [43] |
Richardson SM, Mitchell LA, Stracquadanio G, et al. Design of a synthetic yeast genome. Science, 2017, 355(6329): 1040-1044. DOI:10.1126/science.aaf4557 |
| [44] |
Zhou JT, Wu RH, Xue XL, et al. CasHRA (Cas9-facilitated Homologous Recombination Assembly) method of constructing megabase-sized DNA. Nucleic Acids Res, 2016, 44(14): e124. DOI:10.1093/nar/gkw475 |
| [45] |
Itaya M, Tsuge K, Koizumi M, et al. Combining two genomes in one cell: stable cloning of the Synechocystis PCC6803 genome in the Bacillus subtilis 168 genome. Proc Natl Acad Sci USA, 2005, 102(44): 15971-15976. DOI:10.1073/pnas.0503868102 |
| [46] |
Itaya M, Fujita K, Kuroki A, et al. Bottom-up genome assembly using the Bacillus subtilis genome vector. Nat Methods, 2008, 5(1): 41-43. DOI:10.1038/nmeth1143 |
| [47] |
Guo F, Gopaul DN, Van Duyne GD. Structure of Cre recombinase complexed with DNA in a site-specific recombination synapse. Nature, 1997, 389(6646): 40-46. DOI:10.1038/37925 |
| [48] |
Yang DS, Zhang Y, Zhang JH, et al. Cre/Loxp recombinase system and transgenic. Anhui Agr Sci, 2010, 38(8): 3916-3918 (in Chinese). 杨东生, 张研, 张建会, 等. Cre/Loxp重组酶系统与转基因. 安徽农业科学, 2010, 38(8): 3916-3918. DOI:10.3969/j.issn.0517-6611.2010.08.027 |
| [49] |
Marsischky G, Labaer J. Many paths to many clones: a comparative look at high-throughput cloning methods. Genome Res, 2004, 14(10B): 2020-2028. DOI:10.1101/gr.2528804 |
| [50] |
Parks RJ, Cummings DT, Evelegh CM, et al. A high-efficiency Cre/loxP-based system for construction of adenoviral vectors. Human Gene Therapy, 1999, 10(16): 2667. DOI:10.1089/10430349950016708 |
| [51] |
Zou YR, Müller W, Gu H, et al. Cre-loxP-mediated gene replacement: a mouse strain producing humanized antibodies. Curr Biol, 1994, 4(12): 1099-1103. DOI:10.1016/S0960-9822(00)00248-7 |
| [52] |
Lewandoski M, Martin GR. Cre-mediated chromosome loss in mice. Nat Genetics, 1997, 17(2): 223-225. DOI:10.1038/ng1097-223 |
 2019, Vol. 35
2019, Vol. 35