1. 中国农业科学院兰州兽医研究所 家畜疫病病原生物学国家重点实验室 国家口蹄疫参考实验室,甘肃 兰州 730046;
2. 甘肃农业大学 动物医学院,甘肃 兰州 730070
收稿日期:2020-03-20;接收日期:2020-07-30;网络出版时间:2020-08-12
基金项目:国家重点研发计划项目(No. 2016YFD0501500),宁夏回族自治区重点研发计划(No. 2019BBF02005)资助
Development of a sandwich ELISA for detecting 3AB non-structural protein of foot-and-mouth disease virus
1. State Key Laboratory of Veterinary Etiological Biology, Lanzhou Veterinary Research Institute, Chinese Academy of Agricultural Sciences (CAAS), Lanzhou 730046, Gansu, China;
2. College of Veterinary Sciences, Gansu Agricultural University, Lanzhou 730070, Gansu, China
Received: March 20, 2020; Accepted: July 30, 2020; Published: August 12, 2020
Supported by: National Key Research and Development Program of China (No. 2016YFD0501500), Key Research and Development Program of Ningxia Province (No. 2019BBF02005)
*These authors contributed equally to this study.
口蹄疫(Foot-and-mouth disease,FMD)是由口蹄疫病毒(Foot-and-mouth disease virus,FMDV)引起的高度接触性传染病,主要易感动物为家养和野生的偶蹄动物[1-2]。该病传播迅速,可形成世界性大流行,对养殖业和国际畜产品贸易具有严重影响,是一种典型的“政治经济病”[3-4]。世界动物卫生组织(World Organization for Animal Health,OIE)将其列为必须报告的动物传染病,我国农业农村部也将其列为一类动物疫病。对于大多数发展中国家,接种FMD灭活疫苗是预防口蹄疫最为有效的手段,灭活疫苗的主要成分是FMDV结构蛋白,如果疫苗抗原的纯化工艺不过关,疫苗抗原中仍然会残留部分的非结构蛋白(NSP),多次免疫后会造成NSP抗体的阳转,影响通过检测NSP抗体区分免疫动物与自然感染动物的准确性,不利于免疫背景下感染状况的评价[5-6],影响口蹄疫免疫无疫区的国际认证,因此,口蹄疫疫苗抗原纯净度检验也就成为疫苗质量评价的一个重要内容[7] (OIE,2018)。
世界动物卫生组织(OIE) FMD诊断检测指南中推荐的FMD疫苗抗原纯净度检验评价方法是采用疫苗2次免疫至少8头牛后(OIE,2018),检测NSP是否阳转,以此评价灭活疫苗免疫是否会对感染状况的检测评估产生干扰。该检验方法免疫动物时间长,并且耗费大量人力与物力,因此,疫苗生产企业希望有更简单、有效的标准化检测方法来代替动物免疫实验。Capozzo等[8]开发了一种化学发光免疫分析法,可以在生产过程中定量口蹄疫疫苗抗原中的非结构蛋白,进行疫苗质量控制;李永亮等[9]利用口蹄疫病毒非结构蛋白3B单克隆抗体,建立了一种定量检测病毒培养液中3B蛋白的液相阻断ELISA方法,但是在检测的灵敏度方面仍存在一些问题。双抗体夹心ELISA方法是一种简便、灵敏、特异的检测方法,已广泛应用于多种疫苗的质量控制[10-13]。本研究利用实验室制备的FMDV NSP 3A单克隆抗体和辣根过氧化物酶(HRP)标记的3B单克隆抗体,建立了一种定量检测FMD疫苗抗原中NSP 3AB含量的双抗体夹心ELISA方法,以期为疫苗抗原纯净度检验提供一个可供参考的检测评价方法。
1 材料与方法
1.1 抗体、抗原与疫苗
1.1.1 抗体和质粒 FMDV非结构蛋白3A单克隆抗体[14] (浓度为3 mg/mL)、HRP标记的3B单克隆抗体[15]和塞内卡病毒非结构蛋白3AB由本实验室制备并保存;重组质粒pET30a-3AB[16]由本实验室构建并保存。
1.1.2 主要试剂 大肠杆菌E. coli BL21(DE3)pLysE为博大泰克公司产品,His标签蛋白纯化凝胶购自南京金斯瑞生物科技有限公司,蛋白定量试剂盒(Bradford)购自北京全式金生物技术有限公司。
1.1.3 FMDV全病毒灭活抗原 未纯化的O/Mya98、O/CHA/99、O/HN/93、O/India/2001、A/SEA/97 FMDV灭活抗原,为本实验室制备,并经过灭活检验;来自疫苗生产企业的O/Mya/98、A/WH/09纯化后灭活抗原,Asia1/JS/05 FMDV灭活抗原为2016年生产保存的诊断用抗原。
1.1.4 成品灭活疫苗 来自不同口蹄疫灭活疫苗企业的疫苗成品详见表 1。
表 1 不同疫苗企业的口蹄疫灭活疫苗清单
Table 1 Inactivated FMD vaccines from different manufacturers
| No. |
Company |
Vaccines |
Batch No. |
| 1 |
A |
Bivalent inactivated vaccine against foot-and-mouth disease type O and A for pigs (Re-O/Mya98/JSCZ/2013 strain+Re-A/WH/09 strain) |
A181241J |
| 2 |
A181136J |
| 3 |
Bivalent inactivated vaccine against foot-and-mouth disease type O and A for pigs (O/Mya98/BY/2010 strain+Re-A/WH/09 strain) |
D181211J |
| 4 |
Inactivated vaccine against foot-and-mouth disease type O (OJMS strain) |
F190101J |
| 5 |
B |
Bivalent inactivated vaccine against foot-and-mouth disease type O and A (O/HB/HK/99 strain+AF/72 strain, suspension culture) |
1811004 |
| 6 |
1901003 |
| 7 |
Inactivated vaccine against foot-and-mouth disease type O in pigs (O/Mya98/XJ/2010 strain+O/GX/09-7strain) |
1811002 |
| 8 |
1906001 |
| 9 |
1907001 |
| 10 |
Inactivated vaccine against foot-and-mouth disease type O (OS strain) |
1807001 |
| 11 |
1810001 |
| 12 |
1907002 |
| 13 |
1906002 |
| 14 |
1907005 |
| 15 |
1907001 |
| 16 |
C |
Inactivated vaccine against foot-and-mouth disease type O for pigs (O/Mya98/XJ/2010 strain+O/GX/09-7 strain) |
20180318 |
| 17 |
20180317 |
| 18 |
Bivalent inactivated vaccine against foot-and-mouth disease type O and A (OHM/02 strain+AKT-Ⅲ strain, suspension culture) |
20180516 |
| 19 |
20180517 |
| 20 |
D |
Inactivated vaccine against foot-and-mouth disease type O for pigs (O/Mya98/XJ/2010 strain+O/GX/09-7 strain) |
JH180110 |
| 21 |
Bivalent inactivated vaccine against foot-and-mouth disease type O and A (OHM/02 strain+AKT-Ⅲ strain, suspension culture) |
JH180309 |
| 22 |
JH180310 |
| 23 |
JH190403 |
| 24 |
Trivalent inactivated vaccines for foot-and-mouth disease type O, A and Asia 1 (OHM/02 strain+AKT-Ⅲ strain+Asia1KZ/03 strain, suspension culture) |
JH170208 |
| 25 |
E |
Bivalent inactivated vaccine against foot-and-mouth disease type O and A for pigs (Re-O/Mya98/JSCZ/2013 strain+Re-A/WH/09 strain,suspension culture) |
18392254 |
| 26 |
18392080 |
| 27 |
Bivalent inactivated vaccine against foot-and-mouth disease type O and A (O/Mya98/BY/2010 strain+Re-A/WH/09 strain) |
18371420 |
| 28 |
Trivalent inactivated vaccines for foot-and-mouth disease type O, A and Asia 1 (O/Mya98/BY/2010 strain+Asia1/JSL/ZK/06 strain+Re-A/WH/09 strain) |
17351453 |
| 29 |
F |
Inactivated vaccine against foot-and-mouth disease type O (OHM/02 strain) |
2019015 |
| 30 |
Inactivated vaccine against foot-and-mouth disease type O and A (OHM/02 strain+AKT-Ⅲ strain, suspension culture) |
2019015 |
| 31 |
2019016 |
| 32 |
2019010 |
| 33 |
Inactivated vaccine against foot-and-mouth disease type O for pigs (O/Mya98/XJ/2010 strain+O/GX/09-7 strain, suspension culture) |
2019007 |
1.2 方法
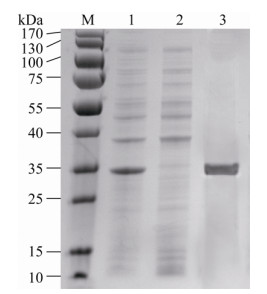
1.2.1 3AB融合蛋白的诱导表达与纯化 将重组质粒pET30a-3AB转化大肠杆菌BL21(DE3)pLysE,挑取单克隆接种于LB (含100 μg/mL卡那霉素)培养基中,37 ℃培养过夜,第2天以1/100的接种量接入新鲜的LB培养液(含100 μg/mL卡那霉素),培养至OD值约为0.6时,加入IPTG至终浓度1 mmol/L,28 ℃、200 r/min振荡培养5 h,最后离心收集菌体。用SDS-PAGE检测表达产物,同时以未诱导菌液作为对照;将表达产物用Invitrogen公司的Probond purification system kit纯化,纯化过程按照试剂盒说明书进行操作,用SDS-PAGE观察;同时用Easy protein quantitation kit (Bradford)进行蛋白定量,按照试剂盒说明书进行操作。
1.2.2 夹心ELISA反应条件的确定 用棋盘滴定法进行夹心ELISA抗体工作浓度的确定:用包被液(0.05 mol/L pH 9.6碳酸盐缓冲液)将3A单克隆抗体作3.0、1.0和0.6 μg/mL三个浓度稀释,横向加入酶标板各孔,100 μL/孔,4 ℃包被过夜;用含1%明胶的PBS溶液在37 ℃封闭1 h,用1×PBST连续洗板3遍,拍干;用1×PBS稀释标准3AB抗原至1.0 μg/mL,每孔加入100 μL,封板,室温振荡反应2 h,洗板,拍干;用1×PBST将HRP标记的3B单克隆抗体进行1︰50 000、1︰100 000、1︰200 000和1︰400 000稀释,纵向加入酶标板各孔,100 μL/孔,封板,室温振荡孵育1 h,洗板,拍干;加入TMB底物溶液避光反应15 min;0.3 mol/L H2SO4溶液终止反应,用酶标仪测定450 nm波长OD值。为了保证检测的敏感性,采用饱和浓度的3A单抗包被酶标板,以OD值变化较小时的3A单抗包被浓度为饱和包被浓度;以OD值达到2.0时的3B单抗最低浓度为其最适工作浓度。
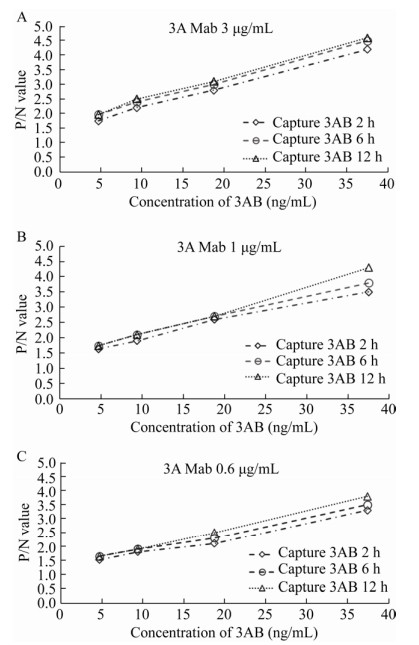
确定3A与3B单抗的最适工作浓度之后,确定捕获3AB蛋白的最适反应时间。将标准品按5、10、15、20、25、30、35、40 ng/mL稀释,室温分别捕获2、6、12 h;洗涤后,加入工作浓度的3B单抗,室温作用1 h;PBST洗涤后,同前加入底物显色并终止反应;以样品OD值与PBS对照的比值大于2.0,且3AB蛋白浓度最低时,所用的时间为最适3AB蛋白捕获反应时间。
1.2.3 夹心ELISA操作流程 包被:用包被缓冲液(0.05 mol/L碳酸盐缓冲液,pH 9.6)稀释3A单克隆抗体至工作浓度,100 μL/孔加入酶标板,封板,4 ℃过夜(12–18 h)。用1×PBST连续洗板3遍,拍干。
封闭:加封闭液(含1%明胶的PBS溶液) 100 μL/孔,37 ℃封闭1 h,用1×PBST连续洗板3遍,拍干。
加待测样品:用1×PBS稀释待测样品和对照样品,每孔加入100 μL,对照加两孔。封板,室温振荡反应6 h,用1×PBST洗板3遍,拍干。
加酶标二抗:用1×PBST稀释HRP标记的3B单克隆抗体至工作浓度,每孔加入100 μL,封板,室温振荡孵育1 h,用1×PBST连续洗板5遍,拍干。
加底物液显色:加入TMB底物溶液100 μL/孔,室温避光反应15 min。
终止反应测定OD值:每孔加入100 μL终止液(0.3 mol/L H2SO4溶液)终止反应,用酶标仪测定450 nm波长OD值。
结果判定:样本OD值与PBS对照孔OD值的比值大于2.0,确定为有3AB蛋白的界限值,然后根据标准曲线的回归方程,即可计算出样品中所含3AB蛋白的浓度。
1.2.4 标准曲线的绘制 用1×PBS (0.01 mol/L磷酸盐缓冲液,pH 7.4) 2倍系列稀释3AB蛋白标准品,浓度依次为600.0、300.0、150.0、75.0、37.5、18.8、9.4、4.7 ng/mL,采用上述夹心ELISA程序检测不同浓度3AB标准品的OD值,重复检测6次,通过计算每个浓度的平均值、标准差,并进行差异显著性分析(t检验),从而确定该方法的检测范围;再以不同浓度3AB蛋白标准品所对应的OD值作为横坐标、以标准品的不同浓度作为纵坐标建立标准曲线,利用Excel软件中的LINEST函数进行线性回归分析,推导回归方程。
1.2.5 3AB定量检测ELISA特异性评价 使用上述3AB定量ELISA方法检测1×PBS、BHK细胞培养液、胎牛血清(FBS)和塞内卡病毒非结构蛋白3AB等,评价该定量检测ELISA方法的特异性。
1.2.6 不同来源FMDV灭活抗原中3AB含量的检测 应用此方法分别检测纯化前后的不同血清型FMDV灭活抗原;检测来自6个FMD全病毒灭活疫苗生产企业的33个批次的口蹄疫全病毒灭活疫苗,先进行破乳处理,分别取疫苗和正戊醇按9:1混合,4 ℃静置2 h后8 000 r/min离心10 min,破乳后取水相用于3AB含量检测,对比分析不同厂家不同批次疫苗中3AB蛋白的残留量。
1.2.7 标准品与灭活疫苗抗原中3AB蛋白Western blotting免疫印迹检测 将200倍浓度的标准品(120 μg/mL)用PBS缓冲液2倍系列稀释后,取50 μL加等量上样缓冲液,煮沸约5 min,取10 μL/孔加入凝胶中,进行SDS-PAGE;然后将分离后的蛋白条带转印至硝酸纤维素膜(NC),将膜放入含10%脱脂奶粉的PBST缓冲液中室温封闭1 h;PBST洗3次后,加入工作浓度的HRP-3B单抗(0.5 μg/mL),室温孵育1 h;PBST洗涤5次,然后加入ECL化学发光底物显色,暗室中压X光片曝光,观察条带显色情况,以眼观有明显条带者判为阳性。
2 结果与分析
2.1 3AB融合蛋白的诱导表达与纯化 收集诱导表达后菌体进行SDS-PAGE,结果与未诱导的阴性对照相比有明显的融合蛋白表达带,分子质量约为33 kDa,与理论值相符(图 1);纯化后的融合蛋白经SDS-PAGE分析,只有1条约33 kDa的蛋白带(图 1),纯度为99%,蛋白定量测得浓度为1.5 mg/mL。
2.2 双抗夹心ELISA的最佳反应条件 用不同浓度3A单克隆抗体和HRP标记3B单克隆抗体进行棋盘滴定,以抗原孔OD值接近2.0、未加抗原孔OD值< 0.1为判定标准,结果显示,3A单克隆抗体的饱和包被浓度为3.0 μg/mL,此时对应的HRP标记3B单克隆抗体的最适工作浓度为1:100 000 (表 2)。
表 2 夹心ELISA抗体工作浓度棋盘滴定结果
Table 2 Chess-board titration of antibodies for sandwich ELISA
| HRP-3B Mab |
3A Mab (μg/mL) |
| 3.0 |
1.0 |
0.6 |
0.0 |
| 1:50 000 |
3.38 |
3.33 |
3.01 |
0.08 |
| 1:100 000 |
2.49 |
2.44 |
2.17 |
0.07 |
| 1:200 000 |
1.57 |
1.56 |
1.30 |
0.06 |
| 1:400 000 |
0.88 |
0.87 |
0.73 |
0.07 |
对比了3A单抗捕获3AB蛋白2、6与12 h的检测敏感性,以3AB蛋白的浓度作为横坐标、以不同浓度3AB蛋白测得OD值与阴性对照OD值的比值作为纵坐标绘制曲线,结果见图 2所示。以最低检测浓度对应的OD值与阴性对照OD值的比值≥2.0时,所对应的3AB标准品浓度为最低检测限,以此确定可达最低检测限的反应条件。由图 2可见,3A单抗的包被浓度为3.0 μg/mL,捕获3AB蛋白的时间为6 h时,标准品最低浓度对应的OD值与阴性对照OD值的比值为2.0,捕获6 h与12 h的结果没有明显差异,由此确定该ELISA方法的最佳反应条件为3.0 μg/mL 3A单克隆抗体包被酶标板,室温捕获6 h进行定量检测,确定为该夹心ELISA的最佳反应条件。在此条件下的3AB蛋白的最低检测限为4.7 ng/mL。
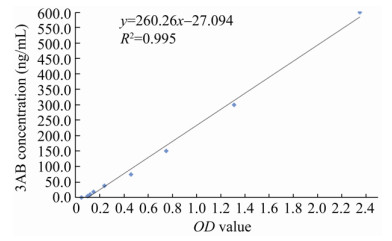
2.3 标准曲线与线性回归分析 采用双抗体夹心ELISA检测不同浓度的3AB蛋白标准品,6次重复检测结果见表 3。对每个浓度标准品的6次检测数据进行差异显著性检验显示,每组检测数据的标准差都在0.05以内,t检验的P值都大于0.05,说明6次检测数值之间差异不显著。根据6次重复检测值的平均值绘制标准曲线(图 3),推导出的回归方程为y=260.26x−27.094,相关系数R2值为0.995 7,根据标准品的检测值,确定3AB蛋白含量的检测范围为4.7–600.00 ng/mL。
表 3 不同浓度3AB蛋白标准品的检测OD值
Table 3 The OD value of different concentrations of 3AB standards
| 3AB standards (ng/mL) |
T1 |
T2 |
T3 |
T4 |
T5 |
T6 |
M |
SD |
P value |
| 600.0 |
2.51 |
2.18 |
2.25 |
2.32 |
2.38 |
2.47 |
2.35 |
0.10 |
P > 0.05 |
| 300.0 |
1.30 |
1.32 |
1.27 |
1.31 |
1.39 |
1.26 |
1.31 |
0.03 |
P > 0.05 |
| 150.0 |
0.76 |
0.81 |
0.78 |
0.70 |
0.67 |
0.79 |
0.75 |
0.04 |
P > 0.05 |
| 75.0 |
0.47 |
0.38 |
0.45 |
0.46 |
0.45 |
0.47 |
0.46 |
0.02 |
P > 0.05 |
| 37.5 |
0.25 |
0.20 |
0.21 |
0.26 |
0.22 |
0.23 |
0.24 |
0.03 |
P > 0.05 |
| 18.8 |
0.16 |
0.14 |
0.15 |
0.15 |
0.13 |
0.16 |
0.15 |
0.01 |
P > 0.05 |
| 9.4 |
0.12 |
0.11 |
0.12 |
0.13 |
0.12 |
0.11 |
0.12 |
0.01 |
P > 0.05 |
| 4.7 |
0.10 |
0.09 |
0.09 |
0.10 |
0.09 |
0.09 |
0.10 |
0.01 |
P > 0.05 |
| 0.0 |
0.05 |
0.04 |
0.05 |
0.06 |
0.05 |
0.05 |
0.05 |
0.01 |
P > 0.05 |
| Notes: T1–T6 shows OD value; M: mean; SD: standard deviation. |
2.4 夹心ELISA定量检测方法的特异性 夹心ELISA定量检测1×PBS缓冲液、BHK细胞培养液、含2%胎牛血清的细胞维持液和塞内卡病毒非结构蛋白3AB,重复检测10次以上其OD值均小于0.05,说明常规的病毒培养液对检测结果没有干扰,与塞内卡病毒的3AB蛋白没有交叉反应,证明该检测方法特异性好。
2.5 夹心ELISA定量检测方法的实际应用 夹心ELISA定量检测12份未纯化灭活FMDV抗原、2份纯化的灭活FMDV抗原,33份来自不同疫苗企业提供的口蹄疫灭活疫苗破乳后抗原,结果见表 4。12份未纯化灭活FMDV抗原中3AB蛋白量介于9.3–200.0 ng/mL之间;而纯化后的2份FMDV抗原中3AB蛋白含量低于最低检测限。检测33份灭活疫苗抗原中的3AB含量,其中有9份抗原中的3AB含量大于10 ng/mL (表 4,灭活疫苗编号为5–7,10–15),其他24份疫苗抗原中3AB蛋白含量低于4.7 ng/mL的最低检测限(表 4中省略)。
表 4 五次重复定量检测口蹄疫病毒灭活抗原与商品化疫苗中3AB蛋白含量结果
Table 4 Quantification of 3AB protein in inactivated antigens of different stains of FMDV and commercial FMD vaccines (ng/mL)
| Antigen |
Strain |
No. |
T1 |
T2 |
T3 |
T4 |
T5 |
M |
SD |
| Unpurified inactivated antigen |
O/Mya/98 |
171108 |
19.8 |
16.4 |
18.3 |
17.9 |
18.6 |
18.2 |
0.7 |
| 180524 |
9.6 |
8.7 |
10.9 |
8.6 |
9.3 |
9.4 |
0.6 |
| 180612 |
14.6 |
12.4 |
15.1 |
13.5 |
14.4 |
14.0 |
0.7 |
| 180720 |
15.8 |
18.6 |
17.4 |
16.2 |
17.9 |
17.2 |
0.8 |
| O/CHA/99 |
181229 |
15.9 |
14.1 |
13.9 |
15.3 |
14.8 |
14.8 |
0.5 |
| O/HN/93 |
181229 |
9.9 |
10.6 |
12.7 |
11.8 |
10.4 |
11.1 |
0.8 |
| O/India/2001 |
190218 |
15.4 |
13.1 |
14.6 |
15.5 |
16.2 |
15.0 |
0.7 |
| A/Sea/97 |
170330 |
74.7 |
70.1 |
72.6 |
69.8 |
71.4 |
71.7 |
1.3 |
| 180525 |
32.5 |
33.1 |
31.3 |
30.5 |
32.1 |
31.9 |
0.7 |
| 180623 |
53.0 |
50.7 |
51.9 |
51.0 |
52.4 |
51.8 |
0.6 |
| 190218 |
21.8 |
19.9 |
22.3 |
20.4 |
21.0 |
21.1 |
0.6 |
| Asia1/JS/05 |
161118 |
201 |
202.1 |
199.5 |
197.4 |
200 |
200.0 |
1.0 |
| Purified inactivated antigens |
O/Mya/98 |
181022 |
< 4.7 |
< 4.7 |
< 4.7 |
< 4.7 |
< 4.7 |
< 4.7 |
0.0 |
| A/WH/09 |
181022 |
< 4.7 |
< 4.7 |
< 4.7 |
< 4.7 |
< 4.7 |
< 4.7 |
0.0 |
| Antigens in commercial vaccines |
5 |
49.0 |
35.0 |
57.0 |
72.0 |
50.0 |
52.6 |
9.5 |
| 6 |
55.0 |
45.0 |
67.0 |
74.0 |
40.0 |
56.2 |
11.4 |
| 7 |
45.0 |
30.0 |
23.0 |
41.0 |
25.0 |
32.8 |
8.1 |
| 10 |
70.1 |
70.7 |
75.5 |
74.5 |
63.5 |
70.86 |
4.7 |
| 11 |
81.5 |
81.4 |
87.2 |
86.0 |
84.2 |
84.06 |
2.6 |
| 12 |
61.7 |
62.4 |
66.4 |
65.5 |
71.4 |
65.48 |
3.9 |
| 13 |
76.4 |
77.0 |
82.4 |
81.2 |
75.8 |
78.56 |
3.0 |
| 14 |
85.8 |
86.2 |
92.5 |
91.1 |
89.6 |
89.04 |
3.0 |
| 15 |
53.0 |
53.8 |
57.0 |
56.3 |
44.4 |
52.9 |
5.0 |
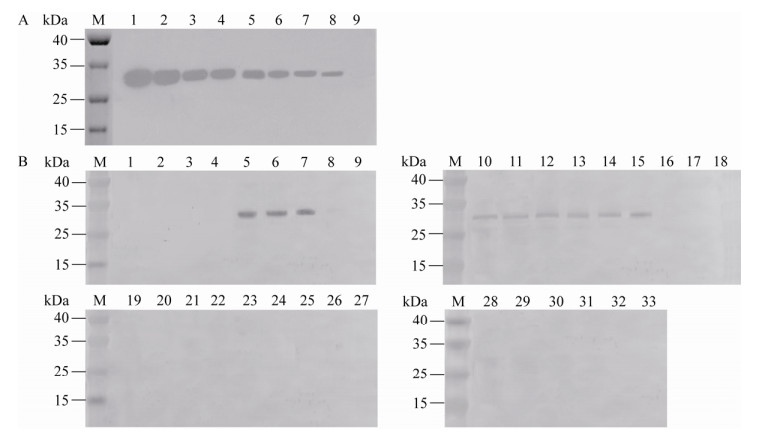
2.6 Western blotting免疫印迹检测 Western blotting结果显示,标准蛋白上样量依次为600.0、300.0、150.0、75.0、37.5、18.8、9.4和4.7 ng时均出现特异性条带,上样蛋白量为2.4 ng时未出现条带(图 4A);33份来自不同厂家的成品疫苗抗原中编号为5、6、7、10、11、12、13、14和15的9份疫苗出现了特异性条带(图 4B),说明有3AB蛋白残留,其余24份疫苗均未出现条带(图 4B)。
3 讨论 在灭活疫苗免疫背景下,口蹄疫感染状况的监测依赖于检测NSP抗体,因此,OIE口蹄疫诊断标准中明确要求,在申请认可口蹄疫免疫无疫区的国家或地区,必须使用对NSP抗体检测没有干扰的抗原纯化灭活疫苗,从而能够通过检测NSP抗体,准确评价区域内免疫动物群体FMD的感染情况。目前,评价灭活疫苗抗原纯净度的方法是通过两次动物免疫试验,以NSP抗体是否阳转来进行判定。已有许多实验室对FMDV NSP 3A、3B、3D、2C和3ABC等非结构蛋白抗体的应答规律进行了研究,并建立了对应的非结构蛋白抗体检测方法[17-21],其中检测NSP 3AB或3ABC抗体是鉴别感染与免疫动物的国际通用方法[22-26],所以检测疫苗抗原中3AB或3ABC蛋白的含量,可以直接反映疫苗抗原的纯化程度,指导疫苗的选择和使用,也可为疫苗的质量控制提供参考方法。
本研究通过优化ELISA反应条件,在3A单抗饱和浓度(3 μg/mL)包被酶标板,6 h捕获3AB蛋白,达到了最高的检测灵敏度,可检测标准品3AB蛋白的最低量为4.7 ng/mL,低于这一最低检测限时,则与空白对照没有差异。采用原核表达纯化的3AB蛋白为标准品,通过多次重复试验建立了相对稳定的标准曲线,样品浓度与OD值呈线性相关,多次重复检测标准曲线R值大于0.99;由于检测样品的成分主要为细胞培养抗原,成分相对稳定,检测特异性好,结果准确。应用本方法检测成品疫苗抗原中3AB蛋白的含量时,检出一些批次的疫苗抗原中残留有3AB蛋白,通过免疫印迹试验也检测出3AB蛋白条带,说明所建立的3AB蛋白定量ELISA方法检测结果准确可靠,但免疫印迹试验不能定量,只能定性判断这些批次的疫苗抗原纯化不完全。这种未完全去除NSP 3AB蛋白的疫苗多次使用会造成免疫动物3AB抗体的阳转,对感染与免疫动物的鉴别诊断产生干扰。至于3AB蛋白残留量与免疫次数和抗体阳转率之间的关系,还需要进一步研究。
本研究中也发现,不同毒株的未纯化灭活抗原中3AB含量存在较大的差异,这可能与病毒的复制滴度、前体蛋白的加工程度有关,Asia1型病毒的灭活抗原中检测到的3AB含量达200 ng/mL,在3个血清型抗原中最高,这可能与Asia1型病毒抗原产量高有关系。
本研究建立的定量检测3AB蛋白的ELISA方法,可以准确检测FMDV疫苗抗原中3AB蛋白的残留量,可以为疫苗抗原纯净度评价提供一定的参考,具有一定的应用价值。
致谢 感谢中农威特生物科技股份有限公司、中牧股份兰州生物药厂、天康生物股份有限公司制药一分公司、金宇保灵生物药品有限公司、内蒙古必威安泰生物科技有限公司、杨凌金海生物技术有限公司为本研究提供了口蹄疫病毒灭活疫苗,并提供了宝贵的建议,在此谢忱。
 2020, Vol. 36
2020, Vol. 36