
中国科学院微生物研究所、中国微生物学会主办
文章信息
- 陈冰清, 沈媚, 司伏生, 董世娟, 于瑞嵩, 谢春芳, 李震
- Chen Bingqing, Shen Mei, Si Fusheng, Dong ShiJuan, Yu RuiSong, Xie ChunFang, Li Zhen
- 猪流行性腹泻病毒ORF3蛋白40–91 aa是其细胞质定位的关键结构域
- The 40–91 aa sequence of porcine epidemic diarrhea virus ORF3 protein is the key structural domain controlling its location in cytoplasm
- 生物工程学报, 2020, 36(6): 1113-1125
- Chinese Journal of Biotechnology, 2020, 36(6): 1113-1125
- 10.13345/j.cjb.200074
-
文章历史
- Received: February 20, 2020
- Accepted: May 11, 2020
- Published: May 28, 2020
2. 上海种猪工程技术研究中心, 上海 201106;
3. 上海海洋大学 水产与生命学院, 上海 201106
2. Shanghai Engineering Research Center of Breeding Pig, Shanghai 201106, China;
3. College of Fisheries and Life Science, shanghai Ocean University, Shanghai 201306, China
猪流行性腹泻(Porcine epidemic diarrhea, PED)是由猪流行性腹泻病毒(Porcine epidemic diarrhea virus,PEDV)引起的一种高度传染性肠道疾病[1-2]。虽然不同年龄的猪均对PEDV易感,但PEDV对哺乳仔猪的危害最为严重,致死率可达90%以上。自20世纪70年代首次在英国和比利发现以来,亚洲和欧洲国家都报道了PED的流行。1980年后,PED一直是许多亚洲国家如中国、日本、韩国和泰国养猪业面临的严重问题[3]。自2010年以来,新变异株PEDV在猪群中再次暴发流行,给东南亚、北美等地区的养猪业造成了巨大的经济损失[4-10]。由于缺乏有效的疫苗,PED仍在世界范围内流行。
PEDV属于尼多病毒目(Nidovirales)、冠状病毒科(Coronaviridae)、α冠状病毒属[11]。PEDV基因组全长约28 kb,包含5′端非翻译区(5′UTR)、3′端非翻译区(3′ UTR)和分别编码纤突蛋白(S)、囊膜蛋白(E)、膜蛋白(M)、核衣壳蛋白(N)、多聚蛋白(1a/1ab)以及附属蛋白(ORF3)的7个开放阅读框(ORFs)。
ORF3蛋白是PEDV唯一的辅助蛋白。虽然ORF3蛋白是PEDV的体外复制非必需的,但是ORF3蛋白影响病毒的复制,与病毒毒力相关。Wang等[12]的研究表明ORF3具有离子通道活性,调节病毒的释放。Ye等[13]发现ORF3蛋白可以延长细胞S期、促进弱毒株PEDV的增殖。最近,Kaewborisuth等[14]发现ORF3蛋白可与S蛋白发生相互作用而影响病毒的复制。Zou等[15]发现ORF3通过上调GRP78蛋白表达和激活PERK-Eif2α信号通路触发内质网应激反应并诱导自噬,但不影响细胞凋亡。与此ORF3细胞表达结果不同,我们最近重组PEDV感染研究发现完整或自然截短的ORF3可以通过抑制PEDV诱导的细胞凋亡过程而促进病毒的复制[16]。上述研究也发现表达的ORF3蛋白位于细胞质中[13-17],融合表达的标签(如EGFP、Flag或Myc)和表达的细胞系(如Vero细胞、HeLa细胞、293 T细胞或PK15细胞)对ORF3蛋白在细胞质内定位没有影响[15]。然而,ORF3蛋白的细胞质定位信号未见报道。
为揭示PEDV ORF3细胞质定位信号,本研究构建了PEDV DR13野毒株(DR13wt) ORF3蛋白全长或系列ORF3蛋白截短肽的EGFP融合表达载体,利用激光共聚焦显微镜分析重组ORF3蛋白及其系列截短肽在细胞内的分布,研究结果将为进一步研究ORF3蛋白的细胞内转运及功能提供参考。
1 材料与方法 1.1 材料 1.1.1 菌种和质粒大肠杆菌Escherichia coli Top10购自天根生化科技(北京)有限公司;非洲绿猴肾细胞(Vero CCL-81)购自ATCC,插入PEDV DR13wt ORF3基因的重组pJET1.2-ORF3由本实验室构建[16];质粒pEGFP-C1购自华越洋生物(北京)科技有限公司。
1.1.2 主要试剂和仪器Prime STARTM HS DNA polymerase、DNA Marker购自大连宝生物有限公司;同源重组试剂盒购自南京诺唯赞生物科技有限公司;T4克隆试剂盒购自NEB公司;限制性内切酶BamH Ⅰ、Bgl Ⅱ购自Thermo Scientific公司;质粒提取试剂盒、DNA胶回收试剂盒购自Axygen公司;琼脂糖购自Sigma公司;脂质体Lipofectamine 2000购自Invitrogen公司;胎牛血清、DMEM培养液、Opti-MEM培养基购自Gibco公司;Hoechst 33342购自北京索莱宝公司。
PCR仪购自BIO-RAD公司;紫外凝胶成像仪购自上海天能科技有限公司;激光共聚焦显微镜购自Leica公司;CO2细胞培养箱购自Thermo公司。
1.1.3 ORF3蛋白及截短蛋白编码DNA扩增引物以PEDV DR13wt ORF3基因序列(GenBank登录号:AFE85963.1)为参考序列,设计扩增全长、截短ORF3基因的引物,送生工生物工程(上海)股份有限公司合成。
1.2 方法 1.2.1 ORF3基因的比对及跨膜区预测PEDV CV777野毒株ORF3 (CV777wt ORF3, GenBank登录号:AAK38657.1)和PEDV DR13野毒株ORF3(DR13wt ORF3, GenBank登录号:AFE85963.1)氨基酸序列比对采用Clustal X2。利用TMHMM 2.0在线预测ORF3蛋白的跨膜域(http://www.cbs.dtu.dk/services/TMHMM/)。
1.2.2 DR13wt ORF3及截短肽真核表达载体的构建利用设计的引物,以pJET1.2-ORF3为模板PCR扩增PEDV DR13wt orf3基因全长和系列截短肽编码DNA;PCR产物以1%琼脂糖凝胶电泳切胶纯化后通过同源重组连接至经BamH Ⅰ和Bgl Ⅱ双酶切的pEGFP-C1载体,构建ORF3及其截短肽的EGFP融合表达质粒。重组质粒经酶切和测序验证。得到的重组质粒见表 1。
| No | Plasmids name |
| 1 | pEGFP-ORF3 |
| 2 | pEGFP-ORF31–173 |
| 3 | pEGFP-ORF3174–225 |
| 4 | pEGFP-ORF31–91 |
| 5 | pEGFP-ORF392–173 |
| 6 | pEGFP-ORF31–39 |
| 7 | pEGFP-ORF340–91 |
| 8 | pEGFP-ORF3Δ40–91 |
| 9 | pEGFP-ORF340–63 |
| 10 | pEGFP-ORF364–74 |
| 11 | pEGFP-ORF375–91 |
| 12 | pEGFP-ORF340–74 |
| 13 | pEGFP-ORF364–91 |
| 14 | pEGFP-ORF340–63+5SG+75–91 |
| 15 | pEGFP-ORF340–91 (AA) |
| 16 | pEGFP-ORF340–91 (GG) |
| 17 | pEGFP-ORF340–91 (HH) |
| 18 | pEGFP-ORF340–91 (EE) |
将Vero细胞接种至预先放置细胞爬片的24孔板中,CO2培养箱中37 ℃培养;待细胞生长至75%的汇合度时,按照Lipofectamine 2000使用说明书配置Lipofectamine 2000与重组质粒混合液,室温下静置5 min;每孔加入50 μL混合液,轻摇混匀,继续培养16–18 h表达ORF3蛋白及其截短肽。
1.2.4 细胞固定和细胞核染色重组质粒转染后16–18 h弃培养液,以PBS漂洗3次,每次3 min;4%的多聚甲醛于37 ℃固定15 min;以PBS漂洗3次,每次3 min;Hoechst 33342室温染核15 min;以PBS漂洗3次,每次3 min;利用激光共聚焦显微镜观察融合蛋白表达及其细胞定位。
1.2.5 数据分析利用McMaster Biophotonics Facility ImageJ软件的Plot Profile插件进行细胞切面荧光强度分析;利用Colocalization Finder插件进行共定位定量分析,共定位比率采用皮尔逊相关系数分析[18-19]。利用SPSS Statistics 17.0进行统计分析,P < 0.05表示差异显著。
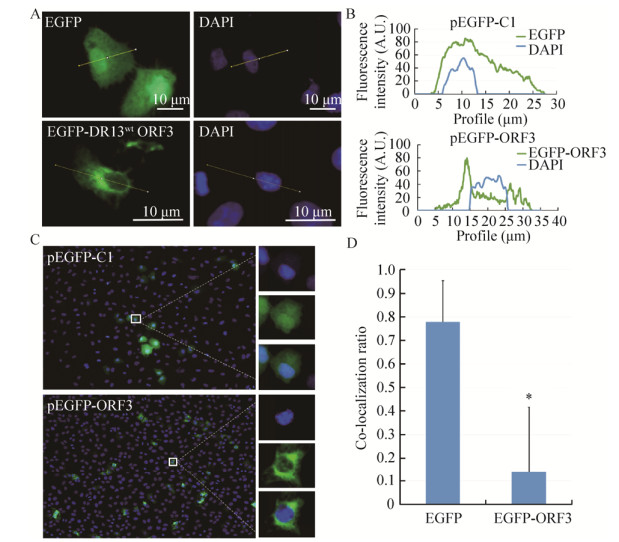
2 结果与分析 2.1 ORF3蛋白定位于细胞质中将PEDV DR13wt orf3基因克隆至pEGFP-C1,通过EGFP荧光观察ORF3蛋白在Vero细胞中定位。结果显示,与EGFP蛋白分布于整个细胞(细胞质和细胞核)中不同,EGFP-ORF3位于靠近细胞核的细胞质中(图 1A)。细胞切面荧光强度分析[18]也显示EGFP蛋白的荧光峰与核的荧光强度峰完全重叠,而融合蛋白EGFP-ORF3荧光信号几乎不与细胞核荧光信号重叠(图 1B)。为了进一步分析ORF3蛋白的细胞内定位情况,我们分析了同一视野范围内所有阳性细胞中EGFP蛋白和EGFP-DR13wt ORF3融合蛋白与细胞核共定位比率[18-19](图 1C),结果表明EGFP蛋白和融合蛋白EGFP-DR13wt ORF3的绿色荧光与细胞核(DAPI)的蓝色荧光共定位比率分别为0.75和0.1,两者差异显著(图 1D)。上述结果表明PEDV ORF3蛋白位于细胞质中。
|
| 图 1 EGFP-ORF3融合蛋白的细胞定位分析 Fig. 1 Localization of EGFP-ORF3. (A) Single-channel fluorescence image. (B) Fluorescence intensity analysis of the cell section in the figure A. (C) Multi-channel superimposed fluorescence images (200×). (D) Quantitative analysis of co-localization ratio of expressed proteins with nuclei in Figure C. The Pearson correlation coefficient is used for the co-localization ratio. * P < 0.05. |
| |
Wang等[12]预测PEDV CV777wt ORF3蛋白包含4个预测跨膜域(TM1 40–63 aa、TM2 75–91 aa、TM3 116–139 aa、TM4 150–173 aa)。PEDV DR13wt ORF3蛋白和CV777wt ORF3蛋白的氨基酸序列进行比对显示,两者氨基酸序列相似度为97.32%,有6个氨基酸不同(图 2)。TM1和TM3的氨基酸序列完全相同,在TM2、TM4分别有3个和1个氨基酸差异。

|
| 图 2 PEDV DR13wt和CV777wt ORF3蛋白氨基酸序列比较 Fig. 2 Amino acid sequence alignment of ORF3 proteins of PEDV DR13wt and CV777wt. The predicted transmembrane domains were shaded gray; differential amino acids were in the bold red. |
| |
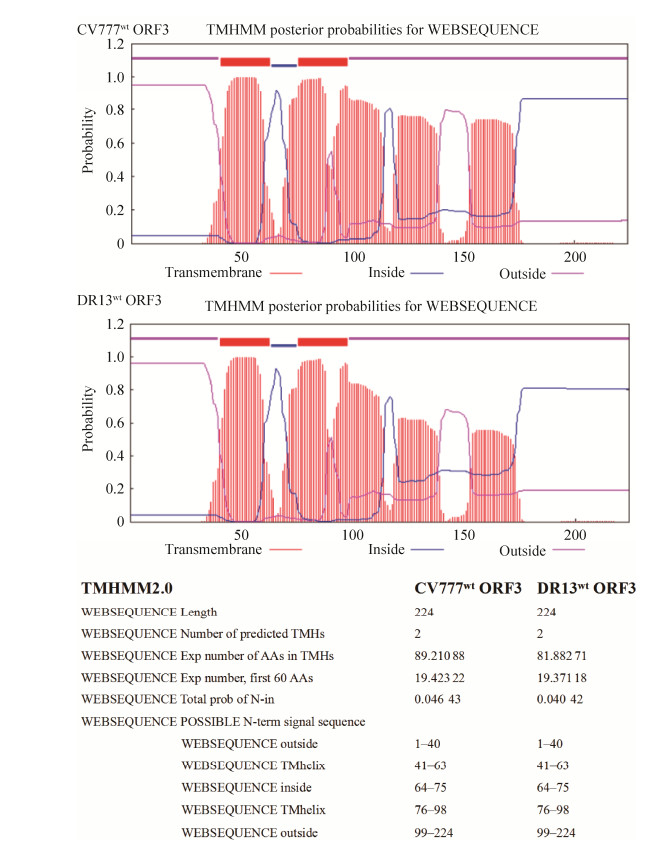
为了进一步了解DR13wt ORF3蛋白的结构,使用TMHMM 2.0分析预测软件预测DR13wt ORF3蛋白、CV777wt ORF3蛋白的跨膜域。如图 3所示,DR13wt ORF3蛋白与CV777wt ORF3蛋白预测的跨膜域完全一致,都仅有2个预测跨膜域TM1 41–63 aa和TM2 76–98 aa。
|
| 图 3 利用TMHMM2.0软件预测PEDV ORF3蛋白跨膜域 Fig. 3 Schematic representation of the predicted transmembrane topology with TMHMM Server version 2.0 of PEDV ORF3 protein. |
| |
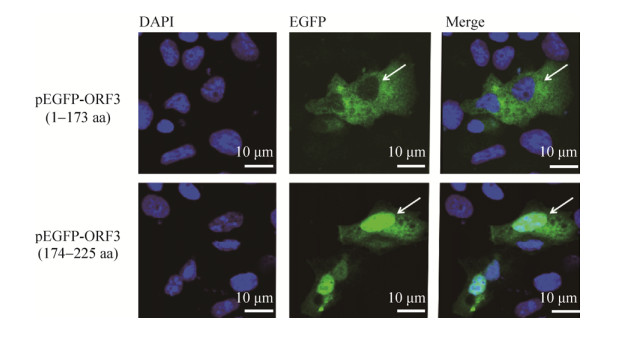
首先参照Wang等预测的4个跨膜域信息将DR13wt ORF3蛋白分成两段:包含4个跨膜域的ORF31–173和ORF3174–225。分别构建重组表达质粒pEGFP-ORF31–173和pEGFP-ORF3174–225,转染Vero细胞。激光共聚焦结果显示EGFP- ORF3174–225融合蛋白在细胞质和细胞核中均存在,而EGFP-ORF31–173仅存在于细胞质中(图 4),表明ORF31–173中存在影响ORF3定位于细胞质中的关键序列。
|
| 图 4 EGFP-ORF31–173和EGFP-ORF3174–225在Vero细胞中定位。 Fig. 4 Localization of EGFP-ORF31–173 and EGFP-ORF3174–225 in Vero cells. The arrows indicate the nuclei. |
| |
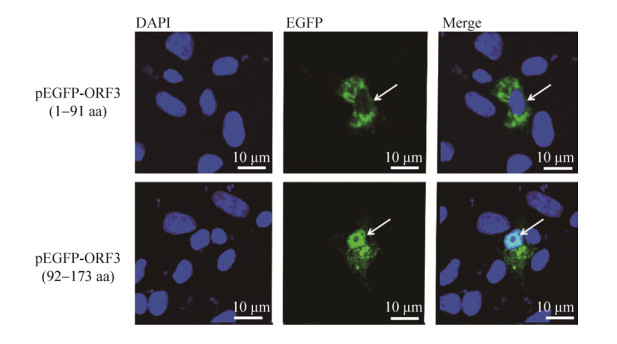
为了确定ORF3的细胞质定位信号,将ORF31–173分为两段:包含Wang等预测前两个跨膜域的ORF31–91和ORF392–173。结果显示,EGFP-ORF392–173融合蛋白存在于细胞质和细胞核中,而EGFP-ORF31–91融合蛋白仅存在于细胞质中(图 5),表明ORF31–91中存在ORF3细胞质定位信号。
|
| 图 5 EGFP-ORF31–91和EGFP-ORF392–173在Vero细胞中的定位 Fig. 5 Localization of EGFP-ORF31–91 and EGFP-ORF392–173 in Vero cells. The arrows indicate the nuclei. |
| |
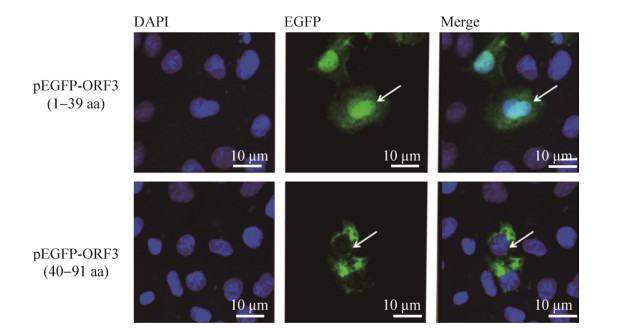
随后,将ORF31–91分为预测胞外区ORF31–39和包含了两个预测跨膜域的ORF340–91。构建相应的重组质粒,转染Vero细胞。结果显示EGFP-ORF31–39融合蛋白分布在细胞质和细胞核中,而EGFP-ORF340–91仅分布在细胞质中(图 6),说明ORF340-91中存在影响ORF3定位于细胞质的关键序列。
|
| 图 6 EGFP-ORF31–39和EGFP-ORF340–91在Vero细胞中的定位 Fig. 6 Localization of EGFP- ORF31–39 and EGFP-ORF340–91 in Vero cells. The arrows indicate the nuclei. |
| |
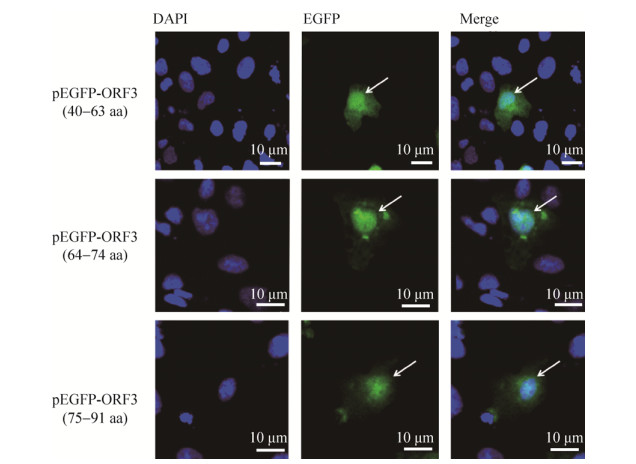
为了进一步确定影响ORF3蛋白定位的最小基序,分别将ORF3蛋白第一跨膜域ORF340–63、胞内区ORF364–74和第二跨膜域ORF375–91的编码DNA克隆至pEGFP-C1,并分别转染Vero细胞。激光共聚焦显微镜分析显示表达的融合蛋白EGFP-ORF340–63、EGFP-ORF364–74、EGFP- ORF375–91均位于细胞质和细胞核中(图 7),表明这3个多肽片段不能单独定位于细胞质中。
|
| 图 7 EGFP- ORF340–63、EGFP-ORF364–74和EGFP-ORF375–91在Vero细胞中定位 Fig. 7 Localization of EGFP-ORF340–63, EGFP-ORF364–74 and EGFP-ORF375–91 in Vero cells. The arrows indicate the nuclei. |
| |
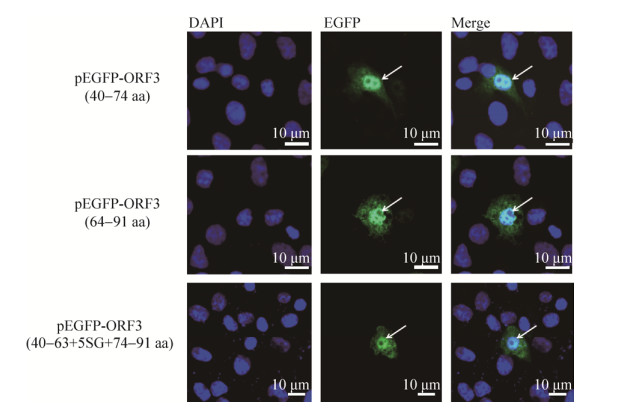
将ORF340–91包含的3个结构域分别两两组合,构建重组表达质粒pEGFP-ORF340–74、pEGFP-ORF364–91和pEGFP-ORF340–63+5SG+75–91,转染Vero细胞并观察他们的细胞内定位。在ORF3的2个跨膜域40–63 aa和75–91 aa中间插入5对Ser-Gly的linker片段(SGSGSGSGSG)替代其胞内区以有利于跨膜域的形成。激光共聚焦显微镜分析结果显示表达的EGFP-ORF340–74、EGFP-ORF364–91和EGFP-ORF340–63+5SG+75–91在细胞定位没有明显差异,均分布在细胞质和细胞核中(图 8),表明ORF340–91包含的3个结构域的两两组合也不能定位到细胞质中。
|
| 图 8 EGFP-ORF340–74、EGFP-ORF364–91和EGFP-ORF340–63+5SG+75–91在Vero细胞中的定位 Fig. 8 Localization of EGFP-ORF340–74, EGFP-ORF364–91 and EGFP-ORF340–63+5SG+75–91 in Vero cells. The arrows indicate the nuclei. |
| |
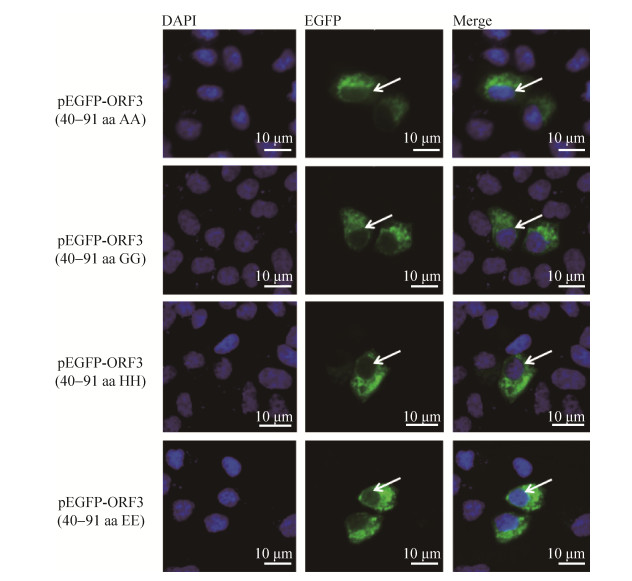
我们对ORF340–91序列分析比对发现其胞内区的存在66RR67双精氨酸结构。有研究证实双精氨酸结构是内质网定位信号[20-21],为了验证66RR67是否为ORF340–91的细胞质定位信号,将pEGFP-ORF340–91的双精氨酸密码子分别突变为非极性的丙氨酸(GCG) (中性)、极性的甘氨酸(GGC) (中性)、带正电荷的组氨酸(CAT) (碱性)和带负电荷的谷氨酸(GAG) (酸性)。结果显示突变前后的融合蛋白在细胞内的分布没有明显的差异(图 9),表明66RR67不是ORF340–91的细胞质定位信号。
|
| 图 9 EGFP-ORF340–91(AA)、EGFP-ORF340–91(GG)、EGFP-ORF340–91(HH)和EGFP-ORF340–91(EE)在Vero细胞中的定位 Fig. 9 Localization of EGFP-ORF340–91(AA), EGFP-ORF340–91(GG), EGFP-ORF340–91(HH)and EGFP-ORF340–91(EE) in Vero cells. The arrows indicate the nuclei. |
| |
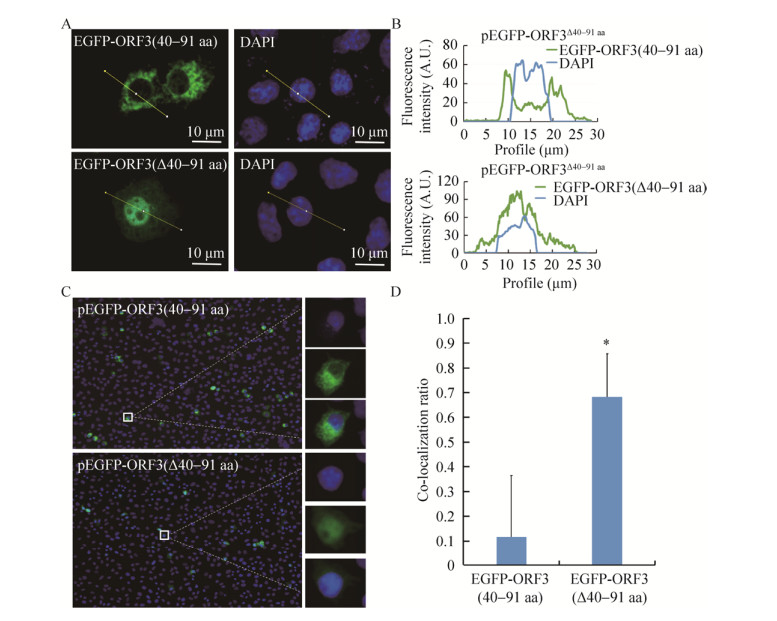
为进一步验证ORF340–91是PEDV ORF3细胞质定位的关键序列,我们构建敲除40–91 aa片段的EGFP-ORF3∆40–91表达载体pEGFP-ORF3∆40–91,并转染Vero细胞。激光共聚焦分析显示,与EGFP- ORF340–91仅定位于细胞质中不同,EGFP- ORF3∆40–91融合蛋白分布在细胞核和细胞质中(图 10A),与EGFP蛋白的细胞内分布相似(图 1A)。细胞切面荧光强度分析显示EGFP-ORF340–91融合蛋白的荧光强度峰集中在细胞质中(图 10B),与EGFP-ORF3的细胞定位相似(图 1B);而EGFP-ORF3∆40–91融合蛋白的荧光强度峰与细胞核的荧光强度峰几乎完全重叠(图 10B),表明其与细胞核共定位。对同一视野范围内所有阳性细胞中表达的融合蛋白与细胞核共定位比率统计分析显示EGFP-ORF340–91和EGFP-ORF3∆40–91的绿色荧光与细胞核(DAPI)的蓝色荧光共定位比率平均值分别为0.1和0.65,具有显著性差异(图 10C、10D)。综合上述结果,证实40–91aa序列是PEDV ORF3蛋白的细胞质定位结构域。
|
| 图 10 EGFP-ORF340–91和EGFP-ORF3∆40–91在Vero细胞中的定位 Fig. 10 Localization of EGFP-ORF340–91 and EGFP-ORF3∆40–91 in Vero cells. (A) Single-channel fluorescence image. (B) Fluorescence intensity analysis of the cell section in the figure A. (C) Multi-channel superimposed fluorescence images (200×). (D) Quantitative analysis of co-localization ratio of the expressed proteins with nuclei in Figure C. The Pearson correlation coefficient is used for the co-localization ratio. |
| |
由于缺乏有效的疫苗,PED依然是影响全球(特别是亚洲国家)生猪产业的重要疫病之一。与其他冠状病毒常编码多个辅助蛋白不同,PEDV仅编码一个辅助蛋白ORF3。研究表明ORF3蛋白与PEDV的毒力有关[22],ORF3蛋白可以通过多种方式影响PEDV的增殖[12, 16, 23]。虽然在不同细胞中表达的携带不同标签的ORF3蛋白均分布在细胞质中[13-15],然而对于ORF3的细胞质定位信号或关键氨基酸基序目前仍不清楚。为此,本研究采用可以自由进入细胞核的EGFP作为标记鉴定ORF3蛋白的细胞质定位标签,发现包含两个跨膜域的40–91 aa片段是ORF3蛋白定位于细胞质中的关键结构域。
Zou等[15]通过预测分析,发现PEDV CV777 ORF3蛋白是包含4个预测跨膜域的Ⅱ类跨膜蛋白,这与Wang等[12]之前的预测结果一致。我们使用TMHMM 2.0重新在线预测PEDV DR13wt和CV777wt ORF3蛋白跨膜域,结果显示二者具有相似的结构特性,均包含5段疏水区。与前期的预测结果不同的是,软件仅认为前2个输水区可形成2个跨膜域。造成预测结果与报道有差异的原因可能与我们采用的升级版TMHMM 2.0软件的算法中界定跨膜域的界限值提高有关。当然,DR13wt ORF3跨膜域的确定还有待于实验验证。本研究中鉴定到的PEDV ORF3的细胞质定位关键基序40–91 aa正好包含了预测的2个跨膜结构域及其中间的预测的胞内域,而且2个跨膜域中任何一个跨膜域的缺失都将使其细胞质定位能力,显示ORF3的细胞质定位需要2个跨膜域的同时存在。姜普等[21]报道跨膜结构域是一类很重要内质网定位信号。如Ryanonine受体的内质网定位需要其第1个跨膜结构域和第4个跨膜区同时起协同作用[20]。因此我们推测PEDV ORF3也通过2个跨膜域定位于内质网上而位于细胞质中。虽然我们选择以亲水性、低电荷效应的Gly-Ser组合5SG替换ORF340–91的胞内区,但替换后的EGFP-ORF375–91不再具有的细胞质定位能力,显示胞内区64–74 aa与2个跨膜域在ORF3的细胞质定位过程中协同发挥作用。当然我们也不能排除5SG替换通过影响1个或2个跨膜域的正确折叠而影响了EGFP-ORF375–91的细胞质定位。
PEDV ORF3蛋白的胞内区64–75 aa存在1个66RR67双精氨酸基序。Scott等[24]在对蛋白质的内质网定位信号研究中发现双精氨酸基序为部分蛋白的内质网定位信号。因此,本研究对EGFP-ORF340–91上的双精氨酸位点进行突变,发现非极性(丙氨酸)和极性(甘氨酸、组氨酸、谷氨酸)氨基酸的替换均对突变后的融合蛋白的细胞定位没有影响,说明66RR67双精氨酸不是影响ORF3蛋白细胞质定位的关键基序。
目前,关于PEDV ORF3蛋白的亚细胞定位还没有定论。有研究报道,ORF3蛋白在表达的初期分布在细胞质中,随着时间的延长逐渐在细胞质中聚集为点状[13, 15]。但也有报道ORF3蛋白在细胞质中弥散、均匀分布[14, 17]。本研究也发现EGFP-ORF3表达融合蛋白早期均匀分布在细胞质中,后期有聚集趋势。总之,本研究证实40–91 aa是ORF3蛋白定位于细胞质中的关键结构域。该研究结果将为ORF3细胞转运机制的揭示及其功能研究奠定重要的前期基础。
| [1] |
Fehr AR, Perlman S. Coronaviruses: an overview of their replication and pathogenesis//Maier HJ, Bickerton E, Britton P, Eds. Coronaviruses. New York: Humana Press, 2015.
|
| [2] |
Guo JH, Fang LR, Ye X, et al. Evolutionary and genotypic analyses of global porcine epidemic diarrhea virus strains. Transbound Emerg Dis, 2019, 66(1): 111-118. DOI:10.1111/tbed.12991 |
| [3] |
Song D, Park B. Porcine epidemic diarrhoea virus: a comprehensive review of molecular epidemiology, diagnosis, and vaccines. Virus Genes, 2012, 44(2): 167-175. DOI:10.1007/s11262-012-0713-1 |
| [4] |
Stevenson GW, Hoang H, Schwartz KJ, et al. Emergence of Porcine epidemic diarrhea virus in the United States: Clinical signs, lesions, and viral genomic sequences. J Vet Diagnost Invest, 2013, 25(5): 649-654. DOI:10.1177/1040638713501675 |
| [5] |
Wang LY, Byrum B, Zhang Y. Detection and genetic characterization of deltacoronavirus in pigs, Ohio, USA, 2014. Emerg Infect Dis, 2014, 20(7): 1227-1230. |
| [6] |
Sun RQ, Cai RJ, Chen YQ, et al. Outbreak of porcine epidemic diarrhea in suckling piglets, China. Emerg Infect Dis, 2012, 18(1): 161-163. DOI:10.3201/eid1801.111259 |
| [7] |
Pensaert MB, De Bouck P. A new coronavirus-like particle associated with diarrhea in swine. Arch Virol, 1978, 58(3): 243-247. DOI:10.1007/BF01317606 |
| [8] |
Temeeyasen G, Srijangwad A, Tripipat T, et al. Genetic diversity of ORF3 and spike genes of porcine epidemic diarrhea virus in Thailand. Infect Genet Evolut, 2014, 21: 205-213. DOI:10.1016/j.meegid.2013.11.001 |
| [9] |
Yang DK, Hyun KH, Heon LS, et al. Isolation and characterization of a new porcine epidemic diarrhea virus variant that occurred in Korea in 2014. J Vet Sci, 2018, 19(1): 71. DOI:10.4142/jvs.2018.19.1.71 |
| [10] |
Rahman SAE, Hoffmann M, Lueschow D, et al. Isolation and characterization of new variant strains of infectious bronchitis virus in northern Egypt. Adv Anim Vet Sci, 2015, 3(7): 362-371. DOI:10.14737/journal.aavs/2015/3.7.362.371 |
| [11] |
Debouck P, Pensaert M, Coussement W. The pathogenesis of an enteric infection in pigs, experimentally induced by the coronavirus-like agent, CV 777. Vet Microbiol, 1981, 6(2): 157-165. DOI:10.1016/0378-1135(81)90007-9 |
| [12] |
Wang K, Lu W, Chen JF, et al. PEDV ORF3 encodes an ion channel protein and regulates virus production. FEBS Lett, 2012, 586(4): 384-391. DOI:10.1016/j.febslet.2012.01.005 |
| [13] |
Ye SY, Li ZH, Chen FZ, et al. Porcine epidemic diarrhea virus ORF3 gene prolongs S-phase, facilitates formation of vesicles and promotes the proliferation of attenuated PEDV. Virus Genes, 2015, 51(3): 385-392. DOI:10.1007/s11262-015-1257-y |
| [14] |
Kaewborisuth C, He QG, Jongkaewwattana A. The accessory protein ORF3 contributes to porcine epidemic diarrhea virus replication by direct binding to the spike protein. Viruses, 2018, 10(8): 399. DOI:10.3390/v10080399 |
| [15] |
Zou DH, Xu JX, Duan XL, et al. Porcine epidemic diarrhea virus ORF3 protein causes endoplasmic reticulum stress to facilitate autophagy. Vet Microbiol, 2019, 235: 209-219. DOI:10.1016/j.vetmic.2019.07.005 |
| [16] |
Si FS, Hu XX, Wang CY, et al. Porcine epidemic diarrhea virus (PEDV) ORF3 enhances viral proliferation by inhibiting apoptosis of infected cells. Viruses, 2020, 12(2): 214. |
| [17] |
Wongthida P, Liwnaree B, Wanasen N, et al. The role of ORF3 accessory protein in replication of cell-adapted porcine epidemic diarrhea virus (PEDV). Arch Virol, 2017, 162(9): 2553-2563. DOI:10.1007/s00705-017-3390-5 |
| [18] |
Fuchsová B, Novák P, Kafková J, et al. Nuclear DNA helicase Ⅱ is recruited to IFN-α-activated transcription sites at PML nuclear bodies. J Cell Biol, 2002, 158(3): 463-473. DOI:10.1083/jcb.200202035 |
| [19] |
Dunn KW, Kamocka MM, Mcdonald JH. A practical guide to evaluating colocalization in biological microscopy. Am J Physiol-Cell Physiol, 2011, 300(4): C723-C742. DOI:10.1152/ajpcell.00462.2010 |
| [20] |
Bhat MB, Ma JJ. The transmembrane segment of ryanodine receptor contains an intracellular membrane retention signal for Ca2+ release channel. J Biol Chem, 2002, 277(10): 8597-8601. DOI:10.1074/jbc.M107609200 |
| [21] |
Jiang P, Sun W, Zhang YM, et al. Research progress in location signal of endoplasmic reticulum proteins. Lett Biotechnol, 2008, 19(6): 895-899 (in Chinese). 姜普, 孙薇, 张迎梅, 等. 内质网蛋白定位信号研究进展. 生物技术通讯, 2008, 19(6): 895-899. DOI:10.3969/j.issn.1009-0002.2008.06.031 |
| [22] |
Song DS, Yang JS, Oh JS, et al. Differentiation of a Vero cell adapted porcine epidemic diarrhea virus from Korean field strains by restriction fragment length polymorphism analysis of ORF3. Vaccine, 2003, 21(17/18): 1833-1842. |
| [23] |
Hu XX, Yu RS, Si FS, et al. ORF3 protein promotes the proliferation of porcine epidemic diarrhea virus on Vero cells. Microbiology China, 2018, 45(7): 1508-1517 (in Chinese). 胡晓霞, 于瑞嵩, 司伏生, 等. ORF3蛋白促进猪流行性腹泻病毒在Vero细胞上的增殖. 微生物学通报, 2018, 45(7): 1508-1517. |
| [24] |
Scott M, Lu G, Hallett M, et al. The Hera database and its use in the characterization of endoplasmic reticulum proteins. Bioinformatics, 2004, 20(6): 937-944. DOI:10.1093/bioinformatics/bth010 |
 2020, Vol. 36
2020, Vol. 36




