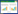中国科学院微生物研究所、中国微生物学会主办
文章信息
- 翟昊天, 祁庆生, 侯进
- Zhai Haotian, Qi Qingsheng, Hou Jin
- 体内连续进化技术的研究进展
- Recent advances of continuous in vivo evolution
- 生物工程学报, 2021, 37(2): 486-499
- Chinese Journal of Biotechnology, 2021, 37(2): 486-499
- 10.13345/j.cjb.200311
-
文章历史
- Received: June 1, 2020
- Accepted: August 12, 2020
- Published: August 31, 2020
随着生物技术的飞速发展,微生物已经越来越多的被用到生物技术、医药、食品、化工等领域[1]。除了进行理性的工程改造,非理性的遗传育种对于提高微生物的性能也至关重要。实验室进化是非理性育种的一种重要方式,已被广泛地应用于菌株遗传育种。但传统进化依赖基于筛选压力的自然突变,或者依赖化学或物理诱变建立突变体库进行高通量筛选,需要进行多轮突变和筛选,难以实现连续的突变进化。而体内连续进化技术不依赖外界人工干预,可以实现体内的连续突变和进化,大大加速了进化筛选过程。
连续进化技术最早可以追溯到20世纪60年代,1967年Spiegelman等在外界给予筛选压力的情况下,对Q噬菌体进行了74次连续传代,产生了一个基因组变异的个体,它比亲本的RNA基因组小83%,但复制速度快了15倍[2]。后续有许多研究人员对RNA连接酶以及RNA聚合酶的启动子进行了连续进化[3-5]。虽然这些方法仅在体外进行,但它们证明了连续进化的潜力,并为后续体内连续进化技术的发展奠定了基础。
达尔文进化包括复制、突变、翻译、筛选4个过程。体内连续进化技术同样包括以上4个过程,使突变能够自发地保留至下一代。体内连续进化常被定义为一种能够在生物体内自发地进行复制、突变、翻译,以最少的人工干预进化出特定表型的技术。
体内连续进化技术的发展,实现了微生物的体内突变,完美地把突变与筛选相结合,节约了时间且减少了人工干扰,能够快速地得到特定的表型。本文主要介绍近年来体内连续进化的各种技术,并从基因组范围内的进化和独立于基因组的进化两个方面介绍相关研究进展。
1 基因组范围的突变及进化基因组范围内的体内突变技术,可以构建基因组范围内的突变体库,通过对DNA复制、修复、重组等过程进行干预,使基因组随机突变的效率大大提高。高频率的基因组突变可以突破自然进化过程中突变率低、进化过程漫长的限制,与常见的化学诱变、物理诱变等突变技术相比,可实现基因组的连续突变和进化,大大加速了微生物的进化过程。
大肠杆菌Escherichia coli的基因组突变是研究较早的体内突变策略。Degnen等[6]在大肠杆菌中鉴定了一个导致基因组突变率提高的基因mutD5,正常情况下大肠杆菌的突变率为10–10每碱基[7],而mutD5能使大肠杆菌在丰富培养基中的突变率达到10-4–10–5每碱基[6, 8]。1986年Takano等[9]发现mutD5突变子来自于mutD (danQ) 上两个碱基的突变(73位的亮氨酸变为色氨酸,164位的丙氨酸变为缬氨酸)。danQ基因负责编码DNA聚合酶Ⅲ具有校正功能的3′核酸外切酶–ε亚基,是染色体保真复制的决定性因素,两个碱基的突变导致DNA聚合酶Ⅲ校正活性的丧失,从而提高了突变率。
利用丧失校正活性的DNA聚合酶可大大加速菌株的突变进程,但需要在菌株获得期望的表型后,使突变率回复到较低的水平。因此有研究利用温度敏感型质粒表达mutD5,使菌株的突变率暂时提高20–4 000倍。在筛选压力下,含有突变质粒的菌株快速进化,并获得新的表型。通过这种方法,研究人员可快速提高不同细菌对二甲基甲酰胺的耐受性[10]。待筛选得到期望的表型后,通过消除质粒,恢复菌株正常的低突变率,以稳定新的表型。
为了连续高效地进化出具有更优表型的产生物燃料的微生物菌株,Luan等构建了一种基因组复制工程辅助的连续进化系统(Genome replication engineering assisted continuous evolution,GREACE),此系统的核心是将突变和筛选相偶联[11]。GREACE的原理是通过引入DNA聚合酶Ⅲ的ε亚基编码基因dnaQ的突变体库,从而将体内连续突变机制引入微生物中,产生随机突变,以加速在筛选压力选择下的进化,将突变与筛选偶联在一起,达到连续定向进化的目的,值得注意的是dnaQ突变体的多样性将有助于产生具有不同突变类型偏好的细胞,从而确保子代细胞具有较高的基因组多样性。得到具有稳定基因型和表型的菌株后,通过去除修饰后的校对原件就能获得期望的突变体。
此系统成功地提高了大肠杆菌的卡那霉素抗性,并且使大肠杆菌在0.1%乙酸水平下的细胞生长速度提高了8倍。此外,还通过进化筛选获得了一株能在1.25%正丁醇浓度下生长的菌株,表明利用基因组复制工程辅助连续进化能够有效提高微生物对胁迫环境的耐受性。
DNA聚合酶关键位点的突变,是提高基因组突变率最直接的手段。除了mutD5,如大肠杆菌的dnaQ49[9, 12]、酿酒酵母的pol3-01[13-15],同样显著提高了基因组的突变率。除此之外,改造DNA的错配修复系统,也可以提高菌株的突变率。如枯草芽孢杆菌的高突变率菌株(mutS,mutM,mutY) 被用于热休克分子伴侣GroEL的突变[16];酿酒酵母错配修复基因PMS1的敲除,也会导致基因组突变率提高[17]。复制过程中校正及错配修复功能的丧失,会使基因组的突变率显著提高,加速进化的过程,但目前仅有少数研究对突变率进行了控制,如何实现突变率的严谨调控,使其在进化时突变率高,进化完成后突变维持在较低的水平,依然是我们需要解决的问题。
除了提高突变率外,在复制过程中向后随链中引入人工合成的具有同源臂的单链DNA,也可以实现基因组的多位点修饰。Murphy等将λ噬菌体的Red系统[18-19]的Exo (对双链DNA具有5′–3′外切酶活性)、Beta (退火互补ssDNA的单链DNA结合蛋白) 以及Gam蛋白(起辅助作用,抑制宿主RecBCD的核酸外切酶活性)[20],替换大肠杆菌的RecBCD,使线性DNA重组的效率显著提高[21]。在此基础上,2009年Wang等[22]利用只含有噬菌体Red系统的Beta蛋白的大肠杆菌实现了多重自动基因组工程(Multiplex automated genome engineering,MAGE)。MAGE通过在染色体复制过程中向后随链中引入大量的人工合成的具有同源臂的单链DNA,进行基因组的多位点修饰。它不仅可以同时针对基因组上的多个位置进行修饰,而且通过将含有寡聚核苷酸链的文库重复地引入细胞,产生了基因组修饰的多样性。利用此技术,研究人员对大肠杆菌的1-脱氧-D-木酮糖-5-磷酸合成途径的24个位置同时进行修饰,优化该途径合成重要的类异戊二烯番茄红素,在3 d之内筛选出了番茄红素产量增加5倍的菌株[22]。由于MAGE技术实现了自动化,研究人员认为这个进化过程是连续的。
MAGE技术提供了一种高效的多位点基因组修饰和文库构建的技术,利用MAGE技术在大肠杆菌中构建核糖体结合位点(Ribosome binding site,RBS) 文库进行体内进化,已有广泛的应用,而MAGE技术在真核生物中的设计和实现,对于在真核生物中建立有效的多位点基因组修饰方法,加速真核生物的进化,也具有重要的意义。Barbieri等在酿酒酵母体内利用复制叉中后随链的合成过程构建了一个多重自动基因组技术(Eukaryotic MAGE,eMAGE)[23]。此技术通过过表达酵母同源重组蛋白,弱化错配修复机制,在染色体复制退火过程中,将人工合成的单链DNA寡核苷酸链结合到后随链上。该技术不需要DNA双链的断裂,就可实现染色体的多位点精确编辑或多位点多样化改造。一次转化即可实现将12个核苷酸链重组到基因组上,通过多次迭代转化,可快速实现基因组的多样性。由于酵母体内单链DNA寡核苷酸链的同源重组效率较低,所以研究人员通过增加同源重组相关蛋白的表达,降低错配修复来增强单链DNA寡核苷酸链的重组。研究人员利用此技术优化酿酒酵母异源β-胡萝卜素的合成途径,通过设计单链DNA寡核苷酸链文库,精确靶向异源β-胡萝卜素合成途径中重要基因的启动子、开放阅读框和终止子,经过eMAGE循环快速地获得了具有不同β-胡萝卜素产量的菌落。
最近,随着人工合成酵母基因组计划的推进,一种全新的酵母体内快速进化的方式应运而生。酿酒酵母基因组的人工再设计与全合成被称为第二代酿酒酵母基因组计划(Saccharomyces cerevisiae 2.0,Sc2.0),通过对酿酒酵母基因的重新设计,人工合成了基因组高度修饰的、有活性的酵母菌株。人工设计合成的酵母基因组,在保持野生型基因顺序的同时,把终止密码子全部替换为TAA,删除了内含子、端粒序列、重复序列以及转座子,并把tRNA设计到一条染色体上,同时安插了许多对LoxP重组位点[21, 24]。
研究人员利用人工合成的酿酒酵母染色体,进行基因组的快速重排和进化。由于在人工合成的酵母基因组上在所有非必需基因的3′非翻译区引入了对称的LoxP重组位点,而在Cre重组酶的作用下,两个LoxP位点会发生位点特异性重组[25]。因此只要在含有人工合成的酵母基因组的菌株中表达Cre重组酶,就能实现LoxP位点介导的合成染色体重排以及修饰的进化(Synthetic chromosome rearrangement and modification by LoxP-mediated evolution,SCRaMbLE)。比如,Jia等利用此技术优化了木糖的利用途径,并使单倍体菌株类胡萝卜素的产量增加到1.5倍。基于二倍体菌株的多重SCRaMbLE迭代循环(MuSIC) 的策略,可通过5个SCRaMbLE迭代循环将类胡萝卜素的产量提高至38.8倍[26],Luo等通过SCRaMbLE技术进化了耐热、耐乙酸和乙醇的酵母菌株[27]。Blount等通过此技术提高菌株合成紫色杆菌素和青霉素的合成能力,并且也优化了木糖的利用[28]。此外,Shen等还发现杂合二倍体菌株(以野生型单倍体菌株和半合成单倍体Sc.2.0菌株作为亲本进行交配的二倍体菌株)比Sc.2.0合成染色体的单倍体菌株对SCRaMbLE造成的影响更具有耐受性,且SCRaMbLE也可以用于种间杂合二倍体的进化[29]。
外源途径优化和底盘细胞的优化是异源途径高效表达及产品高产的两个关键,但二者的优化都是相当繁琐且费时费力的。研究人员基于上述的重组组合方法(SCRaMbLE-in),使这两种方法同时进行[30]。在SCRaMbLE-in中,研究人员设计了一个体外重组酶工具包。首先选择一个感兴趣的调控途径,在这条途径上除了目的基因外的所有基因都含有调控元件,例如,启动子,但是在目的基因的上游有单个重组酶识别位点。之后,设计一系列启动子,且其两侧有方向相同的重组酶识别位点。在重组酶存在的情况下,可以将调控因子整合到目标重组位点,以生成一个组合的途径库。之后设计一个含有靶途径的载体,靶途径两端含有重组酶识别位点,通过SCRaMbLE技术,可以将靶途径整合到染色体的任何LoxP位点上,同时Cre酶还将通过删除、易位以及插入介导合成基因组的重排,使宿主遗传背景多样化。研究人员利用SCRaMbLE-in的方法重组了β-胡萝卜素合成途径,使合成量提高了1倍。
我们将上述技术的原理、应用及特点进行了归纳(表 1),这些策略都是针对基因组进行突变的,利用这种突变技术结合基于生长的筛选,可实现连续突变和生长优势菌的自动富集,实现连续的突变和筛选。利用此类技术提高微生物对环境的耐受性,对特定毒性物质的抗性,或者对特定碳源的利用能力等,具有明显的优势。此外,结合颜色或荧光等高通量筛选技术,也可以实现针对特定产物产量的快速进化筛选。
| Strategies | Principles | Microorganisms | Application examples | Limitations | References |
| mutD5 | Increasing the mutation rate during DNA replication through the mutation of DNA polymerases | Escherichia coli | Increasing the tolerance of strains to dimethylformamide | The mutation rate needs to be tightly controlled | [10] |
| GREACE | E. coli | Improving n-butanol tolerance | [11] | ||
| dnaQ49 | E. coli | Acquired strain with high level resistance to ampicillin, streptomycin and ofloxacin | [12] | ||
| pol3-01 | Saccharomyces erevisiae | Isolating thermotolerant mutants | [13–15] | ||
| mutS, mutM, mutY | Increasing the mutation rate through modifying the mismatch repair | Bacillus subtilis | Isolating thermo-adaptants from the groEL substituted strain | [16] | |
| MAGE | Annealing synthetic oligonucleotides in the lagging strand during DNA replication | E. coli | Evolved thermotolerant mutants | The technology can only be used in very few model organisms | [22] |
| eMAGE | S. erevisiae | Increasing the lycopene production | |||
| SCRaMbLE | Cre recombinase catalyzes recombination reaction between two loxP sites | S. erevisiae | Improving the β-carotene synthesis | The technology can only be used in S. erevisiae | [26–30] |
尽管针对基因组的突变进化对于提高微生物的环境耐受性等具有重要的意义,但是在很多情况下,我们只是把微生物作为一个细胞工厂,利用微生物本身繁殖速度快等特性达到快速合成重要蛋白或化合物的目的。这种情况下,我们只是需要特定的某个基因或者某几个基因能够快速突变进化,而不是基因组范围内的随机突变。目前,大部分针对特定靶基因的突变主要是通过易错PCR等技术实现,然后构建突变体库,进行筛选,再进行下一轮PCR,突变体库的构建,筛选等,如此反复进行,工作量大,且过程不能连续,而针对特定靶基因的体内连续进化技术的建立,可避免这些繁琐的工作,实现连续突变和筛选,加速进化的过程,且大大降低工作量。我们列举了一些经典进化的策略,并对其应用做了简单的介绍(表 2)。
| Strategies | Mechanisms | Microorganisms | Application examples | Limitations | References |
| PACE | Coupling the phage propagation with the activity of desired mutation | E. coli | Evolving T7 RNA Polymerase, cⅠ, Cas9, aminoacyl-tRNA synthetases, et al | The technology requires complicated experimental equipment and can only evolve the proteins which can affect the expression of pⅢ | [31–37] |
| PANCE | E. coli Bacillus methanolicus | Evolving pyrrolysyl- tRNA synthetase and methanol dehydrogenase | The technology only be used in prokaryotic organisms | [38–41] | |
| XL1-Red | Increasing the mutation rate during DNA replication through the modification of DNA polymerases and mismatch repair system | E. coli Lactobacillus Aeromonas punctata | Optimizing the activity of various enzymes such as esterase, arylmalonate decarboxylase, et al. | The system prefers to evolve large DNA fragmentsl | [42–48] |
| Error-prone DNA polymeraseⅠ | Increasing mutation by reducing DNA polymeraseⅠfidelity | E. coli | Generating TEM-1 β-lactamase mutants able to hydrolyze aztreonam | The technology can only be used in very few organisms | [49] |
| Orthogonal DNA replication system | Creating an orthogonal error-prone DNA replication system using P1 DNA Polymerase from Kluyveromyces lactis | S. erevisiae | Increasing DHFR tolerance of antimalarial drugs | Low expression of exogenous gene of interest | [50–53] |
| Ty1 | Generating mutation through the reverse transcription process | S. erevisiae | Evolution of transcription factors Spt15 and xylose metabolic pathway | Mutation rate is limited by transposition frequency | [54] |
Esvelt等[31]在大肠杆菌中构建了一套噬菌体辅助的连续进化系统(Phage-assisted continuous evolution,PACE)。这个系统利用M13噬菌体的连续培养和筛选使蛋白能够在大肠杆菌体内快速进化,该系统把侵染性噬菌体的产生和获得目的基因的突变偶联从而达到连续进化筛选的目的(图 1)。噬菌体的侵染需要gⅢ 基因编码的pⅢ蛋白的参与,只有表达了pⅢ蛋白的噬菌体,才能裂解大肠杆菌产生具有侵染性的子代噬菌体[32-34]。
|
| 图 1 噬菌体辅助的连续进化系统 Fig. 1 Overview of phage-assisted continuous evolution system. E. coli host cells with accessory plasmid (brown) that supplies gⅢ (gene Ⅲ, encoding pⅢ) and mutagenesis plasmid (red) continuously flow through a fixed-volume vessel where containing selection phage (SP, green). If SP encodes the desired protein variants of interest, infectious progeny phage will be produced, then continue to infect a new round of E. coli. With the constant inflow and outflow, only those phages that reproduce faster than the rate of dilution can exist and evolve in the vessel. |
| |
PACE中,噬菌体含有除gⅢ基因以外的所有基因,此外还含有需要进化的基因,这个噬菌体被命名为筛选噬菌体(Selection phage,SP)。在大肠杆菌中含有两个质粒,一个是附加质粒(Accessory plasmid,AP):携带有噬菌体的gⅢ基因并且由特定的启动子控制gⅢ基因的表达。此启动子只有和进化出的目的蛋白结合后,才能起始转录,因此只有待突变蛋白进化出了相应的特性,才能启动gⅢ 基因的表达;另一个质粒是突变质粒(Mutagenesis plasmid,MP):它通过降低大肠杆菌DNA聚合酶的校正功能来增加噬菌体复制过程中的突变率[35]。因此只有SP中的待进化基因发生想要的突变,才能与附加质粒上相应的启动子结合从而启动gⅢ 基因的表达,产生有活性的子代噬菌体,进行下一轮的侵染。最终具有优势突变的SP在不断的循环培养中得以积累,实现连续定向进化。
原则上,PACE可以在大肠杆菌中进化能够诱导pⅢ蛋白表达的所有蛋白。例如,被广泛应用的噬菌体T7 RNA聚合酶,它对启动子序列有高度的特异性,不能识别T3噬菌体相关的启动子,所以Esvelt等利用PACE系统对T7 RNA聚合酶进行定向进化,最终得到了能够识别T3相关启动子的T7 RNA聚合酶突变体。
PACE系统虽然能够较好连续定向的进化特定蛋白,但是pⅢ蛋白的本底表达会给最终的进化带来一些影响。因此,在此系统的基础上,Brodel等[36]对PACE系统进行了改进。此系统与PACE相似,研究人员用gⅥ 基因代替gⅢ 基因作为条件基因,pⅥ蛋白和pⅢ蛋白都能够使噬菌体产生入侵功能,但只有在pⅢ蛋白的存在下pⅥ蛋白才能稳定表达。此系统包含3部分:一个噬菌粒(Phagemid,PM):含有突变的cⅠ和gⅢ,并且相比于正常的噬菌体,较小的噬菌粒可以产生更多的基因突变;一个辅助噬菌体质粒(Helper phage plasmid,HP):携带除了gⅥ和gⅢ基因以外所有的噬菌体基因;一个副质粒:携带需要条件表达的gⅥ基因回路,此基因回路由合成的启动子控制。其工作原理和PACE相似,都是通过特定突变蛋白来激发条件基因的表达。将该系统用于cⅠ蛋白的突变,只有适合的突变cⅠ蛋白能启动gⅥ的表达从而产生有浸染功能的噬菌体,最终获得了多种cⅠ的突变体[37],并构建了第一套用于正交逻辑门的双重激活剂-阻抑物和阻遏物-阻遏物开关。
上述两种系统都是巧妙地利用噬菌体对大肠杆菌的侵染功能,构建了一个定向进化系统。但是它们仍然有一定的局限性,这两种系统并不是能够进化所有的蛋白,而是只能进化能够诱导pⅢ (pⅥ) 蛋白表达的蛋白,且所使用的实验设备较为复杂。
Suzuki等建立了一种新的实验室进化技术—非连续PACE技术(Phage-assisted non-continuous evolution,PANCE)[38]。PACE技术需要连续流动装置。而PANCE则是一种简化的技术,通过连续转接进行快速体内进化,降低了对实验仪器的依赖。利用PANCE技术,Wan等对可利用非天然氨基酸的Pyrrolysyl-tRNA合成酶进行了进化[39]。Roth等把PANCE与甲醛生物传感器相结合,对甲醇芽孢杆菌甲醇脱氢酶进行了进化[40-41]。噬菌体辅助的进化技术在针对特定蛋白的进化中发挥了巨大的作用,但这类技术只能用于可被噬菌体侵染的原核生物,具有一定的宿主局限性。
基于突变的DNA聚合酶的定向进化系统能够突破上述局限,使体内进化更具有普适性,这就要求能够实现独立于基因组的体内连续进化。独立于基因组的体内连续进化需要只对目的基因具有高的突变率,而不会对基因组产生影响,这对突变系统有非常严格的要求。
DNA聚合酶为DNA复制的关键酶,能够催化脱氧核苷酸插入到正在延伸的DNA链末端,并且对正在复制的DNA链进行校正,确保复制的保真性,使基因组的突变率维持在一个很低的水平,而DNA聚合酶校正功能的丧失会引起脱氧核苷酸错误插入,从而造成DNA复制过程中突变率提高。
利用上述原理Greener等[42-43]开发出了一个被命名为XL1-Red的大肠杆菌突变菌株。此菌株是携带DNA修复缺陷(mutT,mutS) 以及DNA聚合酶Ⅲ的ɛ-亚基缺陷(mutD) 的组合菌株,因此会在DNA复制过程中产生突变,突变率大约是野生型的5 000倍。把携带目标基因的质粒转入XL1-Red中,通过质粒的复制扩增,获得随机突变的质粒文库,之后分离质粒文库并将该文库转化到所需的菌株,以筛选突变表型。这种方法是比较简单的诱变策略,被广泛应用。例如,研究人员利用XL1-Red菌株进行酯酶的定向进化;提高芳基丙二酸脱羧酶、β-葡萄糖醛酸苷酶、聚羟基链烷酸酯(Polyhydroxyalkanoate,PHA) 合酶的活性[44-48]。然而该技术的突变率相对较低,倾向于进化较大的DNA片段,限制了其应用。
大肠杆菌中的DNA聚合酶Ⅰ主要负责后随链的合成、DNA修复以及ColEl质粒的复制。Camps等[49]利用易错的大肠杆菌DNA聚合酶Ⅰ构建了一个体内连续突变系统。该工作首先对DNA聚合酶Ⅰ的校正区域进行失活,并对聚合酶A基序的I709、B基序的T664和A661三个控制保真度的关键氨基酸突变,构建了一个高度易错的DNA聚合酶Ⅰ。在此基础上,构建了连续定向突变系统,该系统以JS200为宿主,向宿主体内转化两个质粒:一个是带有pSC101复制起始位点(不需要该DNA聚合酶介导复制) 的低拷贝质粒,含有编码易错的DNA聚合酶Ⅰ的基因,第二个是高拷贝的ColEl质粒,带有需要突变的目的基因,依靠易错的DNA聚合酶Ⅰ完成复制。利用β-内酰胺酶基因作为报告基因进行回复突变,测突变率,结果显示,易错DNA聚合酶Ⅰ对带有目的基因质粒的突变率达到8.1×10–4每碱基,并且相对宿主基因组,突变更倾向于质粒。作者利用该系统对TEM-1 β-内酰胺酶,进行连续突变进化,获得了对氨曲南(莫巴坦抗生素) 具有较高活性的内酰胺酶突变体。该工作利用易错的大肠杆菌DNA聚合酶Ⅰ成功构建了一个独立于基因组的体内连续定向突变系统,只需要将待突变的目的基因置于ColEl质粒上,就可以实现连续突变进化。
除了大肠杆菌,最近也有在真核模式生物中构建独立于基因组的进化系统的相关报道。Ravikumar等把来源于乳酸克鲁维酵母的线性质粒的复制系统转入酿酒酵母,构建了一个独立于基因组的体内连续进化系统。克鲁维酵母的pGKL1/2质粒(简称为P1/2) 是一套含有自身DNA复制元件的质粒对,它包括P1和P2两个线性多拷贝的DNA质粒,P2质粒上含有参与质粒对复制以及转录所需的所有蛋白的编辑基因,而P1上只含有自身复制所需的DNA聚合酶的编码基因。它们的复制发生在细胞质中,且该质粒对的复制机制与常见的DNA复制机制不同,其复制起始不是由RNA引物介导,而是通过蛋白质引发[50]。P1和P2的5′末端共价连接了末端蛋白(Terminal protein,TP),作为启动DNA扩增的复制起点。Ravikumar等把P1/P2转入酿酒酵母,由于质粒的复制机制与基因组复制机制不同,因此两套复制系统不会相互影响,从而实现了一个独立于基因组的体内连续进化系统[51]。作者通过CRISPR介导的同源重组的方式将待突变的基因插入到P1质粒上(图 2)。并突变P1的DNA聚合酶,提高质粒的突变率,通过优化聚合酶的突变,最终使目的基因的突变率达到10–5每碱基,而基因组的突变率则基本不受影响。在后续研究中,该课题组利用此系统,提高了二氢叶酸还原酶(Dihydrofolate reductase,DHFR)[52]对抗疟药物的耐受性[53]。

|
| 图 2 基于正交复制系统的独立于基因组的酿酒酵母体内连续定向进化技术 Fig. 2 Genome-independent continuous directed evolution in vivo in S. cerevisiae by an orthogonal DNA replication system. Schematic diagram of orthogonal replication system based on P1/2 plasmid pair of Kluyveromyces cerevisiae. The gene of interest (blue) is integrated into the P1 plasmid. The error-prone TP-DNAP1 gene (yellow) in the nucleus expresses the error-prone TP-DNAP1 under the expression system of the host cell, and then the replication of the P1 plasmid is initiated. |
| |
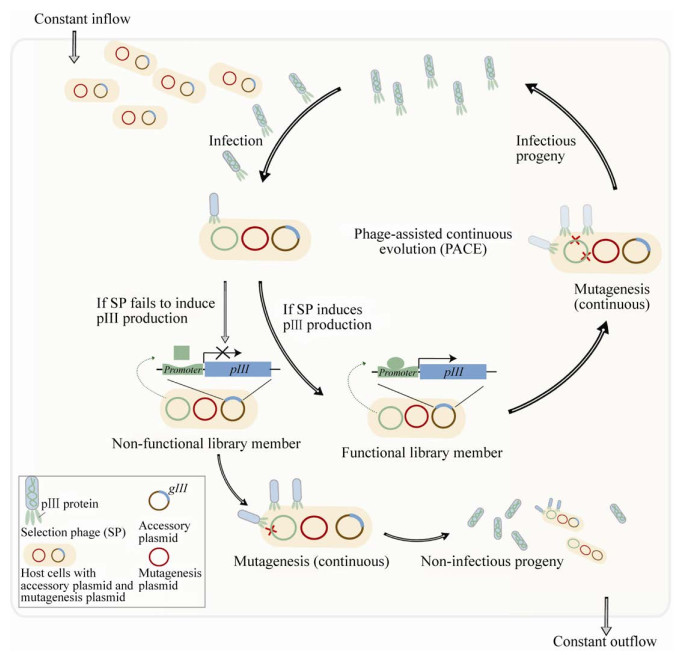
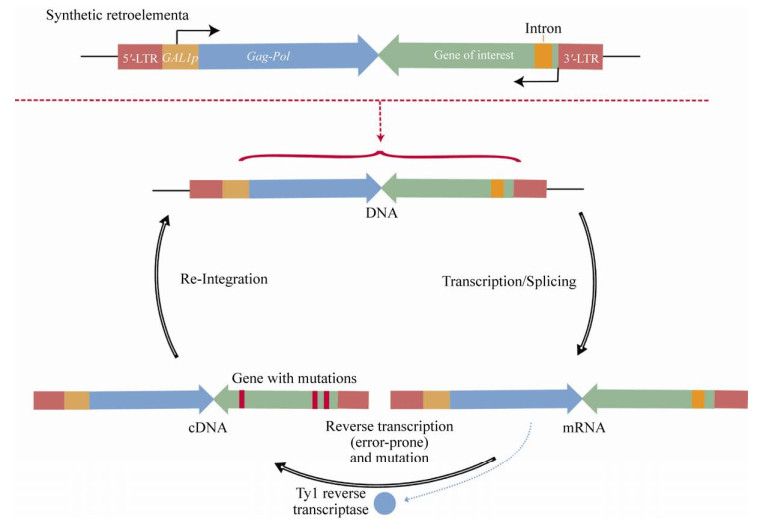
除了利用易错的DNA聚合酶,通过逆转录过程的低保真性导致突变的发生也是近几年开发出的一种体内连续进化的方式。Crook等[54]利用逆转录转座子Ty1在酿酒酵母体内建立了一个连续进化的系统(图 3)。Ty1是酵母体内天然存在的长末端重复逆转录转座子,它在转座过程中会出现一个RNA中间体,通过逆转录形成cDNA[55]。研究人员在Ty1转座子的前端加入了一个半乳糖诱导的启动子(GAL1p) 用来诱导转座子的转录,在5′-LTR和3′-LTR之间插入待突变的目的基因,目的基因内部含有人工合成的内含子,基因的转录方向与转座子的转录方向相反,而内含子的方向则与转座子转录的方向相同,所以内含子的存在阻止了目的基因RNA的剪接。在半乳糖存在的情况下,转座子起始转录,转录成mRNA,并把内含子切除,但是由于目的基因以相反的方向存在于转录本上,所以目的基因不会被翻译。接着mRNA逆转录成cDNA,重新整合到基因组上,最终完成蛋白的表达。而逆转录的过程是一个保真度较低的易错的过程,这样通过Ty1的连续转座与易错的逆转录过程相结合,达到连续进化的目的,再把目的基因的突变与筛选压力结合起来进行定向进化。在此基础上,通过调整目的基因的启动子、敲除RRM3、降低诱导温度以及增加tRNA的表达等一系列措施优化了整个系统,使转座频率达到最高。作者利用此系统可以实现对单个酶、通用转录因子以及代谢途径中多个酶的进化。如对URA3基因进行突变,筛选出对5-氟乳清酸转化5-氟尿嘧啶催化能力降低,但乳清核苷-5-磷酸转化为尿苷-5-磷酸的催化能力不变的URA3突变体。此外,还利用此定向进化系统,对通用转录因子Spt15进行进化,获得1-丁醇耐受性提高突变体;作者还进化了多基因代谢途径,例如,通过木糖异构酶以及木酮糖激酶的突变和筛选提高了酵母的木糖代谢能力。
|
| 图 3 基于反转录转座子的独立于基因组的酿酒酵母体内连续定向进化技术 Fig. 3 Genome-independent continuous directed evolution in vivo in S. cerevisiae by retrotransposon Ty1. Schematic diagram of continuous mutation in vivo mediated by retrotransposon Ty1. The gene of interest (green) containing artificial introns (yellow) is reverse cloned into the genome of the Ty1 retrotransposon, and with the expression of reverse transcriptase, the Ty1 genome containing gene of interest is converted into cDNA in an error-prone manner, and then reintegration into a stable genetic locus. |
| |
基于Ty1反转录转座子的进化系统能够的实现对目的基因甚至多基因的代谢途径的进化,但是该突变系统依赖于转座子的转座,即转座频率的高低直接影响突变的频率,此外,转座子转座存在不定向的特性,这些因素很可能会对连续突变进化造成影响。
3 总结与讨论生物分子的定向进化是产生具有新功能蛋白和核酸的重要技术,促进基本生物学问题的研究。目前,蛋白定向进化技术已经广泛地应用到生物技术的各个领域,极大地加速了生物技术的进展,然而传统的定向进化技术需要体外建立突变体库,再进行体内筛选。与传统的进化技术相比,体内连续进化技术在微生物体内就可以完成突变,并且在选择压力存在的情况下,有利突变可以随着细胞生长繁殖不断积累,在不需要大量人工干预的条件下,就可以实现有利突变的积累和扩增,省时省力,大大地加速进化进程。实际上,体内连续进化可以在不到一周的时间内生成1011种蛋白质变体[31],这种效率可以实现对需要较长进化时间的生物分子的进化[56-57]。且独立于基因组的体内连续进化技术可以在不影响微生物自身基因组复制的情况下,达到目的蛋白进化的要求。
体内连续进化技术结合特定的筛选条件在连续定向进化方面具有独特的优势,为微生物的进化以及特定蛋白或代谢途径的进化提供了极大的方便。但是与传统的定向进化相比,体内连续进化的研究依然处在比较初级的阶段。目前仅在大肠杆菌或酿酒酵母等模式微生物底盘中构建出了体内连续进化系统,并且这些系统本身也有一定的局限,例如PACE技术必须依靠噬菌体的生命活动,只适用于能被噬菌体感染的原核生物,而转座子介导的进化系统的突变则受限于转座的频率,而在酵母中构建的线性质粒复制系统,其外源基因的表达需要依靠线性质粒本身的RNA聚合酶,表达强度依然较低。此外,这些系统的应用范围也有一定的限制,有些系统只能进化某种类型的蛋白,如PACE技术只能对引起gⅢ 基因表达变化的蛋白进行突变。因此,体内连续进化技术还需要进一步的发展和完善,才能满足更为广泛的需求。
此外,体内连续进化技术很大程度上依赖于高效的筛选方法,如果没有有效的筛选方法,进化也难以实现。目前的体内进化,很多是用于提高环境耐受性、底物利用等易于筛选的特性的进化,因此筛选方法的开发也会大大拓宽体内进化的应用。目前常见的高通量筛选方法包括利用紫外光谱、可见光谱、荧光的筛选、或基于生物传感器的筛选等策略。通过紫外/可见光测量吸光度或利用荧光可以筛选具有相对复杂的分子结构或固有颜色特性的产品;如基于颜色的番茄红素高产菌株的筛选,基于荧光的核黄素高产菌株的筛选等[58-59]。近年来随着合成生物学的快速发展,各种类型的生物传感元件被设计出来,也被用来开发基于生物传感器的筛选系统。常见的生物传感器包括基于转录因子的传感器和基于RNA的传感器[60]。它们通过转录水平的调控或RNA的调控,将配体(如代谢物、蛋白、环境因子等) 的变化转化为易于检测的输出信号,因此可以将配体浓度与荧光信号或细胞生长偶联,从而实现高通量筛选[61-62]。进一步开发生物传感器等高通量筛选技术,可拓展体内进化的应用。此外,开发基于细胞生长的筛选系统,将体内进化与生长相偶联,对于实现连续进化和连续筛选至关重要。我们相信筛选技术的发展必会进一步推进和拓展体内连续进化技术的应用。
| [1] |
Way JC, Collins JJ, Keasling JD, et al. Integrating biological redesign: where synthetic biology came from and where it needs to go. Cell, 2014, 157(1): 151-161. DOI:10.1016/j.cell.2014.02.039
|
| [2] |
Mills DR, Peterson RL, Spiegelman S. An extracellular Darwinian experiment with a self-duplicating nucleic acid molecule. Proc Natl Acad Sci USA, 1967, 58(1): 217-224. DOI:10.1073/pnas.58.1.217
|
| [3] |
Wright MC, Joyce GF. Continuous in vitro evolution of catalytic function. Science, 1997, 276(5312): 614-617. DOI:10.1126/science.276.5312.614
|
| [4] |
Breaker RR, Banerji A, Joyce GF. Continuous in vitro evolution of bacteriophage RNA polymerase promoters. Biochemistry, 1994, 33(39): 11980-11986. DOI:10.1021/bi00205a037
|
| [5] |
Voytek SB, Joyce GF. Emergence of a fast-reacting ribozyme that is capable of undergoing continuous evolution. Proc Natl Acad Sci USA, 2007, 104(39): 15288-15293. DOI:10.1073/pnas.0707490104
|
| [6] |
Degnen GE, Cox EC. Conditional mutator gene in Escherichia coli: isolation, mapping, and effector studies. J Bacteriol, 1974, 117(2): 477-487. DOI:10.1128/JB.117.2.477-487.1974
|
| [7] |
Echols H, Lu C, Burgers PM. Mutator strains of Escherichia coli, mutD and dnaQ, with defective exonucleolytic editing by DNA polymerase Ⅲholoenzyme. Proc Natl Acad Sci USA, 1983, 80(8): 2189-2192. DOI:10.1073/pnas.80.8.2189
|
| [8] |
Cox EC, Horner DL. Structure and coding properties of a dominant Escherichia coli mutator gene, mutD. Proc Natl Acad Sci USA, 1983, 80(8): 2295-2299. DOI:10.1073/pnas.80.8.2295
|
| [9] |
Takano K, Nakabeppu Y, Maki H, et al. Sekiguchi M. Structure and function of dnaQ and mutD mutators of Escherichia coli. Mol Gen Genet, 1986, 205(1): 9-13. DOI:10.1007/BF02428026
|
| [10] |
Selifonova O, Valle F, Schellenberger V. Rapid evolution of novel traits in microorganisms. Appl Environ Microbiol, 2001, 67(8): 3645-3649. DOI:10.1128/AEM.67.8.3645-3649.2001
|
| [11] |
Luan GD, Cai Z, Li Y, et al. Genome replication engineering assisted continuous evolution (GREACE) to improve microbial tolerance for biofuels production. Biotechnol Biofuels, 2013, 6: 137. DOI:10.1186/1754-6834-6-137
|
| [12] |
Tanabe K, Kondo T, Onodera Y, et al. A conspicuous adaptability to antibiotics in the Escherichia coli mutator strain, dnaQ49. FEMS Microbiol Lett, 1999, 176(1): 191-196. DOI:10.1111/j.1574-6968.1999.tb13661.x
|
| [13] |
Simon M, Giot L, Faye G. The 3' to 5' exonuclease activity located in the DNA polymerase delta subunit of Saccharomyces cerevisiae is required for accurate replication. EMBO J, 1991, 10(8): 2165-2170. DOI:10.1002/j.1460-2075.1991.tb07751.x
|
| [14] |
Shimoda C, Itadani A, Sugino A, et al. Isolation of thermotolerant mutants by using proofreading- deficient DNA polymerase delta as an effective mutator in Saccharomyces cerevisiae. Genes Genet Syst, 2006, 81(6): 391-397. DOI:10.1266/ggs.81.391
|
| [15] |
Shevelev IV, Hübscher U. The 3'–5' exonucleases. Nat Rev Mol Cell Biol, 2002, 3(5): 364-376. DOI:10.1038/nrm804
|
| [16] |
Endo A, Sasaki M, Maruyama A, et al. Temperature adaptation of Bacillus subtilis by chromosomal groEL replacement. Biosci Biotechnol Biochem, 2006, 70(10): 2357-2362. DOI:10.1271/bbb.50689
|
| [17] |
Morrison A, Johnson AL, Johnston LH, et al. Pathway correcting DNA replication errors in Saccharomyces cerevisiae. EMBO J, 1993, 12(4): 1467-1473. DOI:10.1002/j.1460-2075.1993.tb05790.x
|
| [18] |
Muniyappa K, Radding CM. The homologous recombination system of phage lambda. Pairing activities of beta protein. J Biol Chem, 1986, 261(16): 7472-7478. DOI:10.1016/S0021-9258(17)38416-8
|
| [19] |
Murphy KC. Lambda Gam protein inhibits the helicase and chi-stimulated recombination activities of Escherichia coli RecBCD enzyme. J Bacteriol, 1991, 173(18): 5808-5821. DOI:10.1128/JB.173.18.5808-5821.1991
|
| [20] |
Little JW. An exonuclease induced by bacteriophage lambda. Ⅱ. Nature of the enzymatic reaction. J Biol Chem, 1967, 242(4): 679-686. DOI:10.1016/S0021-9258(18)96258-7
|
| [21] |
Murphy KC. Use of bacteriophage λ recombination functions to promote gene replacement in Escherichia coli. J Bacteriol, 1998, 180(8): 2063-2071. DOI:10.1128/JB.180.8.2063-2071.1998
|
| [22] |
Wang HH, Isaacs FJ, Carr PA, et al. Programming cells by multiplex genome engineering and accelerated evolution. Nature, 2009, 460(7257): 894-898. DOI:10.1038/nature08187
|
| [23] |
Barbieri EM, Muir P, Akhuetie-Oni BO, et al. Precise editing at DNA replication forks enables multiplex genome engineering in eukaryotes. Cell, 2017, 171(6): 1453-1467. DOI:10.1016/j.cell.2017.10.034
|
| [24] |
Dymond JS, Richardson SM, Coombes CE, et al. Synthetic chromosome arms function in yeast and generate phenotypic diversity by design. Nature, 2011, 477(7365): 471-476. DOI:10.1038/nature10403
|
| [25] |
Wu Y, Zhu RY, Mitchell LA, et al. In vitro DNA SCRaMbLE. Nat Commun, 2018, 9: 1935. DOI:10.1038/s41467-018-03743-6
|
| [26] |
Jia B, Wu Y, Li BZ, et al. Precise control of SCRaMbLE in synthetic haploid and diploid yeast. Nat Commun, 2018, 9: 1933. DOI:10.1038/s41467-018-03084-4
|
| [27] |
Luo ZQ, Wang LH, Wang Y, et al. Identifying and characterizing SCRaMbLEd synthetic yeast using ReSCuES. Nat Commun, 2018, 9: 1930. DOI:10.1038/s41467-017-00806-y
|
| [28] |
Blount BA, Gowers GF, Ho JCH, et al. Rapid host strain improvement by in vivo rearrangement of a synthetic yeast chromosome. Nat Commun, 2018, 9: 1932. DOI:10.1038/s41467-018-03143-w
|
| [29] |
Shen MJ, Wu Y, Yang K, et al. Heterozygous diploid and interspecies SCRaMbLEing. Nat Commun, 2018, 9: 1934. DOI:10.1038/s41467-018-04157-0
|
| [30] |
Liu W, Luo ZQ, Wang Y, et al. Rapid pathway prototyping and engineering using in vitro and in vivo synthetic genome SCRaMbLE-in methods. Nat Commun, 2018, 9: 1936. DOI:10.1038/s41467-018-04254-0
|
| [31] |
Esvelt KM, Carlson JC, Liu DR. A system for the continuous directed evolution of biomolecules. Nature, 2011, 472(7344): 499-503. DOI:10.1038/nature09929
|
| [32] |
Rakonjac J, Model P. Roles of pⅢ in filamentous phage assembly. J Mol Biol, 1998, 282(1): 25-41. DOI:10.1006/jmbi.1998.2006
|
| [33] |
Nelson FK, Friedman SM, Smith GP. Filamentous phage DNA cloning vectors: a noninfective mutant with a nonpolar deletion in gene Ⅲ. Virology, 1981, 108(2): 338-350. DOI:10.1016/0042-6822(81)90442-6
|
| [34] |
Boeke JD, Model P, Zinder ND. Effects of bacteriophage f1 gene Ⅲ protein on the host cell membrane. Mol Gen Genet, 1982, 186(2): 185-192. DOI:10.1007/BF00331849
|
| [35] |
Fijalkowska IJ, Schaaper RM. Mutants in the Exo Ⅰ motif of Escherichia coli dnaQ: defective proofreading and inviability due to error catastrophe. Proc Natl Acad Sci USA, 1996, 93(7): 2856-2861. DOI:10.1073/pnas.93.7.2856
|
| [36] |
Brödel AK, Jaramillo A, Isalan M. Engineering orthogonal dual transcription factors for multi-input synthetic promoters. Nat Commun, 2016, 7: 13858. DOI:10.1038/ncomms13858
|
| [37] |
Hochschild A, Lewis M. The bacteriophage λ CI protein finds an asymmetric solution. Curr Opin Struct Biol, 2009, 19(1): 79-86. DOI:10.1016/j.sbi.2008.12.008
|
| [38] |
Suzuki T, Miller C, Guo LT, et al. Crystal structures reveal an elusive functional domain of pyrrolysyl-tRNA synthetase. Nat Chem Biol, 2017, 13(12): 1261-1266. DOI:10.1038/nchembio.2497
|
| [39] |
Wan W, Tharp JM, Liu WR. Pyrrolysyl-tRNA synthetase: an ordinary enzyme but an outstanding genetic code expansion tool. Biochim Biophys Acta, 2014, 1844(6): 1059-1070. DOI:10.1016/j.bbapap.2014.03.002
|
| [40] |
Woolston BM, Roth T, Kohale I, et al. Development of a formaldehyde biosensor with application to synthetic methylotrophy. Biotechnol Bioeng, 2018, 115(1): 206-215. DOI:10.1002/bit.26455
|
| [41] |
Roth TB, Woolston BM, Stephanopoulos G, et al. Phage-assisted evolution of Bacillus methanolicus methanol dehydrogenase 2. ACS Synth Biol, 2019, 8(4): 796-806. DOI:10.1021/acssynbio.8b00481
|
| [42] |
Greener A, Callahan M, Jerpseth B. An efficient random mutagenesis technique using an E. coli mutator strain. Methods Biotechnol, 1997, 7(2): 189-195.
|
| [43] |
Greener A, Callahan M. XL1-red: highly efficient random mutagenesis strain. Strategies, 1994, 7: 32-34.
|
| [44] |
Bornscheuer UT, Altenbuchner J, Meyer HH. Directed evolution of an esterase for the stereoselective resolution of a key intermediate in the synthesis of epothilones. Biotechnol Bioeng, 1998, 58(5): 554-559. DOI:10.1002/(SICI)1097-0290(19980605)58:5<554::AID-BIT12>3.0.CO;2-B
|
| [45] |
Bornscheuer UT, Altenbuchner J, Meyer HH. Directed evolution of an esterase: screening of enzyme libraries based on pH-indicators and a growth assay. Bioorg Med Chem, 1999, 7(10): 2169-2173. DOI:10.1016/S0968-0896(99)00147-9
|
| [46] |
Terao Y, Miyamoto K, Ohta H. Improvement of the activity of arylmalonate decarboxylase by random mutagenesis. Appl Microbiol Biotechnol, 2006, 73(3): 647-653. DOI:10.1007/s00253-006-0518-z
|
| [47] |
Callanan MJ, Russell WM, Klaenhammer TR. Modification of Lactobacillus β-glucuronidase activity by random mutagenesis. Gene, 2007, 389(2): 122-127. DOI:10.1016/j.gene.2006.10.022
|
| [48] |
Amara AA, Steinbüchel A, Rehm BHA. In vivo evolution of the Aeromonas punctata polyhydroxyalkanoate (PHA) synthase: isolation and characterization of modified PHA synthases with enhanced activity. Appl Microbiol Biotechnol, 2002, 59(4/5): 477-482.
|
| [49] |
Camps M, Naukkarinen J, Johnson BP, et al. Targeted gene evolution in Escherichia coli using a highly error-prone DNA polymerase Ⅰ. Proc Natl Acad Sci USA, 2003, 100(17): 9727-9732. DOI:10.1073/pnas.1333928100
|
| [50] |
Gunge N, Sakaguchi K. Intergeneric transfer of deoxyribonucleic acid killer plasmids, pGKl1 and pGKl2, from Kluyveromyces lactis into Saccharomyces cerevisiae by cell fusion. J Bacteriol, 1981, 147(1): 155-160. DOI:10.1128/JB.147.1.155-160.1981
|
| [51] |
Ravikumar A, Arrieta A, Liu CC. An orthogonal DNA replication system in yeast. Nat Chem Biol, 2014, 10(3): 175-177. DOI:10.1038/nchembio.1439
|
| [52] |
Wooden JM, Hartwell LH, Vasquez B, et al. Analysis in yeast of antimalaria drugs that target the dihydrofolate reductase of Plasmodium falciparum. Mol Biochem Parasitol, 1997, 85(1): 25-40. DOI:10.1016/S0166-6851(96)02808-3
|
| [53] |
Ravikumar A, Arzumanyan GA, Obadi MKA, et al. Scalable, continuous evolution of genes at mutation rates above genomic error thresholds. Cell, 2018, 175(7): 1946-1957. DOI:10.1016/j.cell.2018.10.021
|
| [54] |
Crook N, Abatemarco J, Sun J, et al. In vivo continuous evolution of genes and pathways in yeast. Nat Commun, 2016, 7: 13051. DOI:10.1038/ncomms13051
|
| [55] |
Wilhelm FX, Wilhelm M, Gabriel A. Reverse transcriptase and integrase of the Saccharomyces cerevisiae Ty1 element. Cytogenet Genome Res, 2005, 110(1/4): 269-287.
|
| [56] |
Wichman HA, Millstein J, Bull JJ. Adaptive molecular evolution for 13, 000 phage generations: a possible arms race. Genetics, 2005, 170(1): 19-31. DOI:10.1534/genetics.104.034488
|
| [57] |
Marlière P, Patrouix J, Döring V, et al. Chemical evolution of a bacterium's genome. Angew Chem Int Ed Engl, 2011, 50(31): 7109-7114. DOI:10.1002/anie.201100535
|
| [58] |
Qiang W, Ling RF, Luo W, et al. Mutation breeding of lycopene-producing strain Blakeslea trispora by a novel atmospheric and room temperature plasma (ARTP). Appl Biochem Biotechnol, 2014, 174(1): 452-460. DOI:10.1007/s12010-014-0998-8
|
| [59] |
Wagner JM, Liu LQ, Yuan SF, et al. A comparative analysis of single cell and droplet-based FACS for improving production phenotypes: Riboflavin overproduction in Yarrowia lipolytica. Metab Eng, 2018, 47: 346-356. DOI:10.1016/j.ymben.2018.04.015
|
| [60] |
Abatemarco J, Sarhan MF, Wagner JM, et al. RNA-aptamers-in-droplets (RAPID) high-throughput screening for secretory phenotypes. Nat Commun, 2017, 8: 332. DOI:10.1038/s41467-017-00425-7
|
| [61] |
Qiu CX, Zhai HT, Hou J. Biosensors design in yeast and applications in metabolic engineering. FEMS Yeast Res, 2019, 19(8): foz082. DOI:10.1093/femsyr/foz082
|
| [62] |
Chen XX, Yang XY, Shen Y, et al. Screening phosphorylation site mutations in yeast acetyl-CoA carboxylase using malonyl-CoA sensor to improve malonyl-CoA-derived product. Front Microbiol, 2018, 9: 47. DOI:10.3389/fmicb.2018.00047
|
 2021, Vol. 37
2021, Vol. 37