中国科学院微生物研究所、中国微生物学会主办
文章信息
- 谭黄虹, 王静, 刘青, 郑兆娟, 欧阳嘉
- TAN Huanghong, WANG Jing, LIU Qing, ZHENG Zhaojuan, OUYANG Jia
- 果胶D-半乳糖醛酸生物转化制备黏酸研究进展
- Production of mucic acid from pectin-derived D-galacturonic acid: a review
- 生物工程学报, 2022, 38(2): 666-677
- Chinese Journal of Biotechnology, 2022, 38(2): 666-677
- 10.13345/j.cjb.210268
-
文章历史
- Received: March 31, 2021
- Accepted: July 19, 2021
- Published: August 13, 2021
随着化石资源的日益匮乏和环境问题的加剧,基于可再生资源制备能源、功能性材料和化学品越来越受到研究者的关注[1]。生物质是唯一的可再生碳资源,将生物质转化成平台化合物和大宗化学品是生物质高值化利用的重要发展方向[2-3]。黏酸(meso-galactaric acid或mucic acid),也称之为半乳糖二酸,化学结构与葡萄糖二酸(glucaric acid, GA) 相似,同属于己糖二酸,其潜在应用领域也与葡萄糖二酸类似。葡萄糖二酸及其衍生物已被证明具有广泛的应用价值,不仅可以降低胆固醇[4]、治疗糖尿病[5]、预防癌症[6-7]等,也可以应用于医学成像领域[8-9]。葡萄糖二酸还可以作为单体合成新型羟基化尼龙材料等可降解聚合物[10-12],早在2004年就被美国能源部确定为10种“最具价值的生物炼制产品”之一[13]。微生物中不存在完整的从葡萄糖到葡萄糖二酸的合成途径,人工构建的葡萄糖二酸合成路径长、涉及多个酶催化反应,最终产物得率往往比较低[14-15]。黏酸可由果胶生物质中的D-半乳糖醛酸氧化得到,该反应仅涉及一个特异性的糖醛酸脱氢酶的催化,反应过程更可控、反应催化效率更高。相较于葡萄糖二酸,研究者对黏酸的关注比较晚,其生物制备方法和应用领域正处于不断开发中[16]。
本文重点介绍了生物质果胶的结构组成和水解方法、不同微生物中D-半乳糖醛酸的代谢途径以及基于代谢工程改造上述途径利用重组微生物细胞制备黏酸的研究进展,探讨了黏酸在化工、材料等领域的应用潜力,并提出了生物法制备黏酸的未来研究发展方向等,以期为相关研究者提供参考。
1 果胶结构和水解果胶作为细胞壁的重要组分,广泛分布于植物界中,例如苹果渣和柑橘皮等废弃生物质资源都富含果胶。从结构上看,果胶是一种由D-半乳糖醛酸残基(GalpA) 通过α-1, 4-糖苷键连接而成的复杂酸性多糖分子,带有L-鼠李糖、L-阿拉伯糖、D-半乳糖、D-木糖、L-岩藻糖、D-芹菜糖等不同中性糖单元组成的侧链,主链中的羧基常以部分甲酯化或乙酯化形式存在。从糖基组成上看,酸性糖半乳糖醛酸残基占果胶多糖的60%以上,中性糖残基总质量分数约为10%–20%[17]。
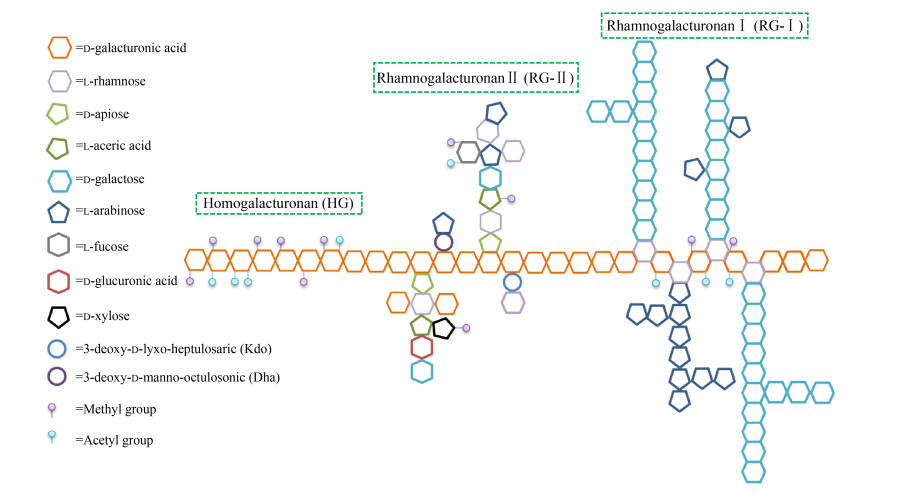
常见的果胶结构区域有3种(图 1):同聚半乳糖醛酸(homogalacturonan, HG)、Ⅰ型聚鼠李半乳糖醛酸(rhamnogalacturonan Ⅰ, RG-Ⅰ)、Ⅱ型聚鼠李半乳糖醛酸(rhamnogalacturonan Ⅱ, RG-Ⅱ)。HG是由α-1, 4-糖苷键连接的GalpA组成的线性链,其中的部分C-6可被甲酯化,其O-2和/或O-3位置可被乙酰化。RG-Ⅰ则是GalpA和鼠李糖残基(Rhap) 重复连接的线性链(→4)-α-D-GalpA-(1→2)-α-L-Rhap-(1→),连接有阿拉伯聚糖、聚半乳糖等支链结构,并且GalpA上的O-2或O-3也会被乙酰化[17]。RG-Ⅱ结构与RG-Ⅰ并不相似,相反地,RG-Ⅱ拥有1条与HG一样的主链,即由α-1, 4-糖苷键连接GalpA组成,而GalpA上含有侧链取代基,可以是2个单糖或8个单糖。果胶还含有其他结构,比如木聚半乳糖醛酸结构和芹菜聚半乳糖醛酸结构[18-19]。
|
| 图 1 常见果胶结构区域 Fig. 1 Schematic illustration of the structure of pectin. |
| |
果胶酶是一类降解果胶分子的多种酶的总称,根据其活性位点差异,果胶酶常被划分为3大类:酯酶、水解酶和裂解酶[20]。
果胶酯化会抑制多聚半乳糖醛酸的解聚断裂,通过果胶酯酶催化酯键水解,将半乳糖醛酸的羧基重新释放出来,可以促进多聚半乳糖醛酸被其他酶类进一步降解。果胶甲酯酶(pectin methyl esterases, PME) 是研究较多的一类果胶酯酶,可水解甲酯化的羧基生成果胶酸,后者是果胶水解酶的更适宜底物[21]。果胶甲酯酶在细菌、真菌和植物中无处不在,在植物的繁殖、生长和防御中起着重要作用[22]。
果胶水解酶也称为多聚半乳糖醛酸酶(polygalcturonase, PG),通过水解作用催化断裂多聚半乳糖醛酸之间的α-1, 4-糖苷键。PG又分为内切果胶水解酶(Endo-PG) 和外切果胶水解酶(Exo-PG),内切果胶水解酶从分子内部随机水解多聚半乳糖醛酸生成寡聚半乳糖醛酸,而外切果胶水解酶从分子末端逐一水解断裂α-1, 4-糖苷键产生半乳糖醛酸单体[20, 23]。果胶水解酶在真菌和细菌中广泛存在,目前主要被应用于果汁澄清、蔬菜浸渍等食品加工行业。果胶裂解酶通过β-消除机制裂解果胶多糖,生成4, 5-不饱和寡聚半乳糖醛酸[21]。果胶裂解酶可以进一步分为两个亚类,分别适宜催化低酯果胶和高酯果胶的解聚。果胶裂解酶在纺织工业、食品加工、纸浆加工、油脂提取和工业废水处理等领域都具有巨大的应用潜力[20]。
利用酸水解和果胶酶解等降解方法或者进一步耦合超声波法、水热法等辅助手段可以对果胶进行可控降解,通过控制反应条件,使得反应产物以果胶低聚糖或者单糖为主[24-25]。若以酸法或者水热法事先除去果胶中性糖支链,则可以显著促进果胶酶的催化性能,大幅提高果胶降解效率[26]。
2 微生物D-半乳糖醛酸代谢途径及相应的生物法合成黏酸策略很多原核生物和真核生物都能够代谢D-半乳糖醛酸,其代谢途径差异较大(表 1)。D-半乳糖醛酸在原核生物中的代谢途径主要有2种:一是氧化途径,通过醛酸脱氢酶将D-半乳糖醛酸氧化为黏酸,之后进入下游分解途径,例如食酸假单胞菌(Pseudomonas acidovorans) 和根癌农杆菌(Agrobacterium tumefaciens) 等微生物以该途径代谢D-半乳糖醛酸[27];二是异构化途径,通过糖醛酸异构酶将D-半乳糖醛酸异构化为D-塔格糖酮酸,进而进入下游分解途径,例如大肠杆菌(Escherichia coli) 和嗜碱芽孢杆菌(Bacillus halodurans) 中都含有糖醛酸异构酶,以异构化途径代谢D-半乳糖醛酸[28-29]。
| Metabolic pathways | Typical strains | The first enzyme | The first intermediate | Advantages | Disadvantages |
| Oxidative pathway | P. acidovorans, A. tumefaciens | Uronate dehydrogenase | Mucic acid | Possessing endogenous Udh | Needing inactivation of endogenous mucic acid dehydratase |
| Isomerization pathway | E. coli, B. halodurans | Uronate isomerase | D-tagaturoronate | E. coli is a prokaryotic model organism | No Udh, needing inactivation of endogenous mucic acid dehydratase and UxaC |
| Reductive pathway | T. reesei, A. niger | D-galacturonate reductase | L-galactonate | Eukaryotic model microorganisms and GRAS strains | No Udh, needing inactivation of D-galacturonate reductase |
| “GRAS”: generally recognized as safe. | |||||
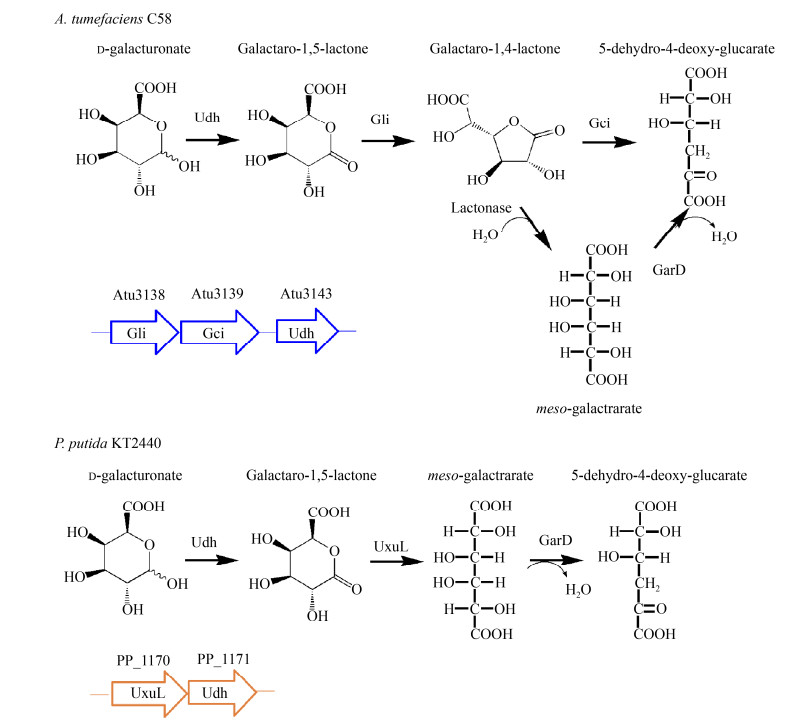
图 2所示是原核微生物中的D-半乳糖醛酸氧化途径。D-半乳糖醛酸首先被糖醛酸脱氢酶(uronate dehydrogenases, Udh) 氧化生成黏酸,黏酸可以进一步脱水脱羧氧化,在黏酸脱水酶(D-galactarate dehydratase,GadD)、4-脱氧-5-脱氢-葡萄糖二酸脱水酶(脱羧) (5-dehydro-4- deoxyglucarate dehydratase (decarboxylating),KdgD)、α-酮戊二酸半醛脱氢酶(2-ketoglutaric semialdehyde dehydrogenase,KgsD) 的依次催化下转化为α-酮戊二酸,后者可以被菌体完全利用。虽然通常认为,D-半乳糖醛酸在Udh的催化下生成黏酸,但实际上,D-半乳糖醛酸的直接氧化产物是半乳糖二酸-1, 5-内酯,随后半乳糖二酸-1, 5-内酯自发水解生成黏酸。Bouvier等基于比较基因组学大数据分析了变形菌门中4种不同科属微生物的D-半乳糖醛酸代谢和调节相关基因或操纵子,发现在伯克氏菌(Burkholderiaceae)、丛毛单胞菌(Comamonadaceae) 和假单胞菌(Pseudomonadaceae) 3个科中,Udh在基因组上的排布往往与2个新型内酯酶UxuL和UxuF相邻,处于同一调节子内,从而推测半乳糖二酸-1, 5-内酯也能被后者水解开环生成黏酸;但是,在盐单胞菌科(Halomonadaceae) 的微生物中,Udh与半乳糖二酸-δ-内酯异构酶Gli (δ-lactone isomerase) 和半乳糖二酸内酯环异构酶Gci (γ-lactone cycloisomerase) 相邻,处于同一调节子内,基因组上也没有UxuL和UxuF的同源蛋白,这与A. tumefaciens类似[30]。A. tumefaciens中的糖醛酸氧化途径是目前研究最多最为清楚的原核生物D-半乳糖醛酸氧化途径,研究者从A. tumefaciens中鉴定了Gli和Gci 2个代谢半乳糖二酸内酯的酶蛋白,推测A. tumefaciens中存在另一条D-半乳糖醛酸氧化途径,即Udh的氧化产物半乳糖酸-1, 5-内酯可被Gli和Gci催化得到产物2-酮基-3-脱氧-L-苏-己糖二酸,后续路径和Pseudomonadaceae等科微生物的氧化路径一致[31-32]。图 3中,笔者以恶臭假单胞菌(Pseudomonas putida) KT2440和A. tumefaciens C58为例,分别阐释了这2株菌中D-半乳糖醛酸氧化途径的初始反应步骤和相关催化酶蛋白,可以看到一个非常明显的区别,即当经由Gli和Gci催化时,中间产物没有黏酸生成。
|
| 图 3 A. tumefaciens C58和P. putida KT2440中D-半乳糖醛酸氧化途径的初始反应步骤和相关催化酶蛋白 Fig. 3 The initial reaction steps of the oxidation pathway of D-galacturonic acid and related catalytic enzymes in A. tumefaciens C58 and P. putida KT2440. |
| |
综上所述,如果基于上述氧化途径生物转化D-半乳糖醛酸生产黏酸,需要选择Pseudomonadaceae等科的微生物,敲除黏酸脱水酶等关键基因,阻断黏酸下游代谢(表 1)。不过,笔者总结现有的黏酸生产相关研究,并没有发现基于该氧化途径生产黏酸的报道。笔者以P. putida KT2440为宿主,通过删除假定的GadD编码基因,并提高Udh的胞内酶活力,证实该路径是一条行之有效的黏酸生产路径,且黏酸生产效率明显高于现有文献报道,相关研究工作结果正在整理中。Udh是一种依赖于NAD+的氧化还原酶,一般由2个亚基组成同型二聚体,相对分子量约为60 kDa[33]。Yoon等研究者分别鉴定了来自丁香假单胞菌(Pseudomonas syringae) DC3000、P. putida KT2440以及A. tumefaciens C58的3个糖醛酸脱氢酶。纯酶动力学分析表明,这3种Udh对D-半乳糖醛酸和D-葡萄糖醛酸都有活力,且对D-半乳糖醛酸的活力略高于对D-葡萄糖醛酸的活力;但对D-半乳糖和D-葡萄糖的醛基无催化活力。来自A. tumefaciens C58的Udh对D-半乳糖醛酸的kcat最高,而来自P. syringae的Udh对D-半乳糖醛酸的催化能力最强(kcat/Km)[34]。之后,Pick等也筛选鉴定了5个不同种属来源的Udh,分别来自Fulvimarina pelagi、产绿色链霉菌(Streptomyces viridochromogenes)、Oceanicola granulosus、A. tumefaciens以及P. syringae,通过分析比较发现,除了O. granulosus来源的Udh活力很低外,其余Udh活力都比较高,尤其是A. tumefaciens和P. syringae来源的Udh[35]。但是,总体上看,目前关于Udh的筛选鉴定工作依然比较少,缺乏更多对D-半乳糖醛酸有高效催化活力的新酶,这也限制了黏酸生产效率的进一步提升。
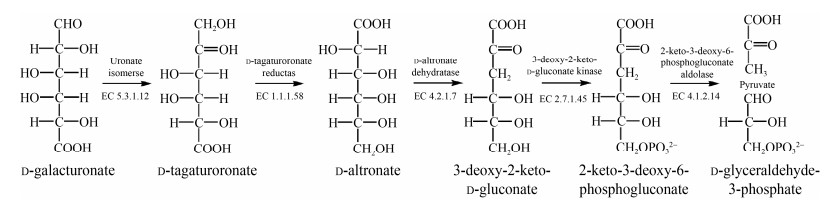
2.2 原核生物中的异构化途径图 4所示是D-半乳糖醛酸在大肠杆菌等原核微生物中的异构化途径。以大肠杆菌为例,糖醛酸异构酶(uronate isomerase, UxaC) 催化D-半乳糖醛酸异构化为D-塔格糖酮酸,随后依次在D-塔格糖酮酸还原酶(D-tagaturonate reductas, UxaB)、D-阿卓糖酸脱水酶(D-altronate dehydratase, UxaA)、2-酮基-3-脱氧-D-葡萄糖酸激酶(2-keto-3-deoxy-D-gluconate kinae, KdgK) 和2-酮基-3-脱氧-6-磷酸葡萄糖酸缩醛酶(2-keto-3-deoxy-6-phosphogluconate aldolase, KdgA) 的催化下,最终断裂为丙酮酸和D-甘油醛-3-磷酸,从而进入TCA循环,使得D-半乳糖醛酸被菌体完全代谢利用[16]。原核生物以异构化途径代谢D-半乳糖醛酸时,中间产物没有黏酸生成。不过,值得一提的是,尽管大肠杆菌无法将D-半乳糖醛酸转化为黏酸,但是大肠杆菌具备分解代谢黏酸的能力,能以黏酸为唯一碳源生长[36]。当黏酸存在时,大肠杆菌中的黏酸脱水酶可以把黏酸转化为2-酮基-3-脱氧-L-苏-己糖二酸,与图 2所示途径的不同之处在于,下一步反应是由2-脱氢-3-脱氧葡萄糖酸缩醛酶(2-dehydro-3-deoxyglucarate aldolase, EC 4.1.2.20) 催化的裂解反应,产物为丙酮酸和L-酒石酸半醛,随后L-酒石酸半醛经2-羟基-3-氧代丙酸还原酶(2-hydroxy-3-oxopropionate reductase, EC 1.1.1.60) 还原为甘油酸。如果以大肠杆菌为宿主生产黏酸,不仅要敲除编码糖醛酸异构酶的基因,阻断D-半乳糖醛酸的内源代谢途径,还要外源表达能氧化D-半乳糖醛酸到黏酸的糖醛酸脱氢酶,并阻断黏酸的下游代谢通路(表 1)。Zhang等利用该策略以大肠杆菌为宿主生产黏酸,他们异源表达了来自A. tumefaciens的糖醛酸脱氢酶编码基因udh,敲除了大肠杆菌中编码糖醛酸异构酶的基因uxaC和编码黏酸脱水酶的基因garD。以该重组大肠杆菌为生物催化剂进行全细胞催化,以D-半乳糖醛酸为底物可生成10.3 g/L的黏酸,得率为95.4% (表 2);以甜菜渣水解液为底物可获得6.9 g/L的黏酸,基于D-半乳糖醛酸的得率为86%,基于甜菜渣的得率为14.2%[37]。
| Biocatalyst | Substrates | Production methods | Time (h) | Titer (g/L) | Yield (%) | References |
| E. coli BL21 ΔuxaC ΔgarD udh | D-galacturonic acid, 10 g/L | Resting cell | 48 | 10.3 | 95.4 | [37] |
| T. reesei QM6a Δgar1 udh | D-galacturonic acid, 17.4 g/L | Growing cell | 211 | 4.2 | 22.3 | [38] |
| A. niger ATCC1015 ΔgaaA udh | D-galacturonic acid, 17.4 g/L | Growing cell | 211 | 1.1 | 5.8 | [38] |
| A. niger ATCC1015 ΔgaaA Δ39114 udh | D-galacturonic acid, 20 g/L | Growing cell | 120 | 4.0 | 18.5 | [39] |
| T. reesei QM6a Δgar1 udh | D-galacturonic acid, 25 g/L | Fed-batch | 200 | 20.0 | 73.8 | [40] |
| T. reesei QM6a Δgar1 udh | Pectin, 29.2 g/L | Fed-batch | 180 | 21.0 | – | [41] |
| Trichoderma sp. LF328 Δgar2 udh | D-galacturonic acid, 72 g/L | Fed-batch | 180 | 25.0 | 34.3 | [42] |
| Coniochaeta sp. MF729 Δgar2 udh | D-galacturonic acid, 72 g/L | Fed-batch | 180 | 2.0 | 2.7 | [42] |
| S. cerevisiae gatA udh | Citrus peel waste | Fed-batch | 80 | 8.0 | – | [43] |
| The yield is defined as the percentage of the measured mucic acid concentration to the theoretical mucic acid concentration based on the initial amount of D-galacturonic acid. The “–” indicates no relevant data. | ||||||
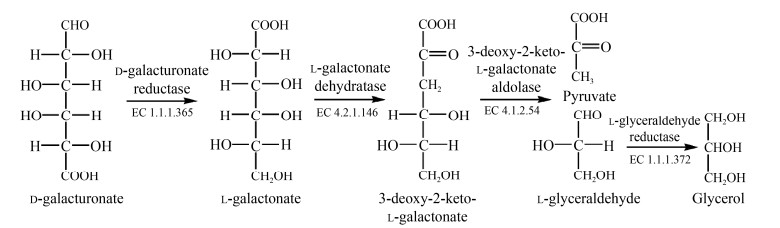
真核生物的D-半乳糖醛酸代谢途径(图 5) 与原核生物不同,在真核生物中,D-半乳糖醛酸首先被NADPH依赖型D-半乳糖醛酸还原酶(D-galacturonate reductase) 还原为L-半乳糖酸,随后经过L-半乳糖酸脱水酶(L-galactonate dehydratase)、2-酮基-3-脱氧-L-半乳糖酸缩醛酶(2-keto-3-deoxy-L-galactonate aldolase) 催化将L-半乳糖酸裂解为丙酮酸和L-甘油醛,后者继续被NADPH依赖型L-甘油醛还原酶(L-glyceraldehyde reductase) 转化为甘油[16]。与原核生物异构化途径类似,真核生物代谢D-半乳糖醛酸时,中间产物也没有黏酸生成。因此,如果以真核生物为宿主生产黏酸,也需要通过分子生物学手段对D-半乳糖醛酸还原酶基因等D-半乳糖醛酸下游代谢关键基因进行敲除,并外源表达糖醛酸脱氢酶编码基因udh,还要考察菌株是否能够代谢黏酸,是否需要进一步失活黏酸代谢相关基因(表 1)。
以里氏木霉(Trichoderma reesei)、黑曲霉(Aspergillus niger) 等真核生物为宿主生产黏酸是目前报道中最常见的黏酸生产方式,其产量也相对较高(表 2)。例如,Mojzita等研究者利用重组的T. reesei和A. niger生产黏酸,首先敲除了D-半乳糖醛酸还原酶基因,其次外源表达了来自A. tumefaciens的醛酸脱氢酶基因udh。工程菌T. reesei QM6a Δgar1 udh和A. niger ATCC 1015 ΔgaaA udh在pH 5.0、30 ℃的条件下,以17 g/L D-半乳糖醛酸和2 g/L D-葡萄糖共培养时,其黏酸产量分别为4.2 g/L和1.1 g/L[38]。其中,A. niger会进一步代谢黏酸,致使黏酸最终浓度偏低。之后,Kuivanen等研究者进一步分析了黑曲霉的黏酸生产过程与代谢调控,基于转录组数据分析,推测了数个可能与黏酸代谢相关的基因,并使用CRISPR/Cas9对其进行敲除。最终,当同时删除D-半乳糖醛酸还原酶和未知功能蛋白39114后,以20 g/L D-半乳糖醛酸为底物,大约生成了4 g/L的黏酸[39]。Barth和Wiebe在Mojzita等构建的重组里氏木霉基础上,进一步考察了培养基和反应条件对黏酸生产的影响。在pH 4.0、35 ℃时,以乳糖为辅助底物,以铵盐和酵母粉为氮源,通过底物流加策略生成了20 g/L的黏酸,黏酸的产量比较高,但总体生产速率比较低,初始产率仅为0.18 g/(L·h)[40]。在此基础上,Paasikallio等研究者利用构建好的工程菌T. reesei QM6a Δgar1 udh以食品级果胶为底物,将生产规模分别扩大到1、10和250 L,其中10 L的产量最高,可达21 g/L[41]。随后,该团队研究考察了利用海洋真菌Trichoderma sp. LF328和Coniochaeta sp. MF729生产黏酸的能力。对上述2株菌株进行代谢工程改造后,Trichoderma sp. LF328在以D-半乳糖醛酸和D-葡萄糖为共培养底物时,黏酸产量能达到25 g/L,是目前生物法生产黏酸所报道的最高产量,而Coniochaeta sp. MF729生产效率比较低,在上述培养条件下仅能生产2 g/L黏酸。但是,值得一提的是,Coniochaeta sp. MF729能以果胶为底物生产黏酸(6 g/L),而Trichoderma sp. LF328则不行,可能是由于后者缺乏相关果胶分解利用蛋白[42]。Protzko等以脐橙皮水解液为底物,利用代谢工程改造过的酿酒酵母(Saccharomyces cerevisiae),实现了D-半乳糖醛酸和D-葡萄糖的同步利用以及黏酸的生产。他们不仅在S. cerevisiae中引入了A. tumefacien来源的Udh,并且鉴定了一个A. niger来源的新型D-半乳糖醛酸转运蛋白GatA,以GatA转运D-半乳糖醛酸时,其转运不受D-葡萄糖抑制,可以实现2种底物的同步利用,最终生成了8.0 g/L黏酸[43]。
综合以上内容可以看出,在生物法生产黏酸的研究中,不管是以原核生物还是真核生物为宿主,都外源表达了来自A. tumefaciens的Udh (表 2),这说明此Udh在D-半乳糖醛酸氧化上的确有催化优势,但也说明了目前可选Udh的种类相对匮乏,需要进一步挖掘鉴定。此外,上述研究都是以菌体细胞为催化剂生产黏酸,目前还没有利用胞外酶催化生产黏酸的报道,这可能是由于Udh以NAD+为辅因子,体外催化需要昂贵的辅因子或耦联高效的辅因子再生系统,从而增加了过程生产成本。
3 黏酸的应用前景黏酸有着广泛的应用前景,其衍生物在医药、化工、化妆品等行业中发挥着重要的作用。例如,它可以合成平台化合物、高分子聚合物和金属有机骨架等[44]。
在平台化合物合成方面,黏酸可以用来制备呋喃二甲酸(2, 5-furandicarboxylic acid, FDCA)和己二酸[37, 45]。FDCA的市场前景非常广阔,其与石油基大宗化学品对苯二甲酸结构相似,可以替代对苯二甲酸用于制造聚酯、聚酰胺类材料。2004年,美国能源部将FDCA列为可通过以生物质为原料制备的化学品,同时也是最具价值、最有希望替代石化产业中基础化学品的12个平台化学品之一[46]。Amarasekara等使用黏酸和HBr混合反应18 h,通过蒸馏除去部分HBr,对黑色悬浮物进行冰浴处理并添加NaOH溶液,过滤后添加HCl置于冰箱过夜使其形成结晶,固体产物通过吸附过滤并在空气中干燥,即可得到纯品FDCA[47]。
己二酸是尼龙的前体,是化学工业中最重要的二元羧酸之一,每年市场容量为280万t[48]。Li等采用一锅两步法以黏酸为底物生产己二酸,第一步在3-戊醇中利用甲基三氧化铼和甲苯磺酸催化黏酸生成中间产物,第二步利用Pt/C催化剂催化中间产物生成己二酸酯。整个反应先在有氧条件下,120 ℃催化12 h,接着在密闭的条件下,160–200 ℃催化12 h。己二酸酯得率为99%,将己二酸酯进一步水解得到游离的己二酸,收率可达94%[49]。Zhang等则是在3-戊醇中利用NH4ReO4对黏酸进行脱水脱氧反应,在120 ℃的条件下反应8 h后对产物进行分离,得到黏糠酸,其得率为90%。随后以Pt/C为催化剂,在温和条件下(水溶液、常温、H2、7 MPa) 对黏糠酸进行加氢反应,8 h后,己二酸得率为92%[37]。
在高分子聚合物合成方面,Mehtiö等[50]利用黏酸合成聚酸酐,它提高了聚酸酐的熔点并减缓了其降解速率。Pan和Davis基于黏酸和聚乙二醇(polyethylene glycol, PEG) 合成1个阳离子黏酸聚合物——mPEG-cMAP-PEGm,并以该三嵌段聚合物制备了含有小干扰RNA的纳米颗粒[51]。Gu等[52]以黏酸为基础合成了1个糖基两亲聚合物(sugar-based amphiphilic polymers, SBAPs),与传统的两亲聚合物相比,SBAPs的疏水链段是烷基化的糖主链,而聚乙二醇链充当亲水结构域,因此表现出较低的临界胶束浓度,有望应用于临床药学上。
在金属有机骨架上,Wong等利用黏酸为基础合成了一个黏酸金属有机框架({[Tb(Mucicate)1.5(H2O)2]•5H2O}n),该有机框架并入了镧系金属中心,这些中心被设计用作监测客体分子存在的检测器[53]。
4 总结与展望黏酸在医药、化工、材料等行业都有着广泛的应用,其生物合成路径简单,由果胶生物质中的D-半乳糖醛酸一步氧化即得。但目前黏酸生产上应用的Udh来源非常局限,构建的微生物细胞催化剂种类也比较少,后续研究中需要挖掘更多催化性能优良的Udh,并进一步开发以微生物为催化剂的生产工艺,尤其是基于原核生物中的氧化途径实现D-半乳糖醛酸至黏酸的生物转化。
为了进一步丰富黏酸生产的生物工艺和手段,提高生物合成黏酸的产量,降低生产成本,研究者还可以从其他方面开展相关研究。例如,开发适于胞外催化的高效酶蛋白用于黏酸生产。Sakuta等发现,吡咯并喹啉醌依赖型葡萄糖脱氢酶(pyrroloquinoline quinone-dependent glucose dehydrogenase, PQQ-GDH) 不仅能氧化一系列单糖生成相应的糖酸,由于其极宽的底物谱,PQQ-GDH也能氧化D-半乳糖醛酸生成黏酸,该酶不仅不需要NAD+等昂贵辅因子,还可以直接固定于电极,在电场中生成黏酸[54]。此外,目前关于D-半乳糖醛酸转运蛋白的报道和相关研究非常少,提高菌株对D-半乳糖醛酸的转运能力也是增强黏酸生产效率的重要方面。例如,Protzko等比较了粗糙脉胞霉(Neurospora crassa)、A. niger、T. reesei等不同来源的D-半乳糖醛酸转运蛋白,发现来自黑曲霉的转运蛋白GatA对D-半乳糖醛酸转运能力更强,对提高黏酸的生产效率有重要的促进作用[43]。
与化学法相比,目前生物法催化D-半乳糖醛酸生产黏酸仍处于初步阶段,但生物法以可再生生物质为出发原料,遵循绿色可持续发展原则,契合国家新近提出的“碳中和”发展理念;此外,生物催化过程具有环境友好、反应条件温和、副产物少等优点,必将成为未来黏酸生产的一个重要研究方向。
| [1] |
A nu, Kumar A, Rapoport A, et al. Multifarious pretreatment strategies for the lignocellulosic substrates for the generation of renewable and sustainable biofuels: a review. Renew Energy, 2020, 160: 1228-1258. DOI:10.1016/j.renene.2020.07.031
|
| [2] |
Zhao Y, Lu KF, Xu H, et al. A critical review of recent advances in the production of furfural and 5-hydroxymethylfurfural from lignocellulosic biomass through homogeneous catalytic hydrothermal conversion- science direct. Renew Sust Energ Rev, 2021, 139: 110706. DOI:10.1016/j.rser.2021.110706
|
| [3] |
Jing YX, Guo Y, Xia QN, et al. Catalytic production of value-added chemicals and liquid fuels from lignocellulosic biomass. Chem, 2019, 5(10): 2520-2546. DOI:10.1016/j.chempr.2019.05.022
|
| [4] |
Walaszek Z, Szemraj J, Hanausek M, et al. D-glucaric acid content of various fruits and vegetables and cholesterol-lowering effects of dietary D-glucarate in the rat. Nutr Res, 1996, 16(4): 673-681. DOI:10.1016/0271-5317(96)00045-0
|
| [5] |
Bhattacharya S, Manna P, Gachhui R, et al. D-saccharic acid 1, 4-lactone protects diabetic rat kidney by ameliorating hyperglycemia-mediated oxidative stress and renal inflammatory cytokines via NF-κB and PKC signaling. Toxicol Appl Pharm, 2013, 267(1): 16-29. DOI:10.1016/j.taap.2012.12.005
|
| [6] |
Gupta KP, Singh J. Modulation of carcinogen metabolism and DNA interaction by calcium glucarate in mouse skin. Toxicol Sci, 2004, 79(1): 47-55. DOI:10.1093/toxsci/kfh098
|
| [7] |
Singh J, Gupta JK. Calcium glucarate prevents tumor formation in mouse skin. Biomed Environ Sci, 2003, 16(1): 9-16.
|
| [8] |
Hartner W, Narula J, Khaw BA. Attenuation of microvascular injury in preconditioned ischemic myocardium: imaging with tc-99m glucaric acid and in-111 human fibrinogen. Curr Mol Imaging, 2015, 4(1): 20-28. DOI:10.2174/2211555204666150402230538
|
| [9] |
Houson HA, Nkepang GN, Hedrick AF, et al. Imaging of isoproterenol-induced myocardial injury with F-18-labeled fluoroglucaric acid in a rat model. Nucl Med Biol, 2018, 59: 99-15.
|
| [10] |
Kruyer NS, Peralta-Yahya P. Metabolic engineering strategies to bio-adipic acid production. Curr Opin Biotechnol, 2017, 45: 136-143. DOI:10.1016/j.copbio.2017.03.006
|
| [11] |
Skoog E, Shin JH, Saez-Jimenez V, et al. Biobased adipic acid—the challenge of developing the production host. Biotech Adv, 2018, 36(8): 2248-2263. DOI:10.1016/j.biotechadv.2018.10.012
|
| [12] |
Li GH, Huang DX, Sui X, et al. Advances in microbial production of medium-chain dicarboxylic acids for nylon materials. React Chem Eng, 2020, 5(2): 221-238. DOI:10.1039/C9RE00338J
|
| [13] |
Werpy T, Petersen G. Top value added chemicals from biomass: volume Ⅰ—results of screening for potential candidates from sugars and synthesis gas. U.S. Department of Energy, 2004[EB/OL]. [2021-03-31] https://www.osti.gov/servlets/purl/15008859.
|
| [14] |
Qu YN, Yan HJ, Guo Q, et al. Biosynthesis of D-glucaric acid from sucrose with routed carbon distribution in metabolically engineered Escherichia coli. Metab Eng, 2018, 47: 393-400. DOI:10.1016/j.ymben.2018.04.020
|
| [15] |
Su HH, Guo ZW, Wu XL, et al. Efficient bioconversion of sucrose to high-value-added glucaric acid by in vitro metabolic engineering. Chem Sus Chem, 2019, 12(10): 2278-2285. DOI:10.1002/cssc.201900185
|
| [16] |
Kuivanen J, Biz A, Richard P. Microbial hexuronate catabolism in biotechnology. AMB Express, 2019, 9(1): 16. DOI:10.1186/s13568-019-0737-1
|
| [17] |
姜美云, 唐硕, 王婷, 等. 果胶多糖水热法降解及其产物体外抗氧化性评价. 食品科学, 2019, 40(12): 253-259. Jiang MY, Tang S, Wang T, et al. Degradation of pectic polysaccharide by hydrothermal treatment and antioxidant activity in vitro of the resulting products. Food Sci, 2019, 40(12): 253-259 (in Chinese). DOI:10.7506/spkx1002-6630-20180724-295 |
| [18] |
Schmitz K, Protzko P, Zhang LS, et al. Spotlight on fungal pectin utilization from phytopathogenicity to molecular recognition and industrial applications. Appl Microbiol Biotechnol, 2019, 103(6): 2507-2524. DOI:10.1007/s00253-019-09622-4
|
| [19] |
Gawkowska D, Cybulska J, Zdunek A. Structure-related gelling of pectins and linking with other natural compounds: a review. Polymers, 2018, 10(7): 762. DOI:10.3390/polym10070762
|
| [20] |
Wu P, Yang SH, Zhan ZC, et al. Origins and features of pectate lyases and their applications in industry. Appl Microbiol Biotech, 2020, 104(17): 7247-7260. DOI:10.1007/s00253-020-10769-8
|
| [21] |
Parmar I, Rupasinghe HPV. Bio-conversion of apple pomace into ethanol and acetic acid: enzymatic hydrolysis and fermentation. Bioresour Technol, 2013, 130: 613-620. DOI:10.1016/j.biortech.2012.12.084
|
| [22] |
Pelloux J, Rustérucci C, Mellerowicz EJ. New insights into pectin methylesterase structure and function. Trends Plant Sci, 2007, 12(6): 267-277. DOI:10.1016/j.tplants.2007.04.001
|
| [23] |
Rebello S, Anju M, Aneesh EM, et al. Recent advancements in the production and application of microbial pectinases: an overview. Rev Environ Sci Bio-Technol, 2017, 16(3): 381-394. DOI:10.1007/s11157-017-9437-y
|
| [24] |
Babbar N, Dejonghe W, Gatti M, et al. Pectic oligosaccharides from agricultural by-products: production, characterization and health benefits. Crit Rev Biotechnol, 2016, 36(4): 594-606. DOI:10.3109/07388551.2014.996732
|
| [25] |
Mao GZ, Wu DM, Wei CY, et al. Reconsidering conventional and innovative methods for pectin extraction from fruit and vegetable waste: targeting rhamnogalacturonan Ⅰ. Trends Food Sci. Technol, 2019, 94: 65-78.
|
| [26] |
Wang T, Jiang M, Tang S, et al. Preparation of di- and tri-galacturonic acid by coupling hydrothermal pretreatment and enzymatic hydrolysis. Process Biochem, 2021, 102: 180-185. DOI:10.1016/j.procbio.2021.01.002
|
| [27] |
Richard P, Hilditch S. D-galacturonic acid catabolism in microorganisms and its biotechnological relevance. Appl Microbiol Biotech, 2009, 82(4): 597-604. DOI:10.1007/s00253-009-1870-6
|
| [28] |
Nguyen TT, Fedorov AA, Williams L, et al. The mechanism of the reaction catalyzed by uronate isomerase illustrates how an isomerase may have evolved from a hydrolase within the amidohydrolase superfamily. Biochem, 2009, 48(37): 8879-8890. DOI:10.1021/bi901046x
|
| [29] |
Williams L, Nguyen T, Li YC, et al. Uronate isomerase: a nonhydrolytic member of the amidohydrolase superfamily with an ambivalent requirement for a divalent metal ion. Biochem, 2006, 45(24): 7453-7462. DOI:10.1021/bi060531l
|
| [30] |
Bouvier JT, Sernova NV, Ghasempur S, et al. Novel metabolic pathways and regulons for hexuronate utilization in proteobacteria. J Bacteriol, 2018, 201(1): e00431-18.
|
| [31] |
Bouvir JT, Groninger-poe FP, Vetting M, et al. Galactaro delta-lactone isomerase: lactone isomerization by a member of the amidohydrolase superfamily. Biochem, 2014, 53(4): 614-616. DOI:10.1021/bi5000492
|
| [32] |
Andberg M, Maaheimo H, Boer H, et al. Characterization of a novel Agrobacterium tumefaciens galactarolactone cycloisomerase enzyme for direct conversion of D-galactarolactone to 3-deoxy-2-keto-L- threo-hexarate. J Biol Chem, 2012, 287(21): 17662-17671. DOI:10.1074/jbc.M111.335240
|
| [33] |
Wagner G, Hollmann S. Uronic acid dehydrogenase from Pseudomonas syringae: purification and properties. Febs J, 1976, 61(2): 589-596.
|
| [34] |
Yoon SH, Moon TS, Iranpour P, et al. Cloning and characterization of uronate dehydrogenases from two Pseudomonads and Agrobacterium tumefaciens strain C58. J Bacteriol, 2009, 191(15): 1565-1573.
|
| [35] |
Pick A, Schmid J, Sieber V. Characterization of uronate dehydrogenases catalysing the initial step in an oxidative pathway. Microb Biotechnol, 2015, 8(4): 633-643. DOI:10.1111/1751-7915.12265
|
| [36] |
Hubbard BK, Koch M, Palmer DR, et al. Evolution of enzymatic activities in the enolase superfamily: characterization of the D-glucarate/galactarate catabolic pathway in Escherichia coli. Biochem, 1998, 37(41): 14369-14375. DOI:10.1021/bi981124f
|
| [37] |
Zhang H, Li X, Su X, et al. Production of adipic acid from sugar beet residue by combined biological and chemical catalysis. Chem Cat Chem, 2016, 8: 1500-1506.
|
| [38] |
Mojzita D, Wiebe M, Hilditch S, et al. Metabolic engineering of fungal strains for conversion of D-galacturonate to meso-galactarate. Appl Environ Microb, 2010, 76(1): 169-175. DOI:10.1128/AEM.02273-09
|
| [39] |
Kuivanen J, Wang YMJ, Richard P. Engineering Aspergillus niger for galactaric acid production: elimination of galactaric acid catabolism by using RNA sequencing and CRISPR/Cas9. Microb Cell Fact, 2016, 15: 210. DOI:10.1186/s12934-016-0613-5
|
| [40] |
Barth D, Wiebe MG. Enhancing fungal production of galactaricacid. Appl Microbiol Biotech, 2017, 101(10): 4033-4040. DOI:10.1007/s00253-017-8159-y
|
| [41] |
Paasikallio T, Huuskonen A, Wiebe MG. Scaling up and scaling down the production of galactaric acid from pectin using Trichoderma reesei. Microb Cell Fact, 2017, 16(1): 2-11. DOI:10.1186/s12934-016-0620-6
|
| [42] |
Vidgren V, Halinen S, Tamminen A, et al. Engineering marine fungi for conversion of D-galacturonic acid to mucic acid. Microb Cell Fact, 2020, 19(1): 156. DOI:10.1186/s12934-020-01411-3
|
| [43] |
Protzko RJ, Latimer LN, Martinho Z, et al. Engineering Saccharomyces cerevisiae for co-utilization of D-galacturonic acid and D-glucose from citrus peel waste. Nat Commun, 2018, 9(1): 5059. DOI:10.1038/s41467-018-07589-w
|
| [44] |
Sakuta R, Nakamura N. Production of hexaric acids from biomass. Int J Mol Sci, 2019, 20(15): 3660. DOI:10.3390/ijms20153660
|
| [45] |
Van Strien N, Rautiainen S, Asikainen M, et al. A unique pathway to platform chemicals: aldaric acids as stable intermediates for the synthesis of furandicarboxylic acid esters. Green Chem, 2020, 22(29): 8271-8277.
|
| [46] |
吴树丽, 刘启顺, 谭海东, 等. 5-羟甲基糠醛的生物催化氧化研究进展. 生物技术通报, 2016, 32: 50-58. Wu SL, Liu QS, Tan HD, et al. Research progress on biocatalytic oxidation of 5-hydroxymethylfurfural. Biotechnol Bull, 2016, 32: 50-58 (in Chinese). |
| [47] |
Amarasekara AS, Razzaq A, Bonham P. Synthesis and characterization of all renewable resources based branched polyester: poly(2, 5-furandicarboxylic acid-co-glycerol). ISRN Polym Sci, 2013, 645169.
|
| [48] |
Xie NZ, Liang H, Huang RB, et al. Biotechnological production of muconic acid: current status and future prospects. Biotechnol Adv, 2014, 32(3): 615-622. DOI:10.1016/j.biotechadv.2014.04.001
|
| [49] |
Li X, Wu D, Lu T, et al. Highly efficient chemical process to convert mucic acid into adipic acid and DFT studies of the mechanism of the rhenium-catalyzed deoxydehydration. Angew Chem Int Edit, 2014, 53(16): 4200-4204. DOI:10.1002/anie.201310991
|
| [50] |
Mehtiö T, Nurmi L, Rämö V, et al. Synthesis and characterization of copolyanhydrides of carbohydrate- based galactaric acid and adipic acid. Carbohyd Res, 2015, 402: 102-110. DOI:10.1016/j.carres.2014.07.009
|
| [51] |
Pan DW, Davis ME. Cationic mucic acid polymer-based siRNA delivery systems. Bioconjugate Chem, 2015, 26(8): 1791-1803. DOI:10.1021/acs.bioconjchem.5b00324
|
| [52] |
Gu L, Faig A, Abdelhamid D, et al. Sugar-based amphiphilic polymers for biomedical applications: from nanocarriers to therapeutics. Accounts Chem Res, 2014, 47(10): 2867-2877. DOI:10.1021/ar4003009
|
| [53] |
Wong KL, Law GL, Yang YY, et al. A highly porous luminescent terbium-organic framework for reversible anion sensing. Adv Mater, 2006, 181(8): 1051-1054.
|
| [54] |
Sakuta R, Takeda K, Igarashi K, et al. Pyrroloquinoline quinone-dependent glucose dehydrogenase anode: D-galacturonic acid oxidation and galactaric acid production. J Mol Catal B-Enzym, 2016, 133: 76-79. DOI:10.1016/j.molcatb.2016.11.021
|
 2022, Vol. 38
2022, Vol. 38