中国科学院微生物研究所、中国微生物学会主办
文章信息
- 黄丽晶, 马小涵, 李晨辉, 王红权
- HUANG Lijing, MA Xiaohan, LI Chenhui, WANG Hongquan
- IL-2修饰药物分子研发进展
- Advances of modified IL-2 molecules in drug development
- 生物工程学报, 2022, 38(9): 3279-3290
- Chinese Journal of Biotechnology, 2022, 38(9): 3279-3290
- 10.13345/j.cjb.210709
-
文章历史
- Received: September 13, 2021
- Accepted: March 22, 2022
- Published: March 31, 2022
2. 河北菲尼斯生物技术有限公司 石家庄自身免疫药物技术创新中心, 河北 石家庄 050035
2. Shijiazhuang Technology Innovation Centre of Autoimmune Disease Drug, Hebei Fitness Biotechnology Co., Ltd., Shijiazhuang 050035, Hebei, China
1984年,一位33岁黑色素瘤转移的病例在接受IL-2治疗3个月后肿瘤消退,此后病人无瘤生存29年。IL-2由此成为人类历史上第一个有效的肿瘤免疫疗法。遗憾的是,在肿瘤治疗中,IL-2治疗的客观缓解率只有约5%−10%,同时伴随致命性血管渗漏综合征等严重不良反应[1],大大限制了IL-2的临床应用。
随着对IL-2及其信号通路研究的深入,人们发现IL-2对免疫系统的作用具有两面性。高剂量IL-2通过结合效应T细胞表面的IL-2Rβγc,刺激效应T细胞增殖,达到治疗肿瘤的作用;但IL-2同时会刺激Treg细胞增殖,从而产生对细胞毒T细胞的抑制作用,降低肿瘤治疗效果。尤其低剂量IL-2,可以通过Treg表面组成型表达的IL-2Rαβγc,特异性刺激Treg增殖。目前,低剂量IL-2作为一种潜在的自身免疫病治疗方法,在多种自身免疫病的治疗中均处于临床研究阶段。
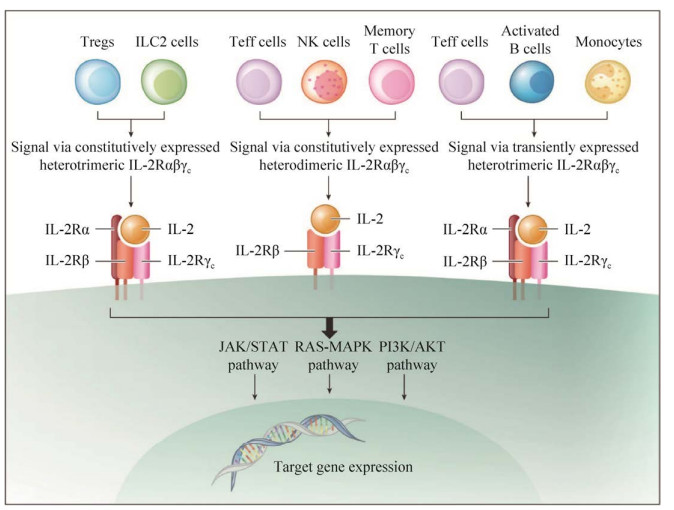
1 IL-2生物学功能及信号转导IL-2是第一个被克隆的细胞因子,因其功能曾被称为“T细胞生长因子”[2]。人IL-2成熟形式的分子量为15.5−16.0 kDa,主要由抗原活化的CD4+ T细胞分泌,其他免疫细胞,如CD8+ T细胞、自然杀伤(natural killer, NK)细胞以及活化的树突状细胞也可分泌IL-2分子。IL-2通过细胞表面的IL-2受体(IL-2Rs) 发挥作用,IL-2Rs包括单体、二聚体和三聚体3种不同形式。IL-2Rs单体即IL-2Rα (CD25),其与IL-2亲和力最弱(Kd꞊10–8 mol/L),IL-2与IL-2Rα的结合不启动信号转导[3],膜结合或游离的IL-2α可能发挥IL-2的清除剂或诱饵受体的作用;二聚体IL-2Rs由IL-2Rβ (CD122) 和IL-2Rγc (CD132) 组成,IL-2Rβγc与IL-2的亲和力中等(Kd≈10–9 mol/L);三聚体IL-2Rs由IL-2Rα、IL-2Rβ和IL-2Rγc组成,与IL-2的亲和力最强(Kd≈10–11 mol/L)。IL-2对免疫系统作用的两面性主要是通过不同细胞类型上所表达的不同受体介导的,如图 1所示,IL-2与IL-2Rβγc或IL-2Rαβγc结合后,启动信号转导。其信号转导过程主要通过3条通路完成:(1) Janus kinase (JAK)/STAT;(2) phosphoinositide 3-kinase (PI3K)/AKT;(3) MAPK信号通路。
|
| 图 1 IL-2信号转导通路[4] Fig. 1 IL-2 signaling pathway[4]. The duality effects of the IL-2 on the immune system is mediated by the spatiotemporal specificity of IL-2R expression. IL-2Rαβγc with the high-affinity to IL-2 is constitutively expressed on Tregs and ILC2 cells and transiently expressed on Teffs, activated B cells, and monocytes. IL-2Rβγc with the intermediate-affinity to IL-2 is constitutively expressed on Teffs, memory T cells, and NK cells. Low dose IL-2 preferentially binds to IL-2Rαβγc and activates Tregs and ILC2 cells, results in immunosuppression. High dose IL-2 by exogenous administration binds Teffs, memory T cells, and NK cellsresults in immune activation. IL-2 signaling activates the JAK/STAT, RAS-MAPK, and PI3K/AKT pathways, which modulate target gene expression and subsequently differentiation, proliferation, survival, and cellular function. Abbreviations: IL-2: interleukin-2; IL-2R: interleukin-2 receptor; ILC2: type-2 innate lymphoid cells; NK: natural killer; Teffs: effector T cells; Tregs: regulatory T cells. |
| |
IL-2在疾病治疗中的两面性,为IL-2的临床应用和分子设计打开了新的思路,IL-2再次成为肿瘤免疫和自身免疫病治疗的热门分子。但IL-2作为一种药物分子,体内半衰期只有13–85 min,需要每天或隔天给药,患者依从性差;另外,IL-2分子对免疫系统刺激具有两面性,高剂量IL-2刺激免疫反应,治疗肿瘤,但同时不可避免地会诱导Treg的升高,削弱药效,其对血管内皮细胞IL-2Rβγc的过度刺激还会引发毛细血管渗漏等严重不良反应,低剂量IL-2虽然安全性相对较好,但也需控制剂量,防止对效应T细胞的激活。因此,如何通过对IL-2进行工程化改造,最大化治疗效果,规避不良反应,成为了目前免疫治疗领域的研发热点之一。
IL-2体内半衰期短主要是因为其分子量小,在体内很容易被肾小球滤过作用清除。目前主要通过PEG修饰以及融合蛋白(HAS、抗体Fc、抗体融合等) 表达等方法提高分子的分子量,减少肾小球滤过作用,延长半衰期。对IL-2不良反应的控制主要通过PEG修饰带来的空间位阻效应和关键互作位点突变等方式,改变分子的受体偏好性来实现。偏向IL-2Rαβγc选择性刺激Treg细胞,用来治疗自身免疫病,偏向IL-2Rβγc选择性刺激效应T细胞用来治疗肿瘤。
2.1 肿瘤 2.1.1 PEG化IL-2激动剂蛋白质PEG修饰是延长蛋白药物体内半衰期的最常用手段,同时可提高蛋白亲水性,降低免疫原性。IL-2特定位点的PEG化还可以改变其受体偏向性。通过特定位点的PEG化使IL-2更倾向于结合IL-2Rβγc,在肿瘤微环境中更加特异地激活Teff,降低对Treg的活化能力,可最大化发挥IL-2的抗肿瘤的作用,并降低其毛细血管渗漏等副作用。
(1) Bempegaldesleukin:Bempegaldesleukin是Nektar公司和BMS公司共同开发的PEG化IL-2分子,由6个可释放PEG分子定点修饰到IL-2的K31、K34、K42、K47、K48和K75上[5],目前与Nivolumab联用在肌层浸润性膀胱癌、恶性黑色素瘤、肾细胞癌3个适应证上处于Ⅲ期临床研究阶段,是目前研发进度最快的PEG修饰IL-2分子。Bempegaldesleukin属于一种前药分子,进入体内后,随着PEG分子的释放发挥其功能。与天然IL-2相比,PEG化IL-2分子优先与NK细胞和Teff细胞表面的IL-2Rβγc结合,相反,与Treg表面IL-2Rαβγc结合减弱,从而实现对Teff和NK细胞的特异活化[5-6]。Bempegaldesleukin的人体半衰期为15.5 h,暴露量较7倍剂量IL-2提高500倍以上。其前药设计可以在活性分子远低于血浆毒性剂量的情况下,大幅提高药物暴露,降低药物毒性,提高药效[5]。
在临床前研究中,Bempegaldesleukin通过诱导瘤内效应细胞Treff和NK的增殖和活化显著诱导黑色素瘤模型小鼠体内肿瘤的消退,值得注意的是,Bempegaldesleukin并未扩增瘤内Treg,给药7 d后,瘤内CD8︰Treg比例较IL-2明显提高。在人体临床研究中,同样观察到Bempegaldesleukin可以显著诱导外周及瘤内CD8+ T细胞的增殖和功能,且未观察到高剂量IL-2在恶性肿瘤治疗中常见的严重不良反应[5]。
Bempegaldesleukin在临床研究中的推荐剂量为0.006 mg/kg,联合360 mg Nivolumab,每3周给药一次。在一项作为恶性黑色素瘤一线治疗的Ⅱ期临床研究中,经过29个月的随访,该剂量Bempegaldesleukin显示出良好的耐受性,客观缓解率(objective response rate, ORR) 达到52.6% (n=20/38),完全缓解率(complete respons, CR) 为34.2% (n=13/38),肿瘤负荷与基线相比下降了78.5%,中位无进展生存期(progression-free survival, PFS) 为30.9个月[7]。较Nivolumab关键Ⅲ期临床CheckMate 067结果:ORR 44%,CR 9%,肿瘤负荷下降34.5%,PFS 6.9个月均有明显提高[8]。与高剂量IL-2相比,Bempegaldesleukin给药更加方便,依从性更好,且有效率更高,与Nivolumab联用,效果明显优于Nivolumab。值得注意的是,临床研究显示,Bempegaldesleukin在黑色素瘤、尿路上皮癌等瘤种中的作用与PD-L1的表达不相关。而且,与Nivolumab联用,Bempegaldesleukin可以诱导相当比例(n=7/10) 肿瘤从PD-L1阴性向PD-L1阳性转变。该特点对于尿路上皮癌等瘤种十分重要,因为这些肿瘤PD-L1的低表达不能使用免疫检查点抑制剂治疗[9]。
(2) THOR-707是由Synthorx公司开发的“not-α ”单PEG定点修饰IL-2分子。通过天然IL-2结构中融入非天然氨基酸,实现定点PEG化,THOR-707对IL-2Rβγc复合物具有亲和力,但不与IL-2Rα链结合[10]。为了进一步拓展肿瘤学市场,赛诺菲2019年底斥资25亿美元收购Synthorx公司,获得了THOR-707。Ⅰ/Ⅱ中期临床结果显示,患者在首次使用THOR-707后体内CD8+ T细胞和NK细胞数量增加,有明显剂量关系,并且可持续整个给药周期[11];与K药(pembrolizumab) 联合使用时,这种效应更加明显,且未观察到CD4+调节性T细胞或嗜酸性粒细胞显著增加,表明THOR-707对IL-2Rα受体没有选择性。安全性方面,单药最高剂量24 μg/kg,联合用药最高剂量为16 μg/kg,未观察到剂量限制性毒性[12]。
(3) TransCon IL-2 β/γ是由Ascendis Pharma公司开发的一款IL-2类似物。其通过在IL-2分子的IL-2Rα结合区引入一个Cys突变,进行定点PEG (5 kDa) 修饰,将其改造为一个非α结合分子,再通过一个TransCon linker将修饰分子连接到TransCon载体上,形成一个前药分子,在生理条件下,TransCon linker裂解,释放出PEG-IL-2分子,发挥药效。TransCon IL-2 β/γ在小鼠体内半衰期为22 h,在猴子体内半衰期约为32 h,优于上述Bempegaldesleukin (小鼠和猴子体内半衰期均为20 h) 和THOR-707 (小鼠13.3 h;猴子11 h) [13]。目前该项目处于临床前研究开发阶段。
(4) SHR-1916是恒瑞医药自主研发的全新基于定点突变的IL-2 PEG分子,详细信息未披露。目前处于Ⅰ期临床阶段。
2.1.2 IL-2融合蛋白(1) ALKS-4230。IL2和IL2Rα胞外域融合蛋白,在体内不与IL2Rα结合,而更倾向于结合IL-2Rβγc。目前处于Ⅱ期临床研究阶段。临床前研究表明,ALKS-4230可以刺激NK细胞和CD8+ T细胞的增殖,并诱导TNF-α、IL-6和IFN-γ等炎症因子的升高。对小鼠肺癌模型B16F10、ALKS-4230表现出明显的抗肿瘤活性。ALKS-4230体内半衰期较IL-2提高了3−4倍[14]。ARTISTRY-1研究了ALKS-4230单药及pembrolizumab联用在晚期实体瘤的药效和安全性。ALKS-4230单药以及与pembrolizumab联用均表现出一定的获益和良好的耐受性[15]。
(2) CUE-101。CUE-101是一种融合蛋白,由HLA-A*0201、HPV16 E7抗原肽(11−20个氨基酸) 一个亲和力减弱IL-2 (F42A和H16A突变,分别降低了IL-2分子和IL-2Rα以及IL-2Rβ的亲和力),以及一个IgG1的Fc结构域融合而成。CUE-101可以特异性结合和激活HPV-16抗原特异性CD8+ T细胞,以清除HPV16驱动的肿瘤细胞[16],目前处于Ⅰ期临床研究阶段。
2.1.3 IL-2抗体融合蛋白(1) Darleukin和NidlegyTM。Darleukin (L19IL2) 是靶向肿瘤的免疫刺激分子,由人L19抗体(靶向纤连蛋白EDB域) 和人IL2融合而成。Darleukin通过激活病变区域的肿瘤特异T细胞和NK细胞杀伤肿瘤细胞,单用或与其他药物联用,具有很强的抗肿瘤活性[17-18]。目前与立体定向消融放射治疗和PD-1抗体联合使用用于恶性非小细胞肺癌的制剂,处于临床Ⅱ期研究阶段。Darleukin与另一个抗体融合分子Fibromun (TNF与IL19抗体融合蛋白) 组成组合制剂(商品名NidlegyTM,曾用名Daromun)。在同系免疫重建小鼠荷瘤模型中,瘤内注射NidlegyTM可以实现肿瘤完全缓解,而Darleukin和Fibromun单药都没有这种效果。在无法切除的恶性黑色素瘤Ⅱ期临床研究中,瘤内注射NidlegyTM使20个病例的32个肿瘤显现出完全缓解,其他未注射肿瘤也有54%表现出完全缓解,说明NidlegyTM可以激活系统性免疫反应[18]。针对ⅢB/C黑色素瘤的Ⅲ期临床研究neo- DREAM目前正在进行中[19]。
(2) APN-301。由IL-2和抗GD2单克隆抗体共价结合组成的。动物研究表明其对黑色素瘤和神经母细胞瘤具有抑制作用[20-21]。已经完成的Ⅱ期临床研究表明,APN-301只对早期较小疾病负担的复发/难治神经母细胞瘤病例(131I-MIBG显像和/或骨髓病理确诊) 作用更加明显,而对标准诊断指标确诊的病例无作用。单药的完全缓解率为21.7% (n=5/23),响应时间长达35个月[22]。与GM-CSF和异维A酸联用的客观缓解率为16%[23]。在接受APN-301治疗的难治复发Ⅲ/Ⅳ期黑色素瘤病例中,33% (n= 6/18) 的病例到研究完成仍未见复发,2年无复发比例和客观存活率分别为39%和65%。所有研究中APN-301安全性均可接受[24]。
(3) RG-7461。由靶向肿瘤相关成纤维细胞的单克隆抗体(抗FAB单抗) 和非IL-2Rα结合IL-2分子融合表达而成,可以诱导瘤内CD8+ T细胞和NK细胞的积累,降低Treg活性。Ⅰ期临床研究中,RG-7461可诱导外周血和肿瘤内的效应T细胞和NK细胞的快速增殖,3位恶性实体瘤患者的长期客观响应时间超过6个月[25]。RG-7461与其他抗肿瘤药物联用的多个Ⅱ期临床研究目前正在进行中。
(4) 阿姆白介素-2-瑟妥珠单抗(cergutuzumab amunaleukin)。是抗癌胚抗原(anti-carcinoembryonic antigen, CEA) 抗体偶联IL-2表达而成,其中IL-2有3个位点突变,降低和IL-2Rα结合。CEA是在特定实体肿瘤,包括结直肠癌(95%)、胰腺癌(90%)、胃癌(80%)、非小细胞肺癌(60%) 以及乳腺癌(40%) 等细胞上特异高表达的糖蛋白。Cergutuzumab amunaleukin一方面可以靶向肿瘤细胞,另一方面也可以延长IL2的半衰期。在人CEA转基因C57BL/6模型上,Cergutuzumab amunaleukin可以显著诱导肿瘤和外周血中的NK和CD8+ T细胞的增殖。在MC38-CEA和PancO2-CEA同源小鼠模型中,Cergutuzumab amunaleukin可以提高小鼠存活率,且不会影响Treg的水平[26]。目前瘤内注射,单药或联合PD-L1单抗atezolizumab治疗晚期/恶性实体瘤的处于Ⅰ期临床研究中。
2.2 自身免疫疾病与高剂量IL2的免疫刺激作用治疗肿瘤不同,低剂量IL2特异作用于Treg表面的高亲和力IL2Rαβγc,提高了Treg的数量和活性,增强其免疫抑制作用,可以用来治疗系统性红斑狼疮等自身免疫疾病。
2016年,栗占国教授团队首次在概念临床上证明了低剂量IL-2针对中重度系统性红斑狼疮患者的疗效以及其作用机制,临床应答率(系统性红斑狼疮反应指数SRI-4) 可达89.5%,用药12周后,91.9%患者的泼尼松龙减量超过25%,67.6%患者泼尼松龙减量超过50%。另外,通过对患者外周血淋巴细胞分型进行检测发现,低剂量IL-2可明显诱导外周血Treg水平,抑制Th17和Tfh细胞水平,Th1和Th2水平变化不明显,与动物模型研究结果类似。与传统的免疫治疗相比,这项低剂量IL-2治疗并未增加感染的风险[27]。随后发表随机、双盲、对照临床研究证明,低剂量IL-2治疗中重度系统性红斑狼疮安全有效。结果显示低剂量IL-2组明显优于对照组,24周IL-2组的该指数为65.52%。低剂量IL-2组患者的耐受性好,感染发生率(6.9%) 明显低于对照组(20.0%)。在免疫指标方面,给予低剂量IL-2治疗后,患者体内的调节性T细胞水平升高,而致病性细胞和因子水平降低,可能说明通过靶向调控IL-2受体改善了患者体内的免疫失衡。同时,低剂量IL-2组患者体内NK细胞水平升高,可能与感染较少发生有关[28]。另外,低剂量IL-2在类风湿关节炎、强直性脊柱炎、Ⅰ型糖尿病、自身免疫性肝炎等自身免疫疾病治疗上也表现出一定的作用[29]。
低剂量IL-2虽然安全性相对较高,不会产生血管漏综合征(vascular leak syndrome, VLS) 等严重不良反应,但如何使之更特异地作用于Treg,避免效应T细胞的刺激,最大程度提高药效、避免不良反应的发生,也是在研究中需要解决的重要问题。
2.2.1 PEG化IL-2与肿瘤药物开发不同,针对自身免疫病的PEG化IL2需要借助PEG分子屏蔽IL-2与IL-2Rβγc的结合位点,使之更加倾向于结合IL-2Rαβγc。
(1) NKTR-358。由Nektar公司开发,2017年礼来公司斥资4亿美元共同开发,目前处于Ⅱ期临床研究阶段。NKTR-358为多种PEG修饰IL-2的混合物,其中双PEG修饰和三PEG修饰分子总占比超80%。主要的修饰位点为K7/8、K31、K34、K42、K47[30]。与IL-2相比,NKTR-358降低了IL-2Rβ的亲和力,使之更加偏向Treg细胞表面的IL-2Rαβγc,特异性刺激Treg水平的升高。小鼠研究表明,单次皮下注射NTKR-358即可强烈诱导外周血Treg细胞增殖,效果优于多次(1次/d,连续5 d) 给药的IL-2。多种Treg的生物标志物都显著诱导,而其他细胞如CD8+ T诱导不明显。IL-2或NTKR-358处理健康人外周血PBMC,利用CyTOF (质谱流式细胞术) 检测,NTKR-358更加特异刺激Treg,对CD8+ T、Tcon和NK细胞刺激不明显[31]。SLE病人体内Ⅰ期临床研究显示,NTKR-358的Cmax和AUC表现出剂量依赖。给药4–6 d达峰,清除半衰期约8–9 d。在最高剂量(28 μg/kg) 下,CD25高表达Treg数量较给药前提高17倍;Treg最高水平出现在10–12 d,其升高可维持20–25 d;在大于13.5 μg/kg剂量下,可观察到ICOS和CTLA-4表达的升高;Foxp3基因甲基化水平的变化与Treg数量结果一致,IDO-1和CD38基因表达水平均和剂量呈相关性。各剂量下,Tcon细胞水平无变化,NK细胞水平仅在高剂量下有轻微升高[32]。目前NKTR-358在SLE适应证上处于Ⅱ期临床研究阶段,在银屑病和特应性皮炎适应症上处于Ⅰ期临床研究阶段。
(2) THOR-809。由Synthorx公司开发,与THOR-707同属拓展密码子平台。在IL-2引入非天然氨基酸后进行定点PEG修饰,与THOR- 707不同的是,THOR-809对IL-2Rαβγc选择性提高。在小鼠和猴体内研究中,THOR-809特异诱导Treg细胞的增殖和活化,在猴体内半衰期约为17.2–18.0 h[33]。2019年底Synthorx被Sanofi收购后,未见THOR-809披露新的研究数据。
(3) Dual-31/51-20K。Dual-31/51-20K是由北京大学药学院的周德敏教授与北京协和医学院张烜教授团队联合开发的双PEG定点修饰IL-2分子。通过周教授团队的非天然氨基酸编码系统,对IL-2分子进行突变,在Y31和T51两个位点引入两个非天然氨基酸,随后在这两个位点上进行定点修饰,PEG分子量为20 K。研究发现,Y31和T51两个位点修饰后可抑制IL-2R介导的内吞作用,延长修饰分子的半衰期,小鼠皮下注射,Dual-31/51-20K分子半衰期为23.1 h。体外细胞研究中,Dual-31/51-20K可特异刺激Treg增殖,模型动物数据结果表明,Dual-31/51-20K可显著降低类风湿关节炎、系统性红斑狼疮及移植物抗宿主病小鼠模型的疾病活动度,且不影响模型动物的抗感染能力[34]。目前该分子已申报专利。
(4) RS2102。RS2102是由恒瑞全资子公司瑞石生物开发的1类生物制品。RS2102通过将N88突变成R,降低了IL-2对IL-2Rβγc的亲和力,提高了对IL-2Rαβγc的选择性,再通过PEG化延长分子半衰期。给药频率预计可以达到2周给药一次。该分子已于2021年10月份申报临床试验。
(5) FNS036。河北菲尼斯生物开发的PEG定点修饰IL-2分子。Cys125位于IL-2和IL-2Rγc结合面上,通过Cys125定点修饰,降低IL-2和IL-2Rγc的亲和力,提高分子对IL-2Rαβγc的选择性。动物研究表明,其可特异诱导Treg水平的升高。目前该分子处于临床前开发阶段。
2.2.2 IL-2融合蛋白(1) AMG592。是由Amgen公司开发的Fc融合IL-2突变体蛋白分子。IL-2突变可提高对IL-2Rα的选择性,Fc融合延长分子半衰期。hPBMC实验结果表明,AMG592较IL-2更加特异刺激Treg (pSTAT5),减少促炎性细胞因子的产生。食蟹猴研究结果,IL-2在诱导FoxP3+ Treg增殖的同时,会引起体温和CRP水平升高,而AMG592未出现以上副作用。在Ⅰ期临床研究中,AMG592耐受性良好,无严重副作用。最常见不良反应是注射部位红肿、疼痛,结束治疗后缓解。AMG592所有剂量都可以引起Treg︰Tcon的升高,在最高剂量下,Treg︰Tcon在第8天达到最高(基线水平4倍),可维持29 d。AMG592介导Treg特异升高,NK无明显升高,Tcon只有微弱升高,血清IL-6、TNFα或IFN-γ无明显升高[35]。AMG592对红斑狼疮的治疗目前处于Ⅱ临床研究阶段。
(2) PT101。也是Fc融合IL-2突变体蛋白分子,由Pandion Therapeutics公司开发,目前被Merck收购。于2021年1月完成Ⅰ期临床。单次皮下注射1–10 mg,观察28 d,耐受性良好,未观察到严重副作用。生物标志物方面,3.5 mg剂量下对Treg的刺激作用最强,总Treg升高3.6倍,CD25highTreg升高72.5倍。Pandion Therapeutics公司计划在今年下半年开展炎性肠炎和系统性红斑狼疮Ⅱ期临床研究[36]。
(3) CC92252 (DEL-106)。最初由Delinia公司开发,现在归Bristol-Myers Squibb所有。CC92252也是一个Fc融合突变IL-2分子,适应症是银屑病,目前处于Ⅰ期临床招募阶段。
(4) RG-7835。RG-7835是一个IgG融合IL-2突变(N88D) 分子。其中N88D突变可以降低分子与IL-2Rβ的亲和力。RG-7835可以特异刺激人源化小鼠体内Treg升高,而IgG融合野生型IL-2分子在刺激Treg的同时,还会刺激NK细胞的增殖。食蟹猴体内,单剂量(100 μg/kg) 可以使Treg水平提高14倍[37]。目前RG-7835已完成健康人体内的Ⅰa临床研究,正在进行炎性肠病病人体内的Ⅰb临床研究。
(5) IL233。由Slate Bio公司开发,目前处于临床前研究阶段。IL233是由IL-2和IL-33分子C末端(aa109–aa266) 融合而成[38]。动物研究显示,IL233在诱导Treg增殖和活化的能力上较IL-2或IL-33单药都明显提高,对狼疮肾炎、阿霉素诱导肾炎以及aGVHD都具有保护或治疗作用[38-40]。目前IL233处于临床前研究阶段。
3 问题与展望IL-2上市之后,因为治疗窗太窄,应用受到很大限制。如今随着免疫学的进步,多种工程化IL-2药物正在接受临床研究的检验,同时更多的分子正在进入临床前研究,见表 1。
| Modification type | Agent | Company | Molecular composition | Indication | Development stage |
| PEG modified IL-2 | Bempegaldesleukin (NKTR-214) | Nektar Therapeutics, Bristol myers squibb | 6 releasable PEG modified IL-2 | Melanoma, RCC, UC | Ⅲ |
| THOR-707 (SAR444245) | Sanofi | MonoPEG site-specific modified IL-2v | Solid tumor | Ⅰ/Ⅱ | |
| SHR-1916 | Hengrui Pharmaceuticals | MonoPEG site-specific modified IL-2v | Solid tumor | Ⅰ | |
| TransCon IL-2β/γ | Ascendis pharma | MonoPEG site-specific modified IL-2v | Solid tumor | Pre-clin | |
| NKTR-358 | Nektar Therapeutics, Lilly | Multi-PEG modified IL-2 | SLE, IBD | Ⅱ | |
| RS2012 | Reistone Biopharma | MonoPEG site-specific modified IL-2v | SLE | Ⅰ | |
| THOR-809 | Sanofi | MonoPEG site-specific modified IL-2v | AID | Ⅰ | |
| 31/51-20K | Peking University/Peking Union Medical College | Double PEG site -specific modified IL-2v | AID | Pre-clin | |
| IL-2 fusion protein | Nemvaleukin alfa (Alks-4230) | Alkermes | IL-2/IL-2Ra fusion protein | Melanoma | Ⅱ |
| Darleukin | Philogen | Anti-EDB mAb (L19)/IL-2v fusion protein | Melanoma, NSCLC, DLBCL | Ⅱ | |
| APN-301 | Merck KGaA, Apeiron Biologics AG | Anti-GD2 mAb/IL-2v fusion protein | Melanoma, Neuroblastoma | Ⅱ | |
| RG-6279 | Roche | Anti- PD1 mAb/IL-2v fusion protein | Solid tumor | Ⅰ | |
| CUE-101 | Cue Biopharma | E7-pHLA-IL-2v-Fc fusion protein | HNSCC | Ⅰ | |
| RG-7461 | Roche | Anti-FAP mAb/IL-2v fusion protein | Solid tumor | Ⅰ | |
| Cergutuzumab amunaleukin | Roche | Anti-CEA mAb/IL-2v fusion protein | Solid tumor | Ⅰ | |
| KY1043 | Kymab | Anti-PDL1 mAb/IL-2v fusion protein | Solid tumor | Pre-clin | |
| Efavaleukin alfa (AMG-592) | Amgen | IL-2v/Fc fusion protein | SLE | Ⅱ | |
| CC92252 | Bristol myers squibb | IL 2v/Fc fusion protein | PS | Ⅰ | |
| RG-7835 | Roche | IL-2v/IgG1 fusion protein | AID | Ⅰ | |
| PT101 | Pandion Therapeutics | IL-2v/Fc fusion protein | IBD, SLE | Ⅰ | |
| IL233 | Slate Bio | IL2/IL33 fusion protein | cGVHD | Pre-clin | |
| AID: autoimmune disease; CEA: carcinoembryonic antigen; DLBCL: diffuse large B cell lymphoma; EDB: extra domain B; GVHD: graft-versus-host disease; HNSCC: head and neck squamous cell carcinoma; IBD: inflammatory bowel disease; IL-2: interleukin-2; IL-2v: interleukin-2 variant; NSCLC: non-small cell lung cancer; PD-l: programmed cell death protein-l; PD-L1: programmed death ligand-1; PS: psoriasis; RCC: renal cell carcinoma; SLE: systemic lupus erythematosus; UC: urothelial carcinoma; | |||||
在肿瘤治疗领域,人们主要关注重点是修饰后分子的药物代谢动力学的改善,降低药物副作用和给药频率,降低药物对Treg活化的同时提高对Teff和NK细胞的激活能力,以及和免疫检查点抑制剂联用的疗效等。未来的基础和临床研究的工作将主要集中在以下重要问题上:降低或彻底消除IL-2Rα亲和力对抗肿瘤药效的影响;IL-2修饰分子免疫原性如何;IL-2修饰分子的抗肿瘤谱较IL-2有什么变化,特别是和免疫检查点联用的情况下;除免疫检查点抑制剂外,IL-2修饰分子还有其他更优组合吗,如CAR-T、TCR-T和CAR-NK疗法等。
在自身免疫病领域中,IL-2修饰的目标主要是改善给药便利性和耐受性,并通过Treg和Teff选择性的差异,达到治疗疾病的目的。未来的工作将集中在给药剂量和频次的探索;生物标志物的探索;长期给药时免疫原性对药效的影响;感染和肿瘤风险的控制;以及与其他疗法的联用方式的探索等。
除了本文介绍的IL-2工程化修饰分子外,近年来人们也开始开发IL-2变体分子,来克服天然IL-2的一些问题,如Neoleukin Therapeutics的NL-201,即基于IL-2和IL-15序列,通过计算机设计出来的新分子,它比IL-2分子短25%,与IL-2序列同源性只有14%[41]。研究显示,其只结合IL-2Rβγc,该项目目前处于Ⅰ期临床研究阶段,用于治疗恶性实体瘤[42]。类似分子还有Synthekine公司的STK-012以及BioNTech的BNT151等,这些项目都还处于早期研究阶段[43]。
IL-2相关药物研发的复兴,是基础研究推动药物工业发展的典型案例。相信未来随着基础和临床研究的进展,IL-2分子在肿瘤、自身免疫病甚至其他新的疾病领域的应用将越来越广泛,为人类提供应对免疫相关疾病的有力武器。
| [1] |
Rosenberg SA. IL-2: the first effective immunotherapy for human cancer. J Immunol, 2014, 192(12): 5451-5458. DOI:10.4049/jimmunol.1490019
|
| [2] |
Taniguchi T, Matsui H, Fujita T, et al. Structure and expression of a cloned cDNA for human interleukin-2. Nature, 1983, 302(5906): 305-310. DOI:10.1038/302305a0
|
| [3] |
Taniguchi T, Minami Y. The IL-2/IL-2 receptor system: a current overview. Cell, 1993, 73(1): 5-8. DOI:10.1016/0092-8674(93)90152-G
|
| [4] |
Overwijk WW, Tagliaferri MA, Zalevsky J. Engineering IL-2 to give new life to T cell immunotherapy. Annu Rev Med, 2021, 72: 281-311. DOI:10.1146/annurev-med-073118-011031
|
| [5] |
Charych DH, Hoch U, Langowski JL, et al. NKTR-214, an engineered cytokine with biased IL2 receptor binding, increased tumor exposure, and marked efficacy in mouse tumor models. Clin Cancer Res, 2016, 22(3): 680-690. DOI:10.1158/1078-0432.CCR-15-1631
|
| [6] |
Charych D, Khalili S, Dixit V, et al. Modeling the receptor pharmacology, pharmacokinetics, and pharmacodynamics of NKTR-214, a kinetically- controlled interleukin-2 (IL2) receptor agonist for cancer immunotherapy. PLoS One, 2017, 12(7): e0179431. DOI:10.1371/journal.pone.0179431
|
| [7] |
Diab A, Tykodi SS, Daniels GA, et al. Bempegaldesleukin plus nivolumab in first-line metastatic melanoma. J Clin Oncol, 2021, 39(26): 2914-2925. DOI:10.1200/JCO.21.00675
|
| [8] |
Larkin J, Chiarion-Sileni V, Gonzalez R, et al. Combined nivolumab and ipilimumab or monotherapy in untreated melanoma. N Engl J Med, 2015, 373(1): 23-34. DOI:10.1056/NEJMoa1504030
|
| [9] |
Siefker-Radtke AO, Fishman MN, Balar AV, et al. NKTR-214 + nivolumab in first-line advanced/ metastatic urothelial carcinoma (mUC): updated results from PIVOT-02. J Clin Oncol, 2019, 37(7_suppl): 388. DOI:10.1200/JCO.2019.37.7_suppl.388
|
| [10] |
Milla ME, Ptacin JL, Ma L, et al. THOR-707, a novel not-alpha IL-2, promotes all key immune system anti-tumoral actions of IL-2 without eliciting vascular leak syndrome (VLS). Ann Oncol, 2019, 30: v501.
|
| [11] |
Janku F, Abdul-Karim R, Azad A, et al. Preliminary results from an open-label, multicenter phase 1/2 dose escalation and expansion study of THOR-707, a novel not-Alpha IL-2, as a single agent in adult subjects with advanced or metastatic solid tumors. Eur J Cancer, 2020, 138: S11.
|
| [12] |
Joseph IB, Ma LN, Ptacin JL, et al. Abstract 3258: THOR-707, a novel not-alpha IL-2, elicits durable pharmacodynamic responses in non-human primates and efficacy as single agent and in combination with anti PD-1 in multiple syngeneic mouse modelsImmunology. American Association for Cancer Research, 2019, 3258.
|
| [13] |
Rosen DB, Laufer B, Knappe T, et al. Abstract 4507: TransConTM IL-2 β/γ: a novel long-acting prodrug of receptor-biased IL-2 designed for improved pharmocokinetics and optimal activation of T cells for the treatment of cancerImmunology. American Association for Cancer Research, 2020, 4507.
|
| [14] |
Lopes JE, Fisher JL, Flick HL, et al. ALKS 4230: a novel engineered IL-2 fusion protein with an improved cellular selectivity profile for cancer immunotherapy. J Immunother Cancer, 2020, 8(1): e000673. DOI:10.1136/jitc-2020-000673
|
| [15] |
Vaishampayan UN, Muzaffar J, Velcheti V, et al. 1027MO ALKS 4230 monotherapy and in combination with pembrolizumab (pembro) in patients (pts) with refractory solid tumours (ARTISTRY-1). Ann Oncol, 2020, 31: S708-S709.
|
| [16] |
Quayle SN, Girgis N, Thapa DR, et al. CUE-101, a novel E7-pHLA-IL2-fc fusion protein, enhances tumor antigen-specific T-cell activation for the treatment of HPV16-driven malignancies. Clin Cancer Res, 2020, 26(8): 1953-1964. DOI:10.1158/1078-0432.CCR-19-3354
|
| [17] |
Ongaro T, Gouyou B, Stringhini M, et al. A novel format for recombinant antibody-interleukin-2 fusion proteins exhibits superior tumor-targeting properties in vivo. Oncotarget, 2020, 11(41): 3698-3711. DOI:10.18632/oncotarget.27726
|
| [18] |
Weide B, Eigentler T, Catania C, et al. A phase Ⅱ study of the L19IL2 immunocytokine in combination with dacarbazine in advanced metastatic melanoma patients. Cancer Immunol Immunother, 2019, 68(9): 1547-1559. DOI:10.1007/s00262-019-02383-z
|
| [19] |
Philogen innovating targeting pipeline: nidlegy TM [EB/OL]. [2022-03-03]. https://www.philogen.com/pipeline/nidlegytm/.
|
| [20] |
Becker JC, Pancook JD, Gillies SD, et al. T cell-mediated eradication of murine metastatic melanoma induced by targeted interleukin 2 therapy. J Exp Med, 1996, 183(5): 2361-2366. DOI:10.1084/jem.183.5.2361
|
| [21] |
Sabzevari H, Gillies SD, Mueller BM, et al. A recombinant antibody-interleukin 2 fusion protein suppresses growth of hepatic human neuroblastoma metastases in severe combined immunodeficiency mice. PNAS, 1994, 91(20): 9626-9630. DOI:10.1073/pnas.91.20.9626
|
| [22] |
Shusterman S, London WB, Gillies SD, et al. Antitumor activity of Hu14. 18-IL2 in patients with relapsed/refractory neuroblastoma: a Children's Oncology Group (COG) phase Ⅱ study. J Clin Oncol, 2010, 28(33): 4969-4975.
|
| [23] |
Shusterman S, Naranjo A, Van Ryn C, et al. Antitumor activity and tolerability of Hu14. 18-IL2 with GMCSF and isotretinoin in recurrent or refractory neuroblastoma: a children's oncology group phase Ⅱ study. Clin Cancer Res, 2019, 25(20): 6044-6051.
|
| [24] |
Albertini MR, Yang RK, Ranheim EA, et al. Pilot trial of the Hu14. 18-IL2 immunocytokine in patients with completely resectable recurrent stage Ⅲ or stage Ⅳ melanoma. Cancer Immunol Immunother, 2018, 67(10): 1647-1658.
|
| [25] |
Soerensen MM, Ros W, Rodriguez-Ruiz ME, et al. Safety, PK/PD, and anti-tumor activity of RO6874281, an engineered variant of interleukin-2 (IL-2v) targeted to tumor-associated fibroblasts via binding to fibroblast activation protein (FAP). J Clin Oncol, 2018, 36(15_suppl): e15155. DOI:10.1200/JCO.2018.36.15_suppl.e15155
|
| [26] |
Klein C, Waldhauer I, Nicolini VG, et al. Cergutuzumab amunaleukin (CEA-IL2v), a CEA- targeted IL-2 variant-based immunocytokine for combination cancer immunotherapy: overcoming limitations of aldesleukin and conventional IL-2-based immunocytokines. Oncoimmunology, 2017, 6(3): e1277306. DOI:10.1080/2162402X.2016.1277306
|
| [27] |
He J, Zhang X, Wei YB, et al. Low-dose interleukin-2 treatment selectively modulates CD4+ T cell subsets in patients with systemic lupus erythematosus. Nat Med, 2016, 22(9): 991-993. DOI:10.1038/nm.4148
|
| [28] |
He J, Zhang RJ, Shao M, et al. Efficacy and safety of low-dose IL-2 in the treatment of systemic lupus erythematosus: a randomised, double-blind, placebo-controlled trial. Ann Rheum Dis, 2020, 79(1): 141-149. DOI:10.1136/annrheumdis-2019-215396
|
| [29] |
Rosenzwajg M, Lorenzon R, Cacoub P, et al. Immunological and clinical effects of low-dose interleukin-2 across 11 autoimmune diseases in a single, open clinical trial. Ann Rheum Dis, 2019, 78(2): 209-217. DOI:10.1136/annrheumdis-2018-214229
|
| [30] |
Kirk P, Langowski J, Zalevsky J. Selective Treg stimulator RUR20kD-IL-2 and related compositions: PCT/US2019/033100. 2019-05-20.
|
| [31] |
Dixit N, Fanton C, Langowski JL, et al. NKTR-358: a novel regulatory T-cell stimulator that selectively stimulates expansion and suppressive function of regulatory T cells for the treatment of autoimmune and inflammatory diseases. J Transl Autoimmun, 2021, 4: 100103. DOI:10.1016/j.jtauto.2021.100103
|
| [32] |
Fanton C, Siddhanti S, Dixit N, et al. op0195 selective expansion of regulatory t-cells in humans by a novel il-2 conjugate treg stimulator, nktr-358, being developed for the treatment of autoimmune diseasesOral presentations. BMJ Publishing Group Ltd and European League Against Rheumatism, 2019.
|
| [33] |
Ptacin J, Caffaro CE, Ma L, et al. THOR-809: an IL-2 engineered from an expanded genetic alphabet for the potential treatment of autoimmune disorders. Poster 86 presented at the ACR/ARP Annual Meeting, Nov. 8–13, 2019, Atlanta: GA.
|
| [34] |
Zhang B, Sun JQ, Wang Y, et al. Site-specific PEGylation of interleukin-2 enhances immunosuppression via the sustained activation of regulatory T cells. Nat Biomed Eng, 2021, 5(11): 1288-1305. DOI:10.1038/s41551-021-00797-8
|
| [35] |
Tchao N, Gorski KS, Yuraszeck T, et al. Amg 592 is an investigational IL-2 mutein that induces highly selective expansion of regulatory T cells. Blood, 2017, 130(Suppl_1): 696. DOI:10.1182/blood.V130.Suppl_1.696.696
|
| [36] |
Sundy JS. Otipoby KL, Higginson-Scott N, et al. ab0282 safety, tolerability and selective expansion of regulatory t cells by a single dose of the novel il-2 mutein Pt101 in a phase 1 study in healthy volunteers. Ann Rheum Dis, 2021, 80(Suppl 1): 1167.1-1167. DOI:10.1136/annrheumdis-2021-eular.1200
|
| [37] |
Peterson LB, Bell CJM, Howlett SK, et al. A long-lived IL-2 mutein that selectively activates and expands regulatory T cells as a therapy for autoimmune disease. J Autoimmun, 2018, 95: 1-14. DOI:10.1016/j.jaut.2018.10.017
|
| [38] |
Stremska ME, Jose S, Sabapathy V, et al. IL233, A novel IL-2 and IL-33 hybrid cytokine, ameliorates renal injury. J Am Soc Nephrol, 2017, 28(9): 2681-2693. DOI:10.1681/ASN.2016121272
|
| [39] |
Stremska ME, Dai C, Venkatadri R, et al. IL233, an IL-2-IL-33 hybrid cytokine induces prolonged remission of mouse lupus nephritis by targeting Treg cells as a single therapeutic agent. J Autoimmun, 2019, 102: 133-141. DOI:10.1016/j.jaut.2019.05.005
|
| [40] |
Venkatadri R, Sabapathy V, Dogan M, et al. Hybrid cytokine IL233 renders protection in murine acute graft vs host disease (aGVHD). Cell Immunol, 2021, 364: 104345. DOI:10.1016/j.cellimm.2021.104345
|
| [41] |
Silva DA, Yu S, Ulge UY, et al. De novo design of potent and selective mimics of IL-2 and IL-15. Nature, 2019, 565(7738): 186-191. DOI:10.1038/s41586-018-0830-7
|
| [42] |
Naing A, Callahan M, Costello B, et al. 509 A first-in-human phase 1 study of NL-201 in patients with relapsed or refractory cancer. J Immunother Cancer, 2021, 9(suppl 2): A540. DOI:10.1136/jitc-2021-SITC2021.509
|
| [43] |
Mullard A. Restoring IL-2 to its cancer immunotherapy glory. Nat Rev Drug Discov, 2021, 20(3): 163-165. DOI:10.1038/d41573-021-00034-6
|
 2022, Vol. 38
2022, Vol. 38




